
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
История создания квантовой механики
1. 1900 год. Макс Планк решает задачу теплового излучения и предлагает заменить непрерывное множество значений энергии дискретным множеством. Вводит понятие кванта энергии: h n. По Планку энергия излучения может принимать значения кратные частоте:
(где n – частота излучения, равная ω/2π; ω – угловая частота). Постоянная Планка h = 6,626•10-34 Дж с. Если пользоваться угловой частотой ω, то постоянная Планка выражается как: ħ = h/2p. При этом выполняется равенство: h n = ħ ω. 2. 1905 год. Эйнштейн выдвигает гипотезу: «Свет также имеет квантовую природу и является потоком световых квантов-фотонов с энергией: Согласно, теории относительности: полная энергия E любой частицы, с массой m, движущейся со скоростью v, равна:
Для фотона: v=c. Отсюда следует, что фотон не имеет массы покоя. 3. 1913 год. Нильс Бор формулирует 2 постулата атомно-молекулярной физики: 1.) Атомная структура устойчива только для определенной совокупности дискретных стационарных состояний; 2.) Способность атома (молекулы) поглощать и испускать излучение подчиняется закону: где ω – частота излучения. Бор предположил, что момент импульса M электрона в атоме водорода равен: 4. 1924 год. Луи де Бройль высказал гипотезу, что соотношение:
где 5. 1927-1932 годы. Джон фон Нейман завершил математическую формулировку квантовой механики на языке гильбертова пространства (линейного векторного, со скалярным произведением). Элементами этого пространства являются волновые функции, описывающие состояние квантовой системы. На основе идеи квантования атомной системы, используя постоянную Планка - ħ, массу m и заряд e электрона, удалось вычислить радиус r1, первой орбиты электрона, в теории Бора:
Гейзенберг опубликовал соотношение неопределенности в атомных системах: 1.) Точность одновременного определения координат и импульса частицы не может превосходить величины ħ: 2.) Точность определения энергии E, за промежуток времени Δt, не может превосходить величины ħ: Эти неопределенности связаны с воздействием на объект при измерении.
Основные понятия и математический аппарат квантовой механики
В квантовой механике, в силу соотношения неопределенности Гейзенберга, классические определения координат, импульса, энергии частиц теряют смысл. Вводится волновая функция Ψ(r, t), являющаяся комплексной величиной, позволяющая вычислить остальные характеристики частицы. Волновая функция - Ψ(r, t), позволяет находить вероятностные характеристики всех параметров микрочастиц. Квадрат модуля волновой функции | Ψ |2, для элемента пространства, объемом dV, определяет вероятность нахождения микрочастицы в данном объеме:
где Ψ* - комплексно-сопряженная волновая функция. Отсюда, функция плотности вероятности (вероятность нахождения микрочастицы в единице объема) P, будет равна:
Функция плотности вероятности должна удовлетворять условиям нормировки:
где интеграл берется по всему пространству, где Ψ ≠ 0. Теперь, вероятность dP нахождения частицы в интервале (X, X+dX) будет равна: Среднее значение координаты - Xср частицы, определяется как
В общем случае, среднее значение любой функции fср(X), находится по аналогичной формуле:
|
|||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 73; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.147.81.214 (0.008 с.) |
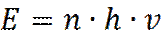
 .»
.» (1)
(1)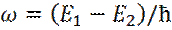 , (2)
, (2) . (3)
. (3) (4)
(4)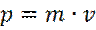 - импульс частицы.
- импульс частицы.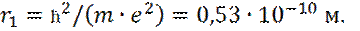 (5)
(5)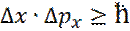 ;
;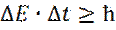 .
. (6)
(6)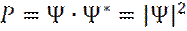 (7)
(7) , (8)
, (8)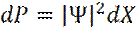 . (9)
. (9)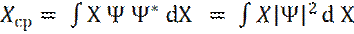 (10)
(10)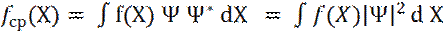 (11)
(11)


