
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Лабораторно-практическим занятиям
Направление подготовки 21.03.01«Нефтегазовое дело»
Нижневартовск 2020
ББК К Печатается по постановлению Редакционно-издательского совета Нижневартовского государственного университета
Рецензент канд.техн.наук, доцент (кафедра
Шатило С.П., Родионцев Н.Н., КучеровС.В., Кочина Т.Б.
ISBN Методические указания к лабораторным и практическим занятиям по дисциплине «Противокоррозионная защита» предназначены для студентов, обучающихся по направлению подготовки «Нефтегазовое дело». Методические указания содержат основные положения изучаемой дисциплины. Приводится перечень лабораторно-практических работ и порядок их выполнения.
ББК ISBN
© Шатило С.П., Родионцев Н.Н., Кучеров С.В., Кочина Т.Б. © НВГУ 2020
Содержание ВВЕДЕНИЕ ……………………………………………………………………….4
Лабораторная работа №1 «ВЛИЯНИЕ ВНЕШНИХ И ВНУТРЕННИХ ФАКТОРОВ НА СКОРОСТЬ КОРРОЗИИ»……………………………………………………………………… 5 Лабораторная работа №2 «КОРРОЗИЯ МЕТАЛЛОВ С КИСЛОРОДНОЙ ДЕПОЛЯРИЗАЦИЕЙ»…….15
Лабораторная работа №3 «ИЗМЕРЕНИЕ РАЗНОСТИ ПОТЕНЦИАЛОВ…МЕЖДУ ТРУБОЙ И ЗЕМЛЕЙ"……………………………………………………………………….…. 26
Лабораторная работа №4 «ОПРЕДЕЛЕНИЕ УДЕЛЬНОГО СОПРОТИВЛЕНИЯ ГРУНТОВ» …….........31
Лабораторная работа №5 «ПРОТЕКТОРНАЯ ЗАЩИТА МАГИСТРАЛЬНЫХ ТРУБОПРОВОДОВ»…..35 Лабораторная работа №6 «ЗАЩИТА ОТ КОРРОЗИИ СТЕКЛОЭМАЛЕВЫМ И ЭПОКСИДНЫМИ ПОКРЫТИЯМИ»…… …………………………………………………………….41
Лабораторная работа №7 «ОПРЕДЕЛЕНИЕ КАЧЕСТВА ЛАКОКРАСОЧНОГО ПОКРЫТИЯ ЭЛЕКТРОХИМИЧЕСКИМ МЕТОДОМ»………………….........................….48
Лабораторная работа №8 «ЗАЩИТА МЕТАЛЛОВ ОТ КОРРОЗИИ С ПОМОЩЬЮ ИНГИБИТОРОВ» …54 Глоссарий...................................................................................................................64 Вопросы к экзамену (зачету) …………………………………………………….67 Список рекомендуемой литературы …………………………………………....70
ВВЕДЕНИЕ Одной из основных проблем, стоящих перед человечеством, является экономия природных ресурсов, поиски их заменителей. Поэтому особенно остро ощущаются убытки, приносимые коррозией. Во всех промышленно - развитых странах они составляют 5 - 10% от национального дохода страны. Основные потери от коррозии - преждевременный выход из строя металлоконструкций, стоимость изготовления которых значительно больше стоимости использованного металла. Вторая крупнейшая статья расхода - проведение комплекса мероприятий по борьбе с коррозией. Это применение средств и методов химической защиты, нанесение различных покрытий, использование смазок и ингибиторов коррозии, дорогостоящих высоколегированных металлов. Трубопроводы, резервуары, нефтепромысловые объекты и оборудование перекачивающих станций в процессе эксплуатации подвергаются процессу коррозии. Коррозия металлических сооружений приводит к преждевременному износу агрегатов, установок, линейной части магистральных трубопроводов, сокращению межремонтных сроков оборудования. Кроме того, коррозия металла может оказаться причиной аварии на магистральном трубопроводе вследствие сквозной перфорации (свищей) стенок трубопроводов. При проектировании и строительстве электрохимической защиты металлических сооружений от коррозии приходится решать комплекс задач, включающий определение коррозионной активности грунта и возможной скорости коррозии, оптимальной степени защиты, выбор средств защиты и в зависимости от них расчет протяженности защитной зоны, размещение средств защиты и их резервирование; при эксплуатации состояния электрохимзашиты, в зависимости от эксплуатации параметров системы, прогнозирование возможностей работы оборудования и его защиты, определение направлений повышения эффективности работы оборудования электрохимзащиты. Поэтому проблемы возникновения коррозии и её предотвращения имеют огромное значение, возрастающее по мере прогресса в различных отраслях промышленности.
Лабораторная работа №1
Цель работы: изучение коррозионного поведения металлов и их сплавов в растворах кислот с разной концентрацией, а также влияние химического состава и структуры материала на скорость коррозии.
Основные положения
1 .Изучить влияние внешних и внутренних факторов на скорость коррозии. Коррозией называется разрушение материала в результате химического или электрохимического взаимодействия его с окружающей внешней средой. В зависимости от механизма коррозионной реакции различают химическую и электрохимическую коррозию. По характеру разрушения поверхности коррозия подразделяется на сплошную и местную. Сплошная коррозия может быть равномерной (разрушается на одинаковую глубину по всей поверхности) и неравномерной (глубина разрушения по поверхности разная). Местная коррозия включает в себя: коррозию пятнами, язвами, точечную, сквозную, подслойную и межкристаллитную. В зависимости от вида коррозионной среды различают атмосферную коррозию, подземную коррозию, микробиологическую, морскую, кислотную, щелочную и другие. По характеру дополнительных воздействий коррозионные разрушения подразделяются на коррозионную усталость, коррозионное растрескивание, коррозию при трении, кавитационную коррозию, эрозию. Скорость протекания коррозионных процессов зависит от внутренних и внешних факторов. Внутренние факторы характеризуют состояние материала. К ним относятся: положение в периодической системе Д. И. Менделеева, термодинамическая устойчивость, химический состав и структура материала, наличие внутренних напряжений и характер обработки поверхности материала. Положение элемента в периодической системе не позволяет охарактеризовать во всех случаях коррозионную стойкость металла. Тем не менее в отношении коррозионного поведения наблюдаются достаточно определённые закономерности, аналогичные закономерностям химических свойств. Наиболее коррозионно неустойчивые металлы находятся в левых подгруппах 1 и 11 групп. В правых подгруппах 1 и 11 групп, как и в других группах, коррозионная стойкость растёт по мере возрастания атомного номера (Си - Ag - Аu, Zn - Cd - Hg, Ni - Pd - Pt). В левых подгруппах IV, VI
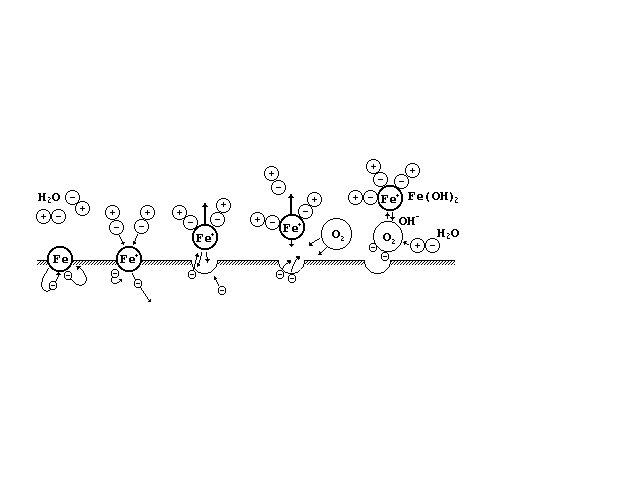
групп и в VIII группе находятся легко пассивирующиеся металлы, причём с ростом атомного номера склонность к пассивации в первом приближении падает (Ti - Zr - Hf, Cr - Mo - W). Термодинамическая устойчивость металла характеризуется величиной его стандартного потенциала. И вес же алюминий (φо = -1,67 в) устойчив в разбавленной серной кислоте, а железо (φо = -0,44 в) неустойчиво. Магний (φо = -2,34 в) не корродирует в плавиковой кислоте, а олово (φо = -0,13 в) корродирует. Следовательно, соотношение стандартных потенциалов металлов не позволяет безоговорочно судить об их коррозионных свойствах. Это связано, во-первых, с тем, что условия протекания реального процесса всегда отличаются от стандартных условий. Во-вторых, невозможность прогнозирования уровня коррозионной стойкости заключается в наличии многих кинетических факторов, которые могут сильно повлиять на скорость коррозии. И, в-третьих, чистые металлы в технике применяются крайне редко. Пусть будет только вода и кислород. Одна из удивительных особенностей молекулы воды - ее дипольные свойства. Несмотря на уравновешенность зарядов Н+ и OH- внутри молекулы, вода - полярно заряженная частица, способная притягиваться к положительно или отрицательно заряженным ионам окружающей среды, например, к ионам железа (Рис.1).
Атомы металла образуют кристаллическую решетку, в пространстве которой свободно перемещаются электроны, покинувшие свои атомы, - так называемые, валентные электроны, что и показано на (Рис.1.), как первое событие процесса коррозии. Неуравновешенный ионизированный атом металла Fe+ - до тех пор, пока он лишен электрона - является слабым местом решетки. Если этот ион доступен для атаки молекул воды, например, он находится на самой поверхности металла, а лучше - на вершине гребня или неровности поверхности, то вступают в действие электростатические силы притяжения. Окружая ион металла, молекулы воды - в силу своей подвижности - способны расшатать решетку и отделить ион. Не будь противодействия такому началу, кристаллическая решетка быстро бы разрушилась. Противодействие процессу “растаскивания” организует фронт валентных электронов - облако свободно странствующих отрицательно заряженных частиц. Электроны, лишенные материнских сил поддержки со стороны своих атомов, ушедших в раствор, собираются вблизи границы металл-электролит, пытаясь вернуться к брошенным ими ранее частицам металла.
Рис.1. Этапы развития коррозионного процесса под действием воды и кислорода
Начинается перетягивание кто-кого: электроны - в одну сторону, вода - в другую. Если процесс возврата ионов металла идет с такой же скоростью, что и процесс их ухода “в воду”, то на границе устанавливается динамическое равновесие без каких либо материальных потерь. Возникает так называемый ток обмена и формируется двойной электрический слой: его внешней обкладкой являются гидратированные ионы металла, внутренней - электроны. Однако равновесие может быть нарушено, если вмешается третья сила, способная благоприятствовать тому или противоположному фронту на двойном слое. Такая сила исходит от молекулы кислорода, которая подобно молекуле воды, являясь в целом нейтральной, но способна, что весьма удивительно при ее электронейтральности, притягивать к себе электроны. В данной ситуации агрессоры поделили сферу деятельности: воде - положительно заряженная частица металла, кислороду - отрицательная.
Кислород ассимилирует электрон и образует вне пределов металла некоторую отрицательно заряженную частицу. Связывая электрон, кислород, таким образом, облегчает работу молекулам воды, которые теперь уже безпрепятственно отрывают, нейтрализуют и безвозвратно уносят ион металла. Разрушение - свершившийся факт. Таким образом, для безостановочного протекания процесса разрушения достаточно воды и кислорода. Для того, чтобы лучше понять каким образом при помощи окраски можно защитить металл от коррозии, нужно познакомиться с четырьмя основными предпосылками для коррозии. Они таковы: – катод, или электрод, на котором происходит катодная реакция. – анод, или электрод, на котором происходит анодная реакция. – проводник электронов – проводник ионов Проводник электронов – это металл, проводящий электрический ток. Проводник ионов – это проводящая электрический ток жидкость или электролит. Электроды, или анод и катод, являются электронными проводниками, которые соприкасаются с проводниками ионов. В проводнике ионов или электролите при известном соотношении на них возникает соответствующий электрический потенциал или электрическое напряжение. Когда электроды соприкасаются между собой, то разность между электродными потенциалами действует как возбудитель коррозионной реакции. Образуется коррозионная пара, в которой один из электродов (анод) является разъедающим металл. Коррозия металла или разъедание (разрушение) происходит таким образом, что атом металла, растворяясь в электролите, на аноде электрически повреждается и выделяет ионную частицу. Одновременно происходит освобождение электронов, которые проходят сквозь металл (проводник электронов) на катод. Это и есть так называемая анодная реакция, при которой положительные заряды из металла переходят в раствор, и происходит процесс окисления, который можно изобразить так:
Анодная реакция: Ме → Меn+ + ne-
Если речь идет о железе (стали), то можно написать так:
Fe (железо) → Fe2+(ион железа) + 2е- (электрон)
На катоде электроны вступают в реакцию с кислородом (О2) и водой (Н2О) электролита (Рис.2). В так называемой катодной реакции отрицательный заряд переходит из металла в электролит. Катодная реакция является процессом очищения. Когда речь идет о железе, катодную реакцию можно изобразить таким образом:
Катодная реакция:
2е- + ½О2 + Н2О → 2OH- (ион гидроксида)
В электролите ионы железа и гидроксида вступают в реакцию между собой так, образуя гидроксид закиси железа: Электролитическая реакция: Fe2+ + 2OH- → Fe (OH)2 (гидроксид закиси железа) Гидроксид закиси железа далее вступает в реакцию с водой и кислородом, когда и образуется продукт коррозии железа или ржавчина (Fe2О3 n Н2О).
При действии коррозионной пары электродные реакции вызывают коррозионный ток, который и производит коррозию или разрушение. Если такой коррозионный ток можно ”выключить” в любой точке коррозионной пары, то коррозия прекратится.
На поверхности стали всегда присутствуют, по меньшей мере, три из четырех предпосылок для коррозии: анод, катод и проводник электронов (металл). В качестве электропроводящей жидкости, или электролита, выступает вода. Водяной пар, содержащийся в воздухе, покрывает поверхность металла тонкой водяной пленкой. Но основное значение для коррозии имеет момент начала превращения (конденсация) пара в жидкость. На чистых гладких поверхностях это происходит при достижении 100% относительной влажности воздуха, например, при снижении температуры до точки росы. На неочищенных поверхностях конденсация может происходить и раньше. Такую величину относительной влажности воздуха, при которой на поверхности металла образуется разъедающая пленка жидкости, называют критической влажностью. Критическая влажность воздуха для коррозии металла, составляет ~ 60-70%. Обычный способ замедлить коррозию – это изолировать поверхность металла от электролита, то есть от влаги. У антикоррозионных лакокрасочных покрытий имеются и другие механизмы замедления коррозии. Химический состав сплава также влияет на скорость коррозии. Чем чище металл, т. е. чем меньше содержится в нем примесей, тем ниже скорость коррозии. В сплавах же, содержащих легирующие элементы, повышающие их коррозионную стойкость, скорость коррозии уменьшается с ростом процентного содержания данных элементов. В зависимости от структуры сплавы подразделяются на многофазные и однофазные. В многофазных сплавах типа «механическая смесь» скорость коррозии будет определяться как весовым соотношением, так и взаимным расположением фаз, выполняющих роль катода и анода. Если фазы распределены равномерно и доля анодной составляющей невелика, то коррозия будет сплошной и непродолжительной. При неравномерном распределении анодной фазы коррозия будет местной и длительной, а очаги коррозии могут при этом распространяться в глубину, что очень опасно. В однофазных сплавах типа «твёрдый раствор» скорость коррозии находится не в прямой зависимости от состава сплава, а меняется скачкообразно по правилу порогов устойчивости, разработанному Тамманом. Это правило, называемое также правилом n/8, гласит, что при легировании менее электроположительного металла более электроположительным (более благородным) скорость коррозии будет снижаться скачкообразно по мере добавления количества кратного n/8 атомной доли более благородного металла.
Рис. 2.Графическое изображение пространственной пары и ее действия в наполненных водой
При этом равновесный потенциал сплава также повышается ступенчато, приближаясь к потенциалу чистого более благородного металла. Однако это не означает, что любой однофазный сплав при изменении его состава имеет вес 8 порогов устойчивости. Количество порогов устойчивости и их значение зависит от природы металлов и степени агрессивности среды. Объясняя причины возникновения порогов устойчивости, Тамман высказал предположение о том, что атомы более благородного металла блокируют атомы корродирующего металла. Внутренние напряжения могут появиться в материале вследствие проведения термической обработки и в процессе изготовления деталей. Чем выше количество этих напряжений, тем больше скорость коррозии. Характер обработки поверхности изделий также влияет на скорость коррозии. Различают грубую и тонкую обработки поверхности. Грубая обработка включает в себя пескоструйную, (обработка с помощью металлических щёток), обработка напильником и др. Тонкая обработка состоит из шлифовки и полировки поверхности. Чем выше степень чистоты обработки, тем выше коррозионная стойкость изделий за счёт удаления неровностей, где могла бы скапливаться агрессивная среда. Внешние факторы характеризуют состояние коррозионной среды. К ним относятся: pH коррозионной среды, температура, давление, концентрация растворенного кислорода, состав и концентрация нейтральных растворов, скорость движения среды относительно металла.
При уменьшении pH раствора активность ионов Н+ возрастает и, как правило, возрастает скорость коррозии. Однако это возможно только в тех случаях, когда агрессивная среда не оказывает пассивирующего действия и не приводит к образованию на поверхности металла защитной плёнки. Природа металла также достаточно чётко проявляется во влиянии pH на скорость коррозии. По характеру этой зависимости при комнатной температуре металлы можно разбить на 5 групп. К первой группе - относятся благородные металлы (Ag, Au, Pt и др.) и в известной мере титан, на коррозию которых pH не оказывает влияния. Ко второй группе - металлы неустойчивые в кислых и щелочных средах и устойчивые в нейтральных (Al, Zn, Sn, Pb). К третьей группе - металлы неустойчивые в кислых средах и стойкие в щелочных (Ni, Со, Cd). К четвертой группе - металлы неустойчивые в щелочных средах и стойкие в кислых (Mo, W, Та). К пятой группе - металлы неустойчивые в кислых средах, слабоустойчивые в нейтральных и стойкие в щелочных (Fe, Cr, Си, Mn, Mg). ЕСЛИ коррозия протекает с водородной деполяризацией, то рост температуры увеличивает скорость коррозии. Это объясняется снижением перенапряжения выделения водорода, ускорением диффузии и уменьшением электросопротивления среды. При коррозии с кислородной деполяризацией с ростом температуры скорость коррозии будет замедляться, так как она зависит от концентрации кислорода. При повышении температуры растворимость кислорода снижается в растворах, и это обстоятельство является решающим. Однако если система закрытая, то скорость коррозии будет возрастать, как и при коррозии с водородной деполяризацией. Увеличение давления приводит к повышению скорости коррозии вследствие увеличения растворимости газов в коррозионной среде и возникновения внутренних напряжений в металле. Существенное влияние па скорость коррозии оказывает концентрация растворенного в среде кислорода. Кислород может выступать либо в роли пассиватора, либо в роли деполяризатора. Если кислород выступает в роли пассиватора, то сначала скорость коррозии возрастает из-за потерь металла, вызванного образованием окисной плёнки, а затем при некоторой концентрации кислорода, когда вся поверхность покроется окисной плёнкой, скорость коррозии будет падать. Если кислород выступает в роли деполяризатора, то скорость коррозии будет расти по линейной зависимости с увеличением количества растворенного кислорода.
Влияние скорости движения раствора на скорость разрушения металла наиболее сильно проявляется при коррозии с кислородной деполяризацией. Движение раствора способствует повышению концентрации кислорода в приэлектродном слое, а также удалению продуктов коррозии, способных пассивировать поверхность. Все это увеличивает скорость коррозии. При значительных скоростях возможна и пассивация поверхности за счёт слишком высокой концентрации кислорода. Наконец, при ещё большем повышении скорости движения среды появляются очаги коррозионной эрозии как результат комбинированного воздействия процессов электрохимического и механического разрушения металла. Влияние нейтральных солей на скорость коррозии проявляется через свойства образующихся продуктов коррозии. При образовании труднорастворимых соединений происходит частичное или полное экранирование поверхности металла и скорость коррозии падает. Соли могут образовывать на металле и окисные плёнки, пассивирующие поверхность. Чаще всего в нейтральных растворах коррозия протекает с кислородной деполяризацией. При повышении концентрации нейтральной соли до некоторых значений наблюдается рост коррозии вследствие увеличения электропроводности раствора, а затем уменьшение коррозии из-за снижения растворимости кислорода, участвующего в катодной реакции.
2. Проведение лабораторной работы Приборы и материалы: - аналитические весы; - фарфоровые стаканы; - кислоты разной концентрации; - образцы материала с различным химическим составом и структурой; - сушильный шкаф; - штангенциркуль; - металлические крючки; - наждачная бумага.
Описание работы: испытания проводят на 6-ти образцах (по три образца на каждую марку сплава). Сначала их зачищают наждачной бумагой, затем измеряют длину, ширину и толщину с помощью штангенциркуля и протирают смоченной в бензине фильтровальной бумагой. Подготовленные образцы взвешивают на аналитических весах с точностью до четвёртого знака после запятой. Взвешенные образцы на металлических крючках погружают в фарфоровые стаканы и наливают в них кислоту согласно индивидуального задания.
Образцы выдерживают в растворах в течение 50 минут, после чего тщательно промывают под струёй холодной воды и подсушивают в сушильном шкафу при температуре 90°С в течении 1-2-х минут. Сухие образцы охлаждают на воздухе до комнатной температуры и вновь взвешивают на аналитических весах. Скорость коррозии определяют по формуле:
где ∆ т - весовые потери металла, вычисляемые по разнице взвешивания до и после проведения опыта, г; S - площадь поверхности образца, м2; τ - время испытания, ч. Глубинный показатель коррозии определяют по формуле:
где K - скорость коррозии, г/м2 -ч; ρ - плотность металла, г/см3; 8,76 - переводной коэффициент. Оформление результатов работы: все данные представляются в виде таблицы 1, а также строятся графики, показывающие зависимость глубинного показателя коррозии от концентрации кислоты для двух марок сплава. В выводе делается заключение о влиянии концентрации кислоты, химического состава и структуры сплава. Балл коррозионной стойкости определяется по ГОСТ 13819.
Результаты лабораторно-практической работы Таблица 1
Требование к отчету: Отчет по выполненной работе должен содержать: 1. Название лабораторной работы и ее цель. 2. Схема лабораторной установки, ее описание. 3. Таблицу измеренных и рассчитанных параметров. 4. Анализ полученных результатов.
Контрольные вопросы 1. Классификация коррозионных разрушений. 2. Влияние внешних факторов на скорость коррозии. 3. Влияние внутренних факторов на скорость коррозии. 4. Показатели скорости коррозии. 5. Этапы развития коррозионного процесса под действием воды и кислорода. Лабораторная работа №2 «КОРРОЗИЯ МЕТАЛЛОВ С КИСЛОРОДНОЙ ДЕПОЛЯРИЗАЦИЕЙ» Цель работы: изучение влияния доступа кислорода на скорость протекания коррозии с кислородной деполяризацией.
Основные положения
|
||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 50; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.17.175.21 (0.116 с.) |
|||||||||||||||||||||||||||||||||||||||


 T HIzUA44J7jqZZ9laOmw5NVjs6dVSczleXXrj852/fKgv5o3yzWjqpV3tO6WeHqeXZxCRpng//k9/ aAX5Cv62JADI8hcAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAA AAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAA AAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQBgVtIRwgAAANsAAAAPAAAA AAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA9gIAAAAA " adj="0,,0" path="m29,l5,r,12l24,12,41,36r17,5l48,43,34,53,,87r27,l53,60,67,48r75,l127,41r8,-2l79,39,70,36,65,34,41,7,29,xm103,48r-24,l79,87r24,l103,48xm142,48r-31,l125,53r31,34l183,87,142,48xm103,l79,r,39l103,39,103,xm178,l163,,144,5,130,24,118,36r-15,3l135,39r7,-3l161,15r17,-3l178,xe" fillcolor="black" stroked="f"> D mGRbSd3iOcFdLSdZ9iIdWk4LBht6M1T+7k5Owbt7PsrL4cPaq9mvcu+3plp2Sg2e+uUriEh9vIf/ 2xutYDKFvy/pB8j5DQAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAA AAAAAAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsA AAAAAAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAMEzrTvEAAAA2wAAAA8A AAAAAAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD4AgAAAAA= " adj="0,,0" path="m65,l31,5,19,12,7,21,3,33,,45,3,60r4,9l19,79r12,5l48,89r19,2l96,86r12,-2l113,79r-46,l55,77,46,74,31,65,27,57,24,50r106,l130,45r-1,-7l27,38r,-7l31,24,46,14r9,l65,12r46,l99,5,84,2,65,xm111,60r-8,l99,67r-3,2l89,74r-7,3l75,77r-8,2l113,79,123,69r4,-7l123,62,111,60xm111,12r-46,l77,14r10,3l94,21r5,3l103,31r,7l129,38r-2,-7l120,21r-9,-9xe" fillcolor="black" stroked="f"> E 6UqpHd4i3DQyTZKJNFhzXKiwpXVFxe/xYhSccHPO6cPt33d5Pvm/pNt69dko9TboVl8gAnXhFX62 v7WCdAqPL/EHyMUdAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAA AAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAA AAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAyME7KMMAAADbAAAADwAA AAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPcCAAAAAA== " adj="0,,0" path="m24,60l,65r7,9l26,86r29,5l77,89,93,84r5,-5l57,79,45,77,36,74,24,60xm94,12r-39,l72,17r7,9l77,31r-8,5l43,38r,12l69,50r15,7l81,69r-9,8l57,79r41,l103,74r5,-9l103,53,86,43r15,-7l103,26r-2,-9l94,12xm55,l29,5,12,14,5,24r21,2l38,17,55,12r39,l84,5,55,xe" fillcolor="black" stroked="f"> U 2ga8pnDX6VmWzbXDllNDgz29NlR9H36cgQ/7vt8FCS9P23K+O8dS8vxhYcz4fnheghIa5Cb+d79Z A7M0Nn1JP0Cv/wAAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAA AAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAA AAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQAcOtXbwgAAANsAAAAPAAAA AAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA9gIAAAAA " adj="0,,0" path="m65,l48,2,34,5,22,9,7,19,,31,,57,7,69,17,79,46,89r19,2l77,89r12,l98,84r10,-3l112,79r-47,l55,77,43,74,29,65,24,55r,-19l29,26,43,17,55,14,65,12r48,l98,5,84,2,65,xm113,12r-48,l77,14r9,3l101,26r5,10l106,55r-5,10l86,74r-9,3l65,79r47,l115,77r7,-8l127,62r3,-7l132,43,130,31,122,21r-9,-9xe" fillcolor="black" stroked="f">
T HIzUA44J7jqZZ9laOmw5NVjs6dVSczleXXrj852/fKgv5o3yzWjqpV3tO6WeHqeXZxCRpng//k9/ aAX5Cv62JADI8hcAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAA AAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAA AAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQBgVtIRwgAAANsAAAAPAAAA AAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA9gIAAAAA " adj="0,,0" path="m29,l5,r,12l24,12,41,36r17,5l48,43,34,53,,87r27,l53,60,67,48r75,l127,41r8,-2l79,39,70,36,65,34,41,7,29,xm103,48r-24,l79,87r24,l103,48xm142,48r-31,l125,53r31,34l183,87,142,48xm103,l79,r,39l103,39,103,xm178,l163,,144,5,130,24,118,36r-15,3l135,39r7,-3l161,15r17,-3l178,xe" fillcolor="black" stroked="f"> D mGRbSd3iOcFdLSdZ9iIdWk4LBht6M1T+7k5Owbt7PsrL4cPaq9mvcu+3plp2Sg2e+uUriEh9vIf/ 2xutYDKFvy/pB8j5DQAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAA AAAAAAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsA AAAAAAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAMEzrTvEAAAA2wAAAA8A AAAAAAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD4AgAAAAA= " adj="0,,0" path="m65,l31,5,19,12,7,21,3,33,,45,3,60r4,9l19,79r12,5l48,89r19,2l96,86r12,-2l113,79r-46,l55,77,46,74,31,65,27,57,24,50r106,l130,45r-1,-7l27,38r,-7l31,24,46,14r9,l65,12r46,l99,5,84,2,65,xm111,60r-8,l99,67r-3,2l89,74r-7,3l75,77r-8,2l113,79,123,69r4,-7l123,62,111,60xm111,12r-46,l77,14r10,3l94,21r5,3l103,31r,7l129,38r-2,-7l120,21r-9,-9xe" fillcolor="black" stroked="f"> E 6UqpHd4i3DQyTZKJNFhzXKiwpXVFxe/xYhSccHPO6cPt33d5Pvm/pNt69dko9TboVl8gAnXhFX62 v7WCdAqPL/EHyMUdAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAA AAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAA AAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAyME7KMMAAADbAAAADwAA AAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPcCAAAAAA== " adj="0,,0" path="m24,60l,65r7,9l26,86r29,5l77,89,93,84r5,-5l57,79,45,77,36,74,24,60xm94,12r-39,l72,17r7,9l77,31r-8,5l43,38r,12l69,50r15,7l81,69r-9,8l57,79r41,l103,74r5,-9l103,53,86,43r15,-7l103,26r-2,-9l94,12xm55,l29,5,12,14,5,24r21,2l38,17,55,12r39,l84,5,55,xe" fillcolor="black" stroked="f"> U 2ga8pnDX6VmWzbXDllNDgz29NlR9H36cgQ/7vt8FCS9P23K+O8dS8vxhYcz4fnheghIa5Cb+d79Z A7M0Nn1JP0Cv/wAAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAA AAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAA AAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQAcOtXbwgAAANsAAAAPAAAA AAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA9gIAAAAA " adj="0,,0" path="m65,l48,2,34,5,22,9,7,19,,31,,57,7,69,17,79,46,89r19,2l77,89r12,l98,84r10,-3l112,79r-47,l55,77,43,74,29,65,24,55r,-19l29,26,43,17,55,14,65,12r48,l98,5,84,2,65,xm113,12r-48,l77,14r9,3l101,26r5,10l106,55r-5,10l86,74r-9,3l65,79r47,l115,77r7,-8l127,62r3,-7l132,43,130,31,122,21r-9,-9xe" fillcolor="black" stroked="f"> 
 2 PT4k3Ld6nmUL7bFhaXDY0c5RdT3cvPS+7d1W77e7EE6LdHS3y3NG78ZMxsNmBSrRkP7Ff+5Pa+BV 1ssX+QG6/AUAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAAAAAA AAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAAAAAA AAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQD3nWqUvwAAANsAAAAPAAAAAAAA AAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA8wIAAAAA " adj="0,,0" path="m24,55l,57,8,72r12,9l39,88r48,l108,79r2,-3l60,76,41,74,32,69,24,55xm106,12r-38,l82,14,94,26r5,12l48,38r,12l99,50,92,67,75,76r35,l120,62r3,-17l118,26,106,12xm60,l39,2,22,7,5,21,3,26r24,2l39,16r9,-4l106,12,84,2,60,xe" fillcolor="black" stroked="f"> i iLIppG6wjXBbydckGUmLJccFgzV9GMr/NierIHGcZ+vLwbSLY5at9tvf8W7ypVTvqXt/AxGoC/fw rb3UCoYDuH6JP0DO/gEAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAA AAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAAL AAAAAAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQDIvVldxQAAANsAAAAP AAAAAAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA+QIAAAAA " adj="0,,0" path="m24,l,,,86r24,l24,46r38,l45,41,60,36r-36,l24,xm62,46r-31,l43,53,77,86r26,l62,46xm96,l74,,65,5,43,31,33,36r27,l79,12,96,10,96,xe" fillcolor="black" stroked="f"> b 9EHWmdQ1PgLclPItisbSYMFhIceKPnNKb4e7UfC9Oe9ubrK6fOjtMsk2L817spZK9XttMgXhqfXP 8H97rRWMRvD3JfwAOf8FAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAA AAAAAAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAA CwAAAAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAobWGQsYAAADbAAAA DwAAAAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPoCAAAAAA== " adj="0,,0" path="m68,12r-22,l46,86r22,l68,12xm113,l,,,12r113,l113,xe" fillcolor="black" stroked="f"> d QR9kV0rd4RDgppHzKIqlwZrDQoUtbSsqrvnNKPi6nhdZu0in/cFMt7s0/1x+HC9KTZ7G9B2Ep9Hf w//tvVbwGsPfl/AD5PoXAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAA AAAAAAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAA CwAAAAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAu+vcT8YAAADbAAAA DwAAAAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPoCAAAAAA== " adj="0,,0" path="m68,l51,,36,4,24,9,10,19,3,28,,45,3,57r7,12l20,79r12,5l48,88r32,l89,86r12,-2l111,81r5,-5l56,76,46,74,39,69,32,62,27,55r,-22l32,26r7,-7l46,14,56,12r57,l101,4,68,xm113,12r-36,l89,14r7,5l104,26r4,7l108,55r-4,7l96,69r-7,5l77,76r39,l123,69r5,-7l132,52r,-9l130,31,123,19,113,12xe" fillcolor="black" stroked="f"> G fZB9KXWPtwA3rXyMohdpsOawUGFHm4qKZv9tFDRfz/OtfF/kp/zTRG/nLj41H7lSD5NhvQThafD3 8H97qxU8xfD3JfwAmf4CAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAA AAAAAAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAA CwAAAAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEA8MfxnMYAAADbAAAA DwAAAAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPoCAAAAAA== " adj="0,,0" path="m24,l,,,86r24,l24,48r91,l115,36r-91,l24,xm115,48r-24,l91,86r24,l115,48xm115,l91,r,36l115,36,115,xe" fillcolor="black" stroked="f">
2 PT4k3Ld6nmUL7bFhaXDY0c5RdT3cvPS+7d1W77e7EE6LdHS3y3NG78ZMxsNmBSrRkP7Ff+5Pa+BV 1ssX+QG6/AUAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAAAAAA AAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAAAAAA AAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQD3nWqUvwAAANsAAAAPAAAAAAAA AAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA8wIAAAAA " adj="0,,0" path="m24,55l,57,8,72r12,9l39,88r48,l108,79r2,-3l60,76,41,74,32,69,24,55xm106,12r-38,l82,14,94,26r5,12l48,38r,12l99,50,92,67,75,76r35,l120,62r3,-17l118,26,106,12xm60,l39,2,22,7,5,21,3,26r24,2l39,16r9,-4l106,12,84,2,60,xe" fillcolor="black" stroked="f"> i iLIppG6wjXBbydckGUmLJccFgzV9GMr/NierIHGcZ+vLwbSLY5at9tvf8W7ypVTvqXt/AxGoC/fw rb3UCoYDuH6JP0DO/gEAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAA AAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAAL AAAAAAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQDIvVldxQAAANsAAAAP AAAAAAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA+QIAAAAA " adj="0,,0" path="m24,l,,,86r24,l24,46r38,l45,41,60,36r-36,l24,xm62,46r-31,l43,53,77,86r26,l62,46xm96,l74,,65,5,43,31,33,36r27,l79,12,96,10,96,xe" fillcolor="black" stroked="f"> b 9EHWmdQ1PgLclPItisbSYMFhIceKPnNKb4e7UfC9Oe9ubrK6fOjtMsk2L817spZK9XttMgXhqfXP 8H97rRWMRvD3JfwAOf8FAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAA AAAAAAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAA CwAAAAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAobWGQsYAAADbAAAA DwAAAAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPoCAAAAAA== " adj="0,,0" path="m68,12r-22,l46,86r22,l68,12xm113,l,,,12r113,l113,xe" fillcolor="black" stroked="f"> d QR9kV0rd4RDgppHzKIqlwZrDQoUtbSsqrvnNKPi6nhdZu0in/cFMt7s0/1x+HC9KTZ7G9B2Ep9Hf w//tvVbwGsPfl/AD5PoXAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAA AAAAAAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAA CwAAAAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAu+vcT8YAAADbAAAA DwAAAAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPoCAAAAAA== " adj="0,,0" path="m68,l51,,36,4,24,9,10,19,3,28,,45,3,57r7,12l20,79r12,5l48,88r32,l89,86r12,-2l111,81r5,-5l56,76,46,74,39,69,32,62,27,55r,-22l32,26r7,-7l46,14,56,12r57,l101,4,68,xm113,12r-36,l89,14r7,5l104,26r4,7l108,55r-4,7l96,69r-7,5l77,76r39,l123,69r5,-7l132,52r,-9l130,31,123,19,113,12xe" fillcolor="black" stroked="f"> G fZB9KXWPtwA3rXyMohdpsOawUGFHm4qKZv9tFDRfz/OtfF/kp/zTRG/nLj41H7lSD5NhvQThafD3 8H97qxU8xfD3JfwAmf4CAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAA AAAAAAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAA CwAAAAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEA8MfxnMYAAADbAAAA DwAAAAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPoCAAAAAA== " adj="0,,0" path="m24,l,,,86r24,l24,48r91,l115,36r-91,l24,xm115,48r-24,l91,86r24,l115,48xm115,l91,r,36l115,36,115,xe" fillcolor="black" stroked="f"> 
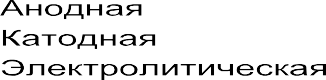 G fZBtIXWLtwA3tZxG0bs0WHFYKLGhTUn5Nfs1CvbXc3xs4nTUHcxos02z3Wx9uij1+tKncxCeev8M /7e/tIL4Ax5fwg+QyzsAAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAA AAAAAAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAA CwAAAAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAUX7vCcYAAADbAAAA DwAAAAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPoCAAAAAA== " adj="0,,0" path="m84,l48,,20,10,10,20,5,32,,46,10,70r10,7l34,84r17,5l84,89,99,87,118,77r-60,l48,75,39,70,32,65,29,58,27,48r105,l132,44r-1,-8l27,36r2,-7l34,22r7,-5l48,15,68,10r45,l101,5,84,xm130,60r-24,l96,70r-4,2l77,77r41,l125,70r5,-10xm113,10r-45,l80,12r9,3l96,20r5,4l104,29r2,7l131,36r-1,-4l123,20,113,10xe" fillcolor="black" stroked="f"> G KNtS6ha7CLe1fErTZ2mx4rhgsKGVoeLncLEKUsdFvr+dTLc+5/n26+N7+jnbKTUa9q8vIAL14R7+ b2+0gskM/r7EHyAXvwAAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAA AAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAAL AAAAAAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQAsjPhqxQAAANsAAAAP AAAAAAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA+QIAAAAA " adj="0,,0" path="m24,l,,,87r24,l24,48r38,l46,44r9,-5l24,39,24,xm62,48r-31,l43,53,77,87r26,l62,48xm98,l74,3,65,8,46,32,34,39r21,l60,36,74,17,84,12r14,l98,xe" fillcolor="black" stroked="f"> U 2uEjwk0jp0kykwZrjgsVtrStqLid70bBKT+ku9rt/3OZdMcUbTG/3VOlRsN+swARqA/f8Kd90Apm E3h/iT9Arl4AAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAAAAAA AAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAAAAAA AAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAtw+vDMAAAADbAAAADwAAAAAA AAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPQCAAAAAA== " adj="0,,0" path="m27,l,,,87r27,l46,70r2,-2l27,68,27,xm118,22r-24,l94,87r24,l118,22xm118,l91,,75,17,43,51,27,68r21,l94,22r24,l118,xe" fillcolor="black" stroked="f">
G fZBtIXWLtwA3tZxG0bs0WHFYKLGhTUn5Nfs1CvbXc3xs4nTUHcxos02z3Wx9uij1+tKncxCeev8M /7e/tIL4Ax5fwg+QyzsAAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAA AAAAAAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAA CwAAAAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAUX7vCcYAAADbAAAA DwAAAAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPoCAAAAAA== " adj="0,,0" path="m84,l48,,20,10,10,20,5,32,,46,10,70r10,7l34,84r17,5l84,89,99,87,118,77r-60,l48,75,39,70,32,65,29,58,27,48r105,l132,44r-1,-8l27,36r2,-7l34,22r7,-5l48,15,68,10r45,l101,5,84,xm130,60r-24,l96,70r-4,2l77,77r41,l125,70r5,-10xm113,10r-45,l80,12r9,3l96,20r5,4l104,29r2,7l131,36r-1,-4l123,20,113,10xe" fillcolor="black" stroked="f"> G KNtS6ha7CLe1fErTZ2mx4rhgsKGVoeLncLEKUsdFvr+dTLc+5/n26+N7+jnbKTUa9q8vIAL14R7+ b2+0gskM/r7EHyAXvwAAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAA AAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAAL AAAAAAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQAsjPhqxQAAANsAAAAP AAAAAAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA+QIAAAAA " adj="0,,0" path="m24,l,,,87r24,l24,48r38,l46,44r9,-5l24,39,24,xm62,48r-31,l43,53,77,87r26,l62,48xm98,l74,3,65,8,46,32,34,39r21,l60,36,74,17,84,12r14,l98,xe" fillcolor="black" stroked="f"> U 2uEjwk0jp0kykwZrjgsVtrStqLid70bBKT+ku9rt/3OZdMcUbTG/3VOlRsN+swARqA/f8Kd90Apm E3h/iT9Arl4AAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAAAAAA AAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAAAAAA AAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAtw+vDMAAAADbAAAADwAAAAAA AAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPQCAAAAAA== " adj="0,,0" path="m27,l,,,87r27,l46,70r2,-2l27,68,27,xm118,22r-24,l94,87r24,l118,22xm118,l91,,75,17,43,51,27,68r21,l94,22r24,l118,xe" fillcolor="black" stroked="f"> 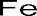 l LEONNtCY4a7DO60LdNRKXmio513D1eX45Qy8oD04P1z0w/7z/WO8X+Jr0GjM9Xx6XIFKPKX/8F/7 2RooCvj9kn8Abn4AAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAA AAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAA AAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAvpDQEMMAAADbAAAADwAA AAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPcCAAAAAA== " adj="0,,0" path="m84,l48,,31,5,17,10,7,20,3,32,,46,3,58,7,70r10,7l31,84r17,5l82,89,96,87r12,-5l115,77r-60,l46,75,31,65,27,58,24,48r106,l130,44r-2,-8l27,36r,-7l31,22r8,-5l46,15,65,10r46,l99,5,84,xm127,60r-24,l94,70r-5,2l75,77r40,l123,70r4,-10xm111,10r-46,l77,12r10,3l96,20r3,4l103,29r,7l128,36r-1,-4l123,20,111,10xe" fillcolor="black" stroked="f"> G KOtc6hrbCLelnCTJTFosOC4YrGhjKPs736yC3edue7TBN8XBtJcs2d9Ogykp1X/v1l8gAnXhFX62 v7WC2RweX+IPkMt/AAAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAA AAAAAAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsA AAAAAAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAAbqx+DEAAAA2wAAAA8A AAAAAAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD4AgAAAAA= " adj="0,,0" path="m74,48r-24,l50,80r24,l74,48xm127,34l,34,,48r127,l127,34xm74,l50,r,34l74,34,74,xe" fillcolor="black" stroked="f"> M 0tdSe7wnuG1lnmWFtNhwWjDY0dpQ9XO4WgXfcnPOj6+658eHKTZ6e/7y+V6pl1H/PgcRqY//4b/2 TisoZvD7Jf0AuXwCAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAA AAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAA AAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAEtzp8MMAAADbAAAADwAA AAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPcCAAAAAA== " adj="0,,0" path="m81,l45,,16,10,7,20,2,32,,46,2,58,7,70r9,7l31,84r17,5l81,89,96,87r12,-5l115,77r-60,l45,75,31,65,26,58,24,48r103,l127,36,26,36r,-7l31,22r7,-5l45,15,64,10r46,l98,5,81,xm127,60r-24,l93,70r-5,2l74,77r41,l122,70r5,-10xm110,10r-46,l76,12r10,3l96,20r4,9l105,36r22,l127,32,120,20,110,10xe" fillcolor="black" stroked="f"> s hiibQuoG2wi3lXxNkqG0WHJcMFjTh6H8b3OyChLHeba+HEy7OGbZar/9He8mX0r1nrr3NxCBunAP 39pLrWA0gOuX+APk7B8AAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAA AAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAAL AAAAAAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQAG0ZPgxQAAANsAAAAP AAAAAAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA+QIAAAAA " adj="0,,0" path="m24,l,,,86r24,l24,46r33,l48,41,62,36r-38,l24,xm57,46r-26,l45,53,77,86r26,l62,48,57,46xm98,l77,,65,5,45,29,33,36r29,l77,17r7,-5l98,12,98,xe" fillcolor="black" stroked="f">
l LEONNtCY4a7DO60LdNRKXmio513D1eX45Qy8oD04P1z0w/7z/WO8X+Jr0GjM9Xx6XIFKPKX/8F/7 2RooCvj9kn8Abn4AAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAA AAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAA AAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAvpDQEMMAAADbAAAADwAA AAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPcCAAAAAA== " adj="0,,0" path="m84,l48,,31,5,17,10,7,20,3,32,,46,3,58,7,70r10,7l31,84r17,5l82,89,96,87r12,-5l115,77r-60,l46,75,31,65,27,58,24,48r106,l130,44r-2,-8l27,36r,-7l31,22r8,-5l46,15,65,10r46,l99,5,84,xm127,60r-24,l94,70r-5,2l75,77r40,l123,70r4,-10xm111,10r-46,l77,12r10,3l96,20r3,4l103,29r,7l128,36r-1,-4l123,20,111,10xe" fillcolor="black" stroked="f"> G KOtc6hrbCLelnCTJTFosOC4YrGhjKPs736yC3edue7TBN8XBtJcs2d9Ogykp1X/v1l8gAnXhFX62 v7WC2RweX+IPkMt/AAAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAA AAAAAAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsA AAAAAAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAAbqx+DEAAAA2wAAAA8A AAAAAAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD4AgAAAAA= " adj="0,,0" path="m74,48r-24,l50,80r24,l74,48xm127,34l,34,,48r127,l127,34xm74,l50,r,34l74,34,74,xe" fillcolor="black" stroked="f"> M 0tdSe7wnuG1lnmWFtNhwWjDY0dpQ9XO4WgXfcnPOj6+658eHKTZ6e/7y+V6pl1H/PgcRqY//4b/2 TisoZvD7Jf0AuXwCAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAA AAAAAAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAA AAAAAAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEAEtzp8MMAAADbAAAADwAA AAAAAAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPcCAAAAAA== " adj="0,,0" path="m81,l45,,16,10,7,20,2,32,,46,2,58,7,70r9,7l31,84r17,5l81,89,96,87r12,-5l115,77r-60,l45,75,31,65,26,58,24,48r103,l127,36,26,36r,-7l31,22r7,-5l45,15,64,10r46,l98,5,81,xm127,60r-24,l93,70r-5,2l74,77r41,l122,70r5,-10xm110,10r-46,l76,12r10,3l96,20r4,9l105,36r22,l127,32,120,20,110,10xe" fillcolor="black" stroked="f"> s hiibQuoG2wi3lXxNkqG0WHJcMFjTh6H8b3OyChLHeba+HEy7OGbZar/9He8mX0r1nrr3NxCBunAP 39pLrWA0gOuX+APk7B8AAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAA AAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAAL AAAAAAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQAG0ZPgxQAAANsAAAAP AAAAAAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA+QIAAAAA " adj="0,,0" path="m24,l,,,86r24,l24,46r33,l48,41,62,36r-38,l24,xm57,46r-26,l45,53,77,86r26,l62,48,57,46xm98,l77,,65,5,45,29,33,36r29,l77,17r7,-5l98,12,98,xe" fillcolor="black" stroked="f"> 
 p a3xHuC3lOEmm0mLBccFgRVtD2fPysgoa08j78UnjUCQ7/eL7eYOnjVL9XruegwjUhv/wX/ugFcwm 8PsSf4BcfgEAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAAAAAA AAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAAAAAA AAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQCxcSXqvwAAANsAAAAPAAAAAAAA AAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA8wIAAAAA " adj="0,,0" path="m77,46r-21,l56,79r21,l77,46xm130,31l,31,,46r130,l130,31xm77,l56,r,31l77,31,77,xe" fillcolor="black" stroked="f">
p a3xHuC3lOEmm0mLBccFgRVtD2fPysgoa08j78UnjUCQ7/eL7eYOnjVL9XruegwjUhv/wX/ugFcwm 8PsSf4BcfgEAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAAAAAA AAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAAAAAA AAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQCxcSXqvwAAANsAAAAPAAAAAAAA AAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA8wIAAAAA " adj="0,,0" path="m77,46r-21,l56,79r21,l77,46xm130,31l,31,,46r130,l130,31xm77,l56,r,31l77,31,77,xe" fillcolor="black" stroked="f"> 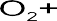 l dYuXFO5q+ZFln9Kh5dRgsKEvQ+X/7uwUrN3br7yeNtbezHGZe/9jqkWn1OuwX0xAROrjU/xwf2sF eRqbvqQfIGd3AAAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAAAAAA AAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsAAAAA AAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAGYY+ATBAAAA2wAAAA8AAAAA AAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD1AgAAAAA= " adj="0,,0" path="m65,l31,4,17,12,7,21,,33,,60r7,9l17,79r14,5l48,88r19,3l82,88r24,-4l115,76r-60,l46,74,36,69,31,64,26,57,24,48r106,l130,45r-2,-9l24,36r2,-8l31,24,46,14r9,-2l110,12,96,4,82,2,65,xm110,60r-7,l89,74r-7,2l115,76r7,-7l127,62r-5,l110,60xm110,12r-33,l86,16r8,3l98,24r3,7l103,36r25,l127,31,120,21,110,12xe" fillcolor="black" stroked="f"> U sgwV2kBDhrsWr7W+Q0eN5IWaOn6suTzvv5yBV7Q75/uzvn36fP8Ybhb4FjQaczkdt0tQicf0H/5r v1gDD/fw+yX/AFz/AAAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAA AAAAAAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsA AAAAAAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAOQJBazEAAAA2wAAAA8A AAAAAAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD4AgAAAAA= " adj="0,,0" path="m84,l48,,31,5,7,19,3,31,,46,3,58r4,9l19,77r12,7l48,89r36,l96,87r12,-5l118,77r-63,l46,75,31,65,27,55r,-7l130,48r,-5l128,36,27,36,31,22r8,-5l46,15r9,-3l113,12,99,5,84,xm106,58r-5,7l96,70r-5,2l77,77r41,l125,70r5,-10l111,60r-5,-2xm113,12r-36,l89,15r7,4l101,24r2,5l106,36r22,l127,31,123,19,113,12xe" fillcolor="black" stroked="f"> M UXaV1B32EW4b+ZSmz9JizXHBYEtvhsrfzckqSB2XxfpyNP3HX1F87XeH2U+2UuphMry+gAg0hHv4 v/2pFWQZ3L7EHyAXVwAAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAA AAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAAL AAAAAAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQDXNULwxQAAANsAAAAP AAAAAAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA+QIAAAAA " adj="0,,0" path="m21,l,,,87r21,l21,48r41,l45,43,55,39r-34,l21,xm62,48r-33,l43,53,77,87r26,l77,60,62,48xm96,l74,3,65,7,45,31,33,39r22,l60,36,79,15,96,12,96,xe" fillcolor="black" stroked="f"> mG Cm2gIYe7Fu+0vkdHjeSGmjp+rLm8nL6dgQPao/P9Ra+ePt8/huUaX4NGY2bTcf8AKvGY/sV/7heb 5+sV/D6TL8DtDwAAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAA AAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAA AAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQCl1HnzwgAAANwAAAAPAAAA AAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA9gIAAAAA " adj="0,,0" path="m65,l31,5,19,12,10,22,2,32,,46,2,58r8,12l19,80r12,4l48,89r36,l96,87r12,-5l118,77r-60,l46,75,31,65,26,58,24,48r106,l130,46,128,36,26,36r3,-7l31,24,46,15r9,-3l110,12,98,5,84,3,65,xm110,60r-7,l101,65r-5,5l89,72r-5,5l118,77r7,-7l130,63r-8,l110,60xm110,12r-33,l89,15r7,5l101,24r2,5l103,36r25,l127,32,122,20,110,12xe" fillcolor="black" stroked="f">
l dYuXFO5q+ZFln9Kh5dRgsKEvQ+X/7uwUrN3br7yeNtbezHGZe/9jqkWn1OuwX0xAROrjU/xwf2sF eRqbvqQfIGd3AAAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAAAAAA AAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsAAAAA AAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAGYY+ATBAAAA2wAAAA8AAAAA AAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD1AgAAAAA= " adj="0,,0" path="m65,l31,4,17,12,7,21,,33,,60r7,9l17,79r14,5l48,88r19,3l82,88r24,-4l115,76r-60,l46,74,36,69,31,64,26,57,24,48r106,l130,45r-2,-9l24,36r2,-8l31,24,46,14r9,-2l110,12,96,4,82,2,65,xm110,60r-7,l89,74r-7,2l115,76r7,-7l127,62r-5,l110,60xm110,12r-33,l86,16r8,3l98,24r3,7l103,36r25,l127,31,120,21,110,12xe" fillcolor="black" stroked="f"> U sgwV2kBDhrsWr7W+Q0eN5IWaOn6suTzvv5yBV7Q75/uzvn36fP8Ybhb4FjQaczkdt0tQicf0H/5r v1gDD/fw+yX/AFz/AAAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAA AAAAAAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsA AAAAAAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAOQJBazEAAAA2wAAAA8A AAAAAAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD4AgAAAAA= " adj="0,,0" path="m84,l48,,31,5,7,19,3,31,,46,3,58r4,9l19,77r12,7l48,89r36,l96,87r12,-5l118,77r-63,l46,75,31,65,27,55r,-7l130,48r,-5l128,36,27,36,31,22r8,-5l46,15r9,-3l113,12,99,5,84,xm106,58r-5,7l96,70r-5,2l77,77r41,l125,70r5,-10l111,60r-5,-2xm113,12r-36,l89,15r7,4l101,24r2,5l106,36r22,l127,31,123,19,113,12xe" fillcolor="black" stroked="f"> M UXaV1B32EW4b+ZSmz9JizXHBYEtvhsrfzckqSB2XxfpyNP3HX1F87XeH2U+2UuphMry+gAg0hHv4 v/2pFWQZ3L7EHyAXVwAAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAA AAAAAAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAAL AAAAAAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQDXNULwxQAAANsAAAAP AAAAAAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA+QIAAAAA " adj="0,,0" path="m21,l,,,87r21,l21,48r41,l45,43,55,39r-34,l21,xm62,48r-33,l43,53,77,87r26,l77,60,62,48xm96,l74,3,65,7,45,31,33,39r22,l60,36,79,15,96,12,96,xe" fillcolor="black" stroked="f"> mG Cm2gIYe7Fu+0vkdHjeSGmjp+rLm8nL6dgQPao/P9Ra+ePt8/huUaX4NGY2bTcf8AKvGY/sV/7heb 5+sV/D6TL8DtDwAAAP//AwBQSwECLQAUAAYACAAAACEA2+H2y+4AAACFAQAAEwAAAAAAAAAAAAAA AAAAAAAAW0NvbnRlbnRfVHlwZXNdLnhtbFBLAQItABQABgAIAAAAIQBa9CxbvwAAABUBAAALAAAA AAAAAAAAAAAAAB8BAABfcmVscy8ucmVsc1BLAQItABQABgAIAAAAIQCl1HnzwgAAANwAAAAPAAAA AAAAAAAAAAAAAAcCAABkcnMvZG93bnJldi54bWxQSwUGAAAAAAMAAwC3AAAA9gIAAAAA " adj="0,,0" path="m65,l31,5,19,12,10,22,2,32,,46,2,58r8,12l19,80r12,4l48,89r36,l96,87r12,-5l118,77r-60,l46,75,31,65,26,58,24,48r106,l130,46,128,36,26,36r3,-7l31,24,46,15r9,-3l110,12,98,5,84,3,65,xm110,60r-7,l101,65r-5,5l89,72r-5,5l118,77r7,-7l130,63r-8,l110,60xm110,12r-33,l89,15r7,5l101,24r2,5l103,36r25,l127,32,122,20,110,12xe" fillcolor="black" stroked="f"> 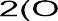
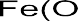
 r pXZ4ieFmkHmaLqTBnmNDhyO9dlSfyl+jgN3P23N1XEzfzfIQxqphWx5ZqafHafcCItAU7uKb+0PH +XkG/8/EC+TmCgAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAAAAAA AAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsAAAAA AAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAMAF9tPBAAAA3AAAAA8AAAAA AAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD1AgAAAAA= " adj="0,,0" path="m43,26r-5,l38,50r5,l43,26xm84,24l,24r,2l84,26r,-2xm43,l38,r,24l43,24,43,xe" fillcolor="black" stroked="f"> S O7zFcNPKSZrOpMGGY0ONHe1qKn7yX6OA3eX97XSe9d/l/Bi6U8k2P7NSL6N+uwQRqA9P8b/7Q8f5 kyk8nokXyPUdAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAAAAAA AAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAAAAAA AAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEA0HJVS8AAAADcAAAADwAAAAAA AAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPQCAAAAAA== " adj="0,,0" path="m45,26r-7,l38,50r7,l45,26xm84,24l,24r,2l84,26r,-2xm45,l38,r,24l45,24,45,xe" fillcolor="black" stroked="f">
r pXZ4ieFmkHmaLqTBnmNDhyO9dlSfyl+jgN3P23N1XEzfzfIQxqphWx5ZqafHafcCItAU7uKb+0PH +XkG/8/EC+TmCgAA//8DAFBLAQItABQABgAIAAAAIQDb4fbL7gAAAIUBAAATAAAAAAAAAAAAAAAA AAAAAABbQ29udGVudF9UeXBlc10ueG1sUEsBAi0AFAAGAAgAAAAhAFr0LFu/AAAAFQEAAAsAAAAA AAAAAAAAAAAAHwEAAF9yZWxzLy5yZWxzUEsBAi0AFAAGAAgAAAAhAMAF9tPBAAAA3AAAAA8AAAAA AAAAAAAAAAAABwIAAGRycy9kb3ducmV2LnhtbFBLBQYAAAAAAwADALcAAAD1AgAAAAA= " adj="0,,0" path="m43,26r-5,l38,50r5,l43,26xm84,24l,24r,2l84,26r,-2xm43,l38,r,24l43,24,43,xe" fillcolor="black" stroked="f"> S O7zFcNPKSZrOpMGGY0ONHe1qKn7yX6OA3eX97XSe9d/l/Bi6U8k2P7NSL6N+uwQRqA9P8b/7Q8f5 kyk8nokXyPUdAAD//wMAUEsBAi0AFAAGAAgAAAAhANvh9svuAAAAhQEAABMAAAAAAAAAAAAAAAAA AAAAAFtDb250ZW50X1R5cGVzXS54bWxQSwECLQAUAAYACAAAACEAWvQsW78AAAAVAQAACwAAAAAA AAAAAAAAAAAfAQAAX3JlbHMvLnJlbHNQSwECLQAUAAYACAAAACEA0HJVS8AAAADcAAAADwAAAAAA AAAAAAAAAAAHAgAAZHJzL2Rvd25yZXYueG1sUEsFBgAAAAADAAMAtwAAAPQCAAAAAA== " adj="0,,0" path="m45,26r-7,l38,50r7,l45,26xm84,24l,24r,2l84,26r,-2xm45,l38,r,24l45,24,45,xe" fillcolor="black" stroked="f"> 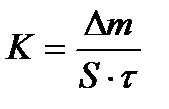 , г/м2 ч, (1)
, г/м2 ч, (1)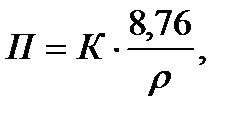 (2)
(2)


