Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Химическая природа и общие свойства ферментов.
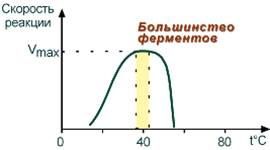
Давно выяснено, что все ферменты являются белками и обладают всеми свойствами белков. Поэтому, подобно белкам, ферменты делятся на простые и сложные. Простые ферменты состоят только из аминокислот – например, пепсин, трипсин, лизоцим. Сложные ферменты (холоферменты) имеют в своем составе белковую часть, состоящую из аминокислот – апофермент, и небелковую часть – кофактор. Примером сложных ферментов являются сукцинатдегидрогеназа (содержит ФАД), аминотрансферазы (содержат пиридоксальфосфат), различные пероксидазы (содержат гем), лактатдегидрогеназа (содержит Zn2+), амилаза (содержит Ca2+). Кофактор, в свою очередь, может называться коферментом (НАД+, НАДФ+, ФМН, ФАД, биотин) или простетической группой (гем, олигосахариды, ионы металлов Fe2+, Mg2+, Ca2+, Zn2+). Деление на коферменты и простетические группы не всегда однозначно: • если связь кофактора с белком прочная, то в этом случае говорят о наличии простетической группы, • но если в качестве кофактора выступает производное витамина – то его называют коферментом, независимо от прочности связи. Свойства ферментов 1. Зависимость скорости реакции от температуры Зависимость активности ферментов (скорости реакции) от температуры описывается колоколообразной кривой с максимумом скорости при значениях оптимальной температуры для данного фермента. Повышение скорости реакции при приближении к оптимальной температуре объясняется увеличением кинетической энергии реагирующих молекул.
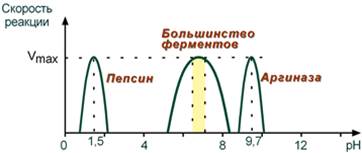
Закон о повышении скорости реакции в 2-4 раза при повышении температуры на 10°С справедлив и для ферментативных реакций, но только в пределах до 55-60°С, т.е. до температур денатурации белков. При понижении температуры активность ферментов понижается, но не исчезает совсем. 2. Зависимость скорости реакции от рН Зависимость также описывается колоколообразной кривой с максимумом скорости при оптимальном для данного фермента значении рН. Данная особенность ферментов имеет существенное значение для организма в его адаптации к изменяющимся внешним и внутренним условиям. Сдвиги величины рН вне- и внутри клетки играет роль в патогенезе заболеваний, изменяя активность ферментов разных метаболических путей. Для каждого фермента существует определенный узкий интервал рН среды, который является оптимальным для проявления его высшей активности. Например, оптимальные значения рН для пепсина 1,5-2,5, трипсина 8,0-8,5, амилазы слюны 7,2, аргиназы 9,7, кислой фосфатазы 4,5-5,0, сукцинатдегидрогеназы 9,0.
3. Зависимость от количества фермента При увеличении количества молекул фермента скорость реакции возрастает непрерывно и прямо пропорционально количеству фермента, т.к. большее количество молекул фермента производит большее число молекул продукта.
4. Зависимость скорости реакции от концентрации субстрата При увеличении концентрации субстрата скорость реакции сначала возрастает, т.к. к катализу добавляемых молекул субстрата подключаются новые и новые молекулы фермента. Т.е. скорость накопления продукта возрастает, и это означает увеличение активности фермента. Затем наблюдается эффект насыщения (плато на кривой), когда все молекулы фермента заняты молекулами субстрата и непрерывно ведут катализ, здесь скорость реакции максимальна. В некоторых случаях, при дальнейшем увеличении концентрации субстрата между его молекулами возникает конкуренция за активный центр фермента и активность фермента (скорость реакции) снижается.
(несмотря на качество, можно рассмотреть подъем, плато и начало снижения) ---
|
|||||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 124; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.14.130.24 (0.005 с.) |