Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Применение первого закона термодинамики к изопроцессам
Напомним, что в изопроцессе остаётся неизменным значение некоторой величины, характеризующей состояние газа — температуры, объёма или давления. Для каждого вида изопроцессов запись первого закона термодинамики упрощается. Изотермический процесс, T = const. Внутренняя энергия идеального газа зависит только от его температуры. Если температура газа не меняется, то не меняется и внутренняя энергия: ∆ U = 0. Тогда формула (2) даёт: Q = A. Всё подведённое к газу тепло идёт на совершение газом работы. Изохорный процесс, V = const. Если объём газа остаётся постоянным, то поршень не перемещается, и потому работа газа равна нулю: A = 0. Тогда первый закон термодинамики даёт: Q = ∆ U. Всё тепло, переданное газу, идёт на изменение его внутренней энергии. Изобарный процесс, p = const. Подведённое к газу тепло идёт как на изменение внутренней энергии, так и на совершение работы. Имеем: Q = ∆ U + p ∆ V. Адиабатный процесс Процесс называется адиабатным, если он идёт без теплообмена с окружающими телами. Адиабатный процесс совершается газом, находящимся в теплоизолированном сосуде. Такой сосуд препятствует всем видам теплопередачи: теплопроводности, конвекции, излучению. Пример теплоизолированного сосуда — термос. Приблизительно адиабатным будет всякий процесс, протекающий достаточно быстро: в течение процесса теплообмен просто не успевает произойти. При адиабатном процессе Q = 0. Из первого закона термодинамики получаем: A + ∆ U = 0, или A = −∆ U. В процессе адиабатного расширения газ совершает положительную работу, поэтому ∆ U < 0 (работа совершается за счёт убыли внутренней энергии). Следовательно, газ охлаждается. Если заставить газ совершить достаточно большую работу, охладить его можно весьма сильно. Именно на этом основаны методы сжижения газов. Наоборот, в процессе адиабатного сжатия будет A < 0, поэтому ∆ U > 0: газ нагревается. Адиабатное нагревание воздуха используется в дизельных двигателях для воспламенения топлива. Кривая, изображающая ход адиабатного процесса, называется адиабатой. Интересно сравнить ход адиабаты и изотермы на pV -диаграмме.
V Сравнительный ход изотермы и адиабаты
В обоих процессах давление убывает с увеличением объёма, но в адиабатном процессе убывание идёт быстрее. Почему? При изотермическом расширении давление падает потому, что уменьшается концентрация частиц газа, в результате чего удары частиц по стенкам сосуда становятся реже. Однако интенсивность этих ударов остаётся прежней: ведь температура газа не меняется — значит, не меняется и средняя кинетическая энергия его частиц. А при адиабатном расширении, наряду с уменьшением концентрации частиц, падает также и температура газа. Удары частиц становятся не только более редкими, но и более слабыми. Вот почему адиабата убывает быстрее изотермы.
Решение задач Задача №1 При изохорном процессе углероду массой 600 грамм было передано 80 КДж тепла. На сколько при этом изменится его температура?
Q=80 КДж 80*103Дж Q=∆U
∆Т-? Ответ:128 К
Задача №2 При адиабатном процессе объем газа изменился на 6 литров, его внутренняя энергия изменилась на 36 кДж. Какое давление при этом оказывает газ на стенки сосуда?
∆V=6л 6*10-3м3 ∆U=А1=p∆V =>p=
p-? Ответ:6 МПа
Задача №3 Какую работу совершает кислород массой 320 грамм при изобарном нагревании на 10 К?
m=320г 0,32кг А1=p∆V=
А1-? Ответ:830 К
|
|||||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 198; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.14.130.24 (0.004 с.) |


 M=600 гр 0,6 кг Q=
M=600 гр 0,6 кг Q= 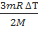 =>∆Т=
=>∆Т= 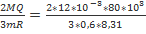 =128 K
=128 K
 Дано: СИ: Решение:
Дано: СИ: Решение:
 ∆U=36 кДж 36*103Дж p=
∆U=36 кДж 36*103Дж p= 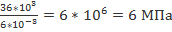

 Дано: CИ: Решение:
Дано: CИ: Решение: