
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Работа газа в изобарном процессе
Работа газа равна: A = F ∆ x = pS ∆ x. Но S ∆ x = ∆ V — изменение объёма газа. Поэтому для работы газа при изобарном расширении мы получаем формулу: A = p ∆ V. (9) Рис. 26. A = p ∆ V Если V 1 и V 2 — начальный и конечный объём газа, то для работы газа имеем: A = p (V 2 − V 1). Изобразив данный процесс на pV -диаграмме, мы видим, что работа газа равна площади прямоугольника под графиком нашего процесса (рис. 27). p
p V 1 V 2 V Рис. 27. Работа газа как площадь Пусть теперь газ изобарно сжимается от объёма V 1 до объёма V 2. С помощью аналогичных рассуждений приходим к формуле: A = − p (V 1 − V 2). Но −(V 1 − V 2) = V 2 − V 1 = ∆ V, и снова получается формула (9). Работа газа опять-таки будет равна площади под графиком процесса на pV -диаграмме, но теперь со знаком минус. Итак, формула A = p ∆ V выражает работу газа при постоянном давлении — как в процессе расширения газа, так и в процессе сжатия. Работа, совершаемая над газом Наряду с работой A, которую совершает газ по передвижению поршня, рассматривают также работу A 0, которую поршень совершает над газом. Если газ действует на поршень с силой F~, то по третьему закону Ньютона поршень действует на газ с силой F~ 0, равной силе F~ по модулю и противоположной по направлению: F~ 0 = − F~ (рис. 29).
Рис. 29. Внешняя сила F~ 0, действующая на газ Следовательно, работа поршня A 0 равна по модулю и противоположна по знаку работе газа: A 0 = − A. Так, в процессе расширения газ совершает положительную работу (A > 0); при этом работа, совершаемая над газом, отрицательна (A 0 < 0). Наоборот, при сжатии работа газа отрицательна (A < 0), а работа, совершаемая поршнем над газом, положительна (A 0 > 0). Будьте внимательны: если в задаче просят найти работу, совершённую над газом, то имеется в виду работа A 0. Решение задач Задача №1 Какое количество вещества содержится в газе, если при его давлении 200 кПа и температуре 240 К его оббьем равен 40 л?
P=200кПа 200*103Па pV= υRT => υ= T=240 K Ответ:4 моль
υ -? Задача №2 Баллон какой вместимости нужен для содержания в нем газа, взятого в количестве 50 моль, если при максимальной температуре 360 К давлении 6 МПа?
υ =50 моль pV=υRT Т=360 K V=
V-?
Задача №3 Каково давление сжатого воздуха, находящегося в баллоне вместимостью 20л при 300К, если масса этого воздуха 2 кг?
V=20л 20*10-3м3 pV= m=2кг p=
p-? Ответ:8,6 Мпа
Тема 2.4. Основы термодинамики Содержание учебного материала: «Первый закон термодинамики. Применение первого закона термодинамики к изопроцессам». Цели: Учебные: Раскрыть сущность первого закона термодинамики. Вывести формулы применения первого закона термодинамики к изопроцессам. Научить решать задачи по применению первого закона ТД к изопроцессам. Обучить навыкам постановки демонстрационного эксперимента. Воспитательные: Воспитывать трудолюбие, внимательность и наблюдательность. Научить слушать, анализировать, чётко аргументировать, излагать и отстаивать своё мнение. Повысить интерес обучающихся к изучаемому материалу путем разнообразия форм проведения уроков. Развивающие: Развивать познавательные способности обучающихся. Активизировать исследовательские способности. Расширять кругозор, исследовательское мышление обучающихся. Прививать умения применять полученные теоретические знания на практике. Оборудование: секундомер, термометр, манометр, гофрированный сосуд для газа, измерительная лента.
Как мы знаем, существует лишь два способа изменения внутренней энергии тела: теплопередача и совершение работы.
Опыт показывает, что эти способы независимы — в том смысле, что их результаты складываются. Если телу в процессе теплообмена передано количество теплоты Q, и если в то же время над телом совершена работа A 0, то изменение внутренней энергии тела будет равно: ∆ U = Q + A 0 . (1) Нас больше всего интересует случай, когда тело является газом. Тогда A 0 = − A (где A, как всегда, есть работа самого газа). Формула (1) принимает вид: ∆ U = Q − A, или Q = ∆ U + A. (2) Соотношение (2) называется первым законом термодинамики. Смысл его прост: количество теплоты, переданное газу, идёт на изменение внутренней энергии газа и на совершение газом работы. Напомним, что величина Q может быть и отрицательной: в таком случае тепло отводится от газа. Но первый закон термодинамики остаётся справедливым в любом случае. Он является одним из фундаментальных физических законов и находит подтверждение в многочисленных явлениях и экспериментах.
|
||||||||||||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 98; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.67.26 (0.008 с.) |
|||||||||||||
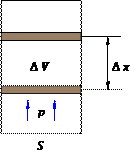 Предположим, что газ расширяется при постоянном давлении p. Тогда сила F, с которой газ действует на поршень, также постоянна. Пусть поршень переместился на расстояние ∆ x (рис. 26).
Предположим, что газ расширяется при постоянном давлении p. Тогда сила F, с которой газ действует на поршень, также постоянна. Пусть поршень переместился на расстояние ∆ x (рис. 26).


 V=40л 40*10-3м3
V=40л 40*10-3м3 
 Дано: СИ Решение
Дано: СИ Решение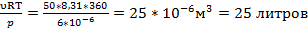
 p=6 МПа 6*106 Ответ:
p=6 МПа 6*106 Ответ: 

 Дано: СИ Решение:
Дано: СИ Решение: =>p=
=>p= 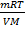
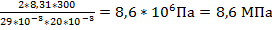
 Т=300К
Т=300К 


