Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Пантотеновая кислота, антидерматитный витамин
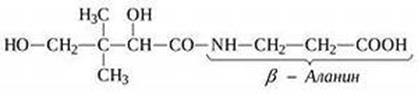
Пантотеновая кислота в качестве витамина была открыта в 1933 г. Р. Уильямсом и соавторами в составе группы веществ природного происхождения, стимулирующих рост дрожжей. Данный витамин присутствует фактически во всех пищевых продуктах, поэтому получил название «пантотеновая кислота» (от греч. pantoten – повсюду). В 1940 г. была расшифрована и подтверждена химическим синтезом структура этого витамина. Пантотеновая кислота состоит из остатков D-2,4-дигидрокси-3,3-диметилмасляной кислоты и β-аланина, соединённых между собой амидной связью (рис.9)
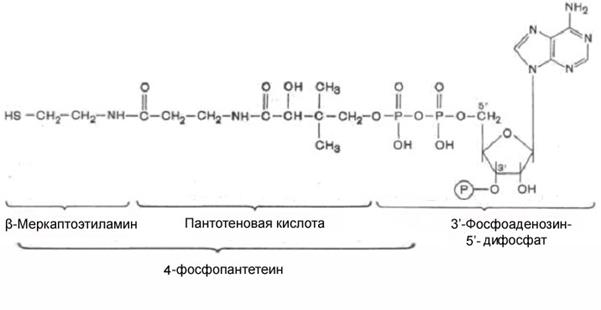
Рис 9. Формула пантотеновой кислоты Пантотеновая кислота представляет собой белые кристаллы, хорошо растворимые в воде; она малоустойчива и легко подвергается гидролизу по амидной связи под действием слабых кислот и щелочей. Суточная потребность и распространение в природе. Пантотеновая кислота содержится во многих продуктах животного и растительного происхождения (яйцах, печени, мясе, рыбе, молоке, дрожжах, картофеле, моркови, пшенице, яблоках, зелени). В небольших количествах пантотеновая кислота синтезируется микрофлорой кишечника. Суточная потребность в пантотеновой кислоте для взрослого человека составляет 3–12 мг. Биологическая роль пантотеновой кислоты. Пантотеновая кислота используется в клетках для синтеза двух коферментов: кофермента А (коэнзима А, КоА) и 4-фосфопантетеина. Формула кофермента А представлена на рисунке 10. Она включает три фрагмента: остаток 3'-фосфоаденозин-5'-дифосфата, остаток пантотеновой кислоты и остаток β-меркаптоэтиламина (тиоэтиламина). 4-фосфопантетеин является составной частью кофермента А (рис. 10)
Рис. 10. Строение кофермента А и 4-фосфопантетеина. Синтез КоА в организме включает множество стадий и требует энергии АТФ. Коэнзим А является коферментом ацилтрансфераз – ферментов, катализирующих реакции переноса ацильных групп. В трансферазных реакциях непосредственно участвует SH-группа молекулы, поэтому в биохимических реакциях принято обозначать коэнзим А в виде HS-KoA. Присоединение ацильного остатка к коферменту А (образование ацил-КоА) приводит к активации карбоновой кислоты, что создает термодинамические предпосылки для ее участия в реакциях, протекающих с потреблением энергии. Кофермент А участвует в переносе ацильных радикалов в реакциях общего пути катаболизма, обмена липидов и кетоновых тел, синтеза ацетилглюкозаминов, стероидных гормонов, гема, ацетилхолина, обезвреживания чужеродных веществ в печени.
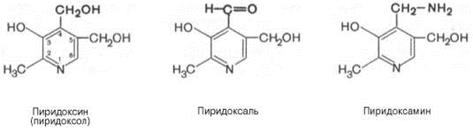
4-фосфопантотеин,являющийся составной частью коэнзима А, входит в состав ацилпереносящего белка (АПБ) сложного мультиферментного комплекса пальмитоилсинтазы, обеспечивающего синтез жирных кислот у млекопитающих. Гипо- и авитаминоз. Признаки авитаминоза пантотеновой кислоты изучены на лабораторных животных с использованием специальных диет. Недостаток витамина сопровождался развитием дерматитов, поражением слизистых оболочек, дистрофическими изменениями желез внутренней секреции (в частности, надпочечников) и нервной системы (невриты, параличи), изменением сердечной мышцы и почек, депигментацией шерсти, прекращением роста, потерей аппетита, истощением, выпадением волос (алопецией). Применение пантотеновой кислоты в медицинской практике. Производные пантотеновой кислоты применяются в виде двух лекарственных препаратов – кальция пантотената (кальциевая соль D-пантотеновой кислоты) и пантенола (соответствующего спирта). Пантенол является синтетически аналогом пантотеновой кислоты. В организме животных и человека он легко превращается в пантотеновую кислоту, поэтому может считаться ее провитамином. Пантенол хорошо всасывается при нанесении на кожу, поэтому этот препарат широко применяется в дерматологии и косметике. Применение препаратов пантотеновой кислоты преимущественно связано с их ранозаживляющим действием. Они используются при лечении воспалительных заболеваний полости рта, роговицы, дыхательных путей, слизистой оболочки желудка, урогенитального тракта. Витамин В6, пиридоксин, пиридоксаль, пиридоксамин, антидерматитный витамин. Витамин В6 как самостоятельный независимый пищевой фактор был обнаружен П. Дьерди в 1934 г. В 1938 г. витамин В6 был выделен из дрожжей и печени, а затем синтезирован химически. Он оказался производным 3-оксипиридина. Вскоре выяснилось, что процесс переаминирования аминокислот, открытый в 1937 году нашим соотечественником, выдающимся ученым-биохимиком Александром Браунштейном, возможен лишь при участии пиридоксина. В 1944 году американец Е.Снелл выделил еще две разновидности этого витамина: пиридоксаль и пиридоксамин. Термином «витамин В6», по рекомендациям Международной комиссии по номенклатуре биологической химии, обозначают все три производных 3-оксипиридина, обладающих одинаковой витаминной активностью: пиридоксин (пиридоксол), пиридоксаль и пиридоксамин. Формы витамина В6 отличаются друг от друга природой замещающей группы в положении 4 пиридинового кольца (рис.11).
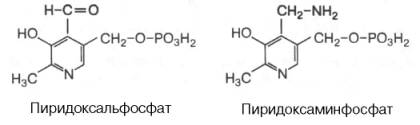
Рис.11. Формулы витамина В6 Все три формы витамина В6 - бесцветные кристаллы, хорошо растворимые в воде и этаноле. Водные растворы весьма устойчивы по отношению к кислотам и щелочам, однако они чувствительны к влиянию света. Суточная потребность и распространение. Источники витамина В6 для человека являются яйца, печень, молоко, зеленый перец, морковь, пшеница, дрожжи. Некоторое количество витамина синтезируется кишечной флорой. Суточная потребность составляет 2-3 мг. Биологическая роль витамина В6. Все формы витамина В6 используются в организме для синтеза коферментов: пиридоксальфосфата (ПФ) и пиридоксаминфосфата (ПАФ) (рис.12).
Рис.12. Строение коферментов – производных витамина В6 Коферменты образуются путём фосфорилирования по гидроксиметильной группе в пятом положении пиридинового кольца при участии фермента пиридоксалькиназы и АТФ как источника фосфата. Пиридоксалькиназа наиболее активна в тканях мозга. У активных курильщиков токсические продукты, образующиеся при пиролизе табака, ингибируют пиридоксалькиназу, что приводит к нарушению синтеза пиродоксальфосфата. Пиридоксальзависимые ферменты играют ключевую роль в обмене аминокислот. Пиридоксальфосфат является простетической группой аминотрансфераз, катализирующих обратимый перенос аминогруппы (NH2-группы) от аминокислот на α-кетокислоту с образованием заменимых аминокислот и α-кетокарбоновых кислот, идущих на восполнение метаболитов ЦТК (рис.13).
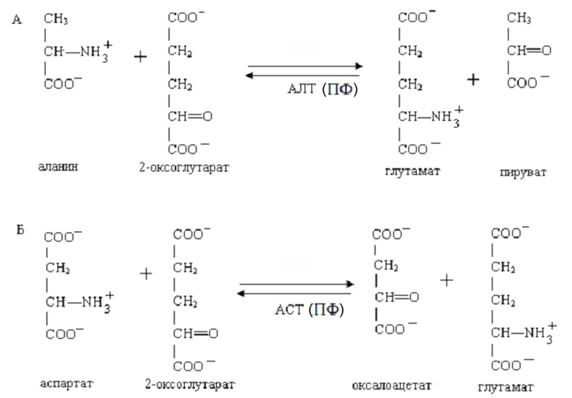
Рис.13. Реакции трансаминироваия аланина (А) и аспартата (Б) (АЛТ - аланинаминотрансферазы и АСТ – аспартатаминотрансферазы). Пиридоксальзависимые ферменты участвуют в специфических реакциях метаболизма отдельных аминокислот (серина, треонина, серосодержащих аминокислот, триптофана), а также в синтезе гема. С участием пиридоксальфосфата идут реакции прямого неокислительного дезаминирования серина и треонина (рис.14).
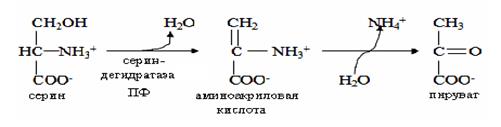
Рис.14. Реакция неокислительного дезаминирования серина. Участие пиридоксальфосфата необходимо для осуществления реакций регенерации метионина, при его недостаточности происходит накопление гомоцитеина, который оказывает повреждающее действие на эндотелий кровеносных сосудов. Пиридоксальфосфат участвует в реакциях метаболизма триптофана по кинурениновому пути, одним из важнейших продуктов этого пути является кофермент НАД+. Пиридоксальфосфат также необходим для работы декарбоксилаз аминокислот, осуществляющих необратимое отщепление карбоксильной группы в виде СО2 с образованием биогенных аминов (гистамина, g-аминомасляной кислоты (ГАМК), дофамина и др.) (рис.15).
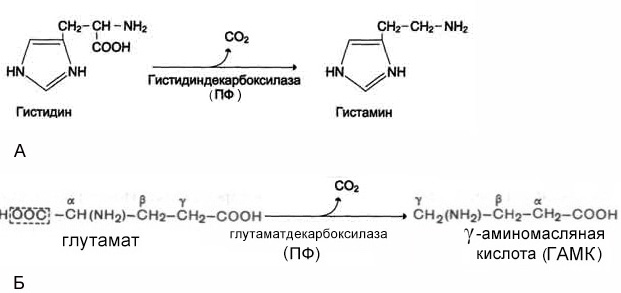
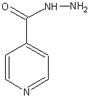
Рис 15. Образование гистамина (А) и g -аминомасляной кислоты (Б). Пиридоксальфосфат является коферментом ключевого фермента синтеза гема 5-аминолевулинатсинтазы. Гипо- и авитаминоз. Недостаточность витамина В6 наиболее подробно изучена в экспериментах на крысах. Наиболее характерным признаком гиповитаминоза является специфический дерматит с преимущественным поражением кожи лапок, хвоста, носа и ушей. Данная форма дерматита носит название акродиния. Помимо шелушения кожи и выпадения шерсти, наблюдается изъязвление кожи конечностей, гангрена пальцев. При более тяжелых формах авитаминоза В6 у собак, свиней, крыс и кур наблюдаются эпилептиформные припадки с дегенеративными изменениями в ЦНС. У человека недостаточность витамина В6 встречается редко. Описаны пеллагроподобные дерматиты, не поддающиеся лечению никотиновой кислотой, но быстро исчезающие при введении пиридоксина. У грудных детей описан гиповитаминоз В6, связанный с недостатком этого витамина в смесях для искусственного вскармливания. В этих случаях наряду с дерматитами наблюдались повышенная возбудимость, судороги, периодические эпилептиформные припадки. Эти нарушения со стороны ЦНС вероятнее всего связаны с недостаточным синтезом тормозного медиатора ГАМК, образуемого из глутаминовой кислоты при декарбоксилировании. У взрослых дефицит В6 чаще всего проявляется в виде полиневрита и дерматита, может также развиваться микроцитарная анемия. В настоящее время все более распространенным становится дефицит витамина В6, обусловленный применением лекарственных средств, которые действуют как его антагонисты. Так, например, препараты изониазид (рис. 16) и циклосерин, применяемые для лечения туберкулеза, блокируют коферментную функцию пиридоксальфосфата. Также признаки гиповитаминоза В6 наблюдают при длительном лечении аутоиммунных заболеваний пеницилламином.
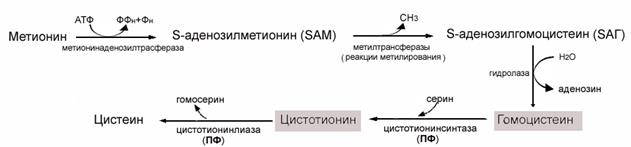
Рис.16. Строение изониазида, антагониста пиридоксина При недостаточности В6 нарушается обмен серосодержащих аминокислот метионина и цистеина, замедляется утилизация гомоцистеина и цистатионина под действием пиридоксальзависимых ферментов (рис.17). Вследствие этого при биохимическом анализе мочи наблюдается гомоцистеинурия и цистатионинурия.
Рис.17. Процесс образования цистеина. Отмечены вещества, накапливающиеся при недостаточности В6.
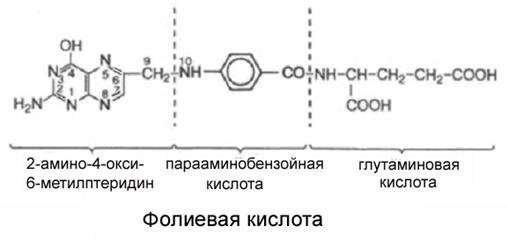
Недостаточность пиридоксина приводит к нарушению обмена триптофана, что сопровождается повышением экскреции с мочой ксантуреновой кислоты и снижением выведения кинуреновой кислоты. Кинуреновая кислота является одним из продуктом катаболизма триптофана и ее образование требует присутствия ПФ. Нехватка пиридоксальфосфата приводит к нарушению синтеза эндогенного НАД+, который образуется в реакциях метаболизма триптофана. Клинически это проявляется симптомами, характерными для пеллагры. Применение В6 в медицинской практике. В качестве лекарственных препаратов применяются пиридоксина гидрохлорид и пиридоксальфосфат. Показанием к назначению является нарушение обмена веществ, в первую очередь белкового и липидного обмена. Пиридоксальфосфат эффективен при различных кожных заболеваниях (крапивница, экзема, нейродермиты, псориаз и др.). Для профилактики гиповитаминоза препараты В6 назначают при беременности. Высокие дозы пиридоксина необходимы при приеме лекарственных препаратов-антогонистов В6. Витамин В9, фолиевая кислота, Вс, фолацин, Антианемический витамин В 30-х годах ХХ века советский врач-биолог В.Ефремов и английский врач Уилс диагностировали у беременных женщин макроцитарную анемию, особую форму нарушения кроветворения, при которой образуются крупные эритроциты (макроциты) и увеличена скорость их распада по сравнению со скоростью образования. Оба врача обнаружили, что заболевание проходит при приеме экстрактов печени. Лечебный компонент из печени был вскоре выделен и назван «фактором Уилса». Позднее его переименовали в витамин "М", а в 1941 году установили, что его содержат также листья шпината и петрушки, и появилось очередное название - фолиевая кислота (от лат. folium - лист). Еще до определения химического строения фолиевой кислоты было установлено, что для роста некоторых бактерий необходимо присутствие в питательной среде парааминобензойной кислоты. Добавление структурных аналогов парааминобензойной кислоты, в частности сульфаниламидных препаратов, затормаживало бактериальный рост. В дальнейшем было показано, что парааминобензойная кислота необходима бактериям для синтеза фолиевой кислоты. Фолиевая кислота состоит из трёх структурных единиц: остатка 2-амино-4-окси-6-метилптеридина, парааминобензойной и глутаминовой кислот (рис.18). Витамин, полученный из разных источников, может содержать до 6 остатков глутаминовой кислоты. Фолиевая кислота ограниченно растворима в воде, но хорошо растворима в разбавленных спиртовых растворах.
Рис. 18. Строение фолиевой кислоты. Суточная потребность и распространение. В значительных количествах фолиевая кислота присутствует не только в печени и зеленых частях растений, но и в дрожжах, почках, мясе и других продуктах животного происхождения. Суточная потребность в фолиевой кислоте колеблется от 50 до 200 мкг; однако вследствие плохой всасываемости этого витамина рекомендуемая суточная доза - 400 мкг.
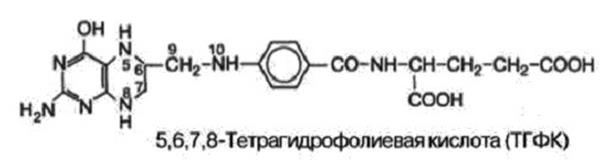
Биологическая роль фолиевой кислоты. Коферментные функции фолиевой кислоты связаны с образованием восстановленного птеридинового производного. Восстановление сводится к разрыву двух двойных связей и присоединению четырех водородных атомов в положениях 5, 6, 7 и 8 с образованием тетрагидрофолиевой кислоты (ТГФК) (рис.19). Синтез ТГФК протекает в 2 стадии при участии специфических ферментов, содержащих восстановленный НАДФ. Сначала при действии фолатредуктазы образуется дигидрофолиевая кислота (ДГФК), которая при участии второго фермента – дигидрофолатредуктазы – восстанавливается в ТГФК.
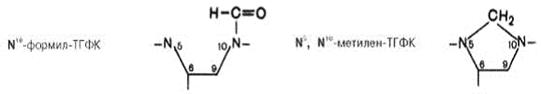
Рис. 19. Строение ТГФК Коферментные функции ТГФК непосредственно связаны с переносом различных одноуглеродных групп, за исключением СО2. Первичными источниками этих групп являются β-углеродный атом серина, α-углеродный атом глицина, углерод метильных групп метионина, холина, 2-й углеродный атом индольного кольца триптофана, 2-й углеродный атом имидазольного кольца гистидина, а также формальдегид, муравьиная кислота и метанол. Известно шесть одноуглеродных групп, вступающих в реакции в составе ТГФК: формильная (—СНО), метильная (—СН3), метиленовая (—СН2—), метенильная (—СН=), оксиметильная (—СН2ОН) и формиминовая (—CH=NH). Перечисленные одноуглеродные группы могут присоединяться к 5-му или 10-му атомом азота, а также к обоим атомам. На рис. 20 в качестве примера показано присоединение формильной и метиленовой групп.
Рис. 20. Производные ТГФК. В организме человека производные ТГФК участвуют в различных процессах: синтезе пуриновых и тимидиловых нуклеотидов, в обмене метионина, цистеина, глицина и серина. Так как названные вещества играют ключевую роль в синтезе белков и нуклеиновых кислот, то недостаточность фолиевой кислоты приводит к глубоким обменным нарушениям. Гипо- и авитаминоз. Фолиевая кислота синтезируется микрофлорой кишечника в необходимых количествах, поэтому для изучения ее авитаминоза у лабораторных животных предварительно подавляли рост микрофлоры антибиотиками. У обезьян недостаточность фолиевой кислоты сопровождается развитием специфической анемии; а у крыс сначала развивается лейкопения, а далее анемия. У человека наблюдается клиническая картина макроцитарной анемии, лейкопении; у молодых организмов может быть задержка роста. Патология кроветворения при недостаточности фолиевой кислоты объясняется нарушением синтеза нуклеотидов, что влечет за собой нарушение процессов репликации и транскрипции в клетках костного мозга, в которых осуществляется гемопоэз. В результате этого в периферической крови появляются клетки крови, имеющие патологическую морфологию. При гиповитаминозе фолиевой кислоты нарушается регенерации эпителия, что особенно выражено в ЖКТ. Патология обусловлена недостатком пуринов и пиримидинов для синтеза ДНК в постоянно делящихся клетках слизистой оболочки, поэтому при гиповитаминозе В9 может наблюдаться диарея. Развитие авитаминоза В9 может вызвать использование сульфаниламидных препаратов. Эти препараты являются структурными аналогами парааминобензойной кислоты и ингибируют синтез фолиевой кислоты у микроорганизмов. Некоторые производные птеридина (аминоптерин и метотрексат) тормозят рост быстороделящихся клеток. Они используются в лечебной практике для подавления роста опухолевых клеток. Применение В9 в медицинской практике. В качестве лекарственных средств используются два препарата: фолиевая кислота и фолинат кальция. Фолинат кальция – кальциевая соль фолиновой кислоты, которая является активным метаболитом фолиевой кислоты. Фолинат кальция применяется как антагонист побочного действия противоопухолевого препарата метатрексата. Показаниями для применения фолиевой кислоты являются, прежде всего, макроцитарная анемия, которая чаще развивается у беременных женщин. Фолиевую кислоту применяют при прогрессирующих энтеритах (болезнь «спру»). Витамин В12, кобаламин, антианемический витамин Витамин В12 был выделен из печени в кристаллическом виде в 1948 г. В 1955 г. Дороти Ходжкин с помощью рентгено-структурного анализа расшифровала структуру этого витамина, а в 1964 г. за эту работу ей была присуждена Нобелевская премия. Витамин В12 - единственный витамин, содержащий в своём составе ион кобальта. B12 имеет самую сложную по сравнению с другими витаминами структуру, основой которой является корриновое кольцо (рис. 21).
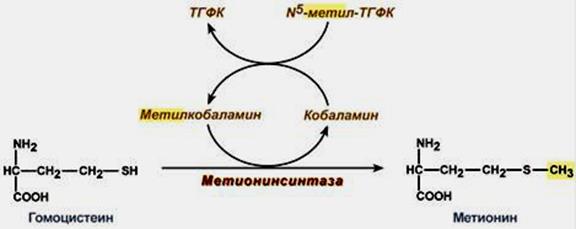
Рис. 21. Структурная формула витамина В12 Корриновое кольцо отличается от порфирина, входящего в состав гема и цитохромов, тем, что два пиррольных цикла в его составе соединены между собой непосредственно, а не метиленовым мостиком. В центре корриновой структуры располагается атом кобальта, который образует четыре координационные связи с атомами азота четырех восстановленных пиррольных колец и одну с атомом азота 5,6-диметил-бензимидазола. Остаток 5,6-диметилбензимидазола связан с остатком рибозы, фосфорилированным по 3-ему атому углерода. Вся структура получила название «кобаламин». Последняя, шестая координационная связь кобальта остаётся свободной, по ней могут присоединятся различные группы (цианогруппа, гидроксильная, метильная или 5'-дезоксиаденозильный остаток). Ковалентная связь углерод-кобальт в структуре цианокобаламина— единственный в живой природе пример ковалентной связи металл-углерод. Суточная потребность и распространение в природе. Кобаламин – это единственный витамин, который синтезируется исключительно прокариотами. Из животных тканей наиболее богаты витамином В12 печень и почки. Основные источники витамина В12 для человека – мясо, говяжья печень, почки, рыба, молоко, яйца. Кобаламин синтезируется микрофлорой кишечника при условии достаточного поступления кобальта с пищей. Суточная потребность в витамине В12 для взрослого человека составляет около 3 мкг (0,003 мг). Биологическая роль витамина В12.. Впервые коферменты, образующиеся из В12, были выделены Г. Баркером и сотр. в 1958 г. из микроорганизмов. Позже было доказано их существование в тканях животных. С участием кобаламина происходит образование двух коферментов: метилкобаламина (СН3-В12) в цитоплазме и дезоксиаденозилкобаламина в митохондриях. Метилкобаламин участвует в реакциях трансметилирования в роли промежуточного переносчика метильной группы. Единственный фермент, коферментом которого является метилкобаламин - это 5-метилтетрагидрофолат-гомоцистеин-метилтрансфераза (метионинсинтаза). Фермент катализирует превращение аминокислоты гомоцистеина в аминокислоту метионин (рис.22).
Рис. 22. Синтез метионина. Донором метильной группы для образования метилкобаламина является N5-метилтетрагидрофолевая кислота, поэтому обмен витамина В9 и В12 в организме человека тесно взаимосвязаны. Второй кофермент, образуемый из витамина В12 - 5-дезоксиаденозилкобаламин, участвует в реакциях внутримолекулярного переноса групп (изомеризации). Данные реакции протекают по схеме:
В организме человека с участием 5-дезоксиаденозилкобаламина идет только одна реакция изомеризации молекулы метилмалонил-КоА в сукцинил-КоА (рис. 23). Эта реакция протекает в ходе обмена жирных кислот с нечётным числом углеродных атомов и аминокислот с разветвлённой углеводородной цепью.
Рис. 23. Реакция изомеризации метилмалонил-Ко в сукцинила-КоА. Гипо- и авитаминоз. У человека и животных недостаток витамина В12 приводит к развитию злокачественной макроцитарной, мегалобластической, пернициозной анемии. Помимо изменений кроветворной функции, для авитаминоза В12 специфичны также нарушения деятельности нервной системы. Нарушения гемопоэза развиваются на фоне органических поражений слизистой оболочки желудка, резкого снижения кислотности желудочного сока. Сходные патологические симптомы развиваются и после резекции желудка. Дело в том, что для активного всасывания витамина В12 в тонкой кишке обязательным условием является наличие в желудочном соке особого белка – гастромукопротеина, получившего название внутреннего фактора Касла (витамин В12, называют внешним фактором Касла). Внутренний фактор Касла специфически связывает витамин В12 в особый сложный комплекс с участием ионов кальция, комплекс необходим для транспорта витамина В12 в энтероциты. В плазме крови витамин В12 переносится в комплексе со специфическими белками транскобаламинами, один из которых способствует депонированию этого витамина в организме. Нарушение синтеза внутреннего фактора Касла в слизистой оболочке желудка приводит к развитию авитаминоза В12 даже при наличии в пище достаточного количества кобаламина. В подобных случаях витамин с лечебной целью обычно вводят парентерально или с пищей, но в сочетании с желудочным соком, в котором содержится внутренний фактор. Также описаны формы пернициозной анемии, обусловленные наследственными дефектами синтеза коферментов метилкобаламина и/или дезоксиаденозилкобаламина. В этих случаях даже 1000-кратная доза витамина В12 не оказывает лечебного эффекта. Участие метилкобаламина в обмене цистеина и метионина, а дезоксиаденозилкобаламина в изомеризации метилмалонилКоА, объясняет такие биохимические показатели недостаточности витамина В12, как метилмалонилацидурия и гомоцистинурия. При дефиците витамина B12 на фоне анемической клинической картины или без неё могут возникнуть неврологические расстройства, в том числе демиелинизация и необратимая гибель нервных клеток. Симптомами такой патологии являются онемение или покалывание конечностей и атаксия. Имеются данные о влиянии дефицита витамина B12 на появление клинических депрессий у пожилых пациентов. Неврологические симптомы при авитаминозе В12 связано с токсичностью метилмалоновой кислоты, накапливающейся в организме при распаде жирных кислот с нечётным числом углеродных атомов, а также некоторых аминокислот с разветвлённой цепью. Применение витамина В12 в медицинской практике. В качестве лекарственных средств выпускаются цианокобаламин и коферментная форма витамина В12 – 5′-дезоксиаденозилкобаламин под названием «кобабамид». Они используются для лечения мегалобластических анемий, в том числе форм, которые сопровождаются неврологическими нарушениями и не поддаются лечению фолиевой кислотой. Кроме того препараты витамина В12 применяются для ослабления симптомов депрессии, при лечении невралгии, для профилактики заболеваний сердца, при поражении нервной системы при сахарном диабете, при рассеянном склерозе и тинните (звоне в ушах).
|
|||||||||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 157; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.85.76 (0.054 с.) |