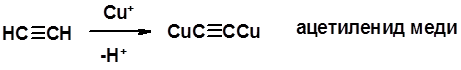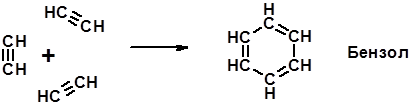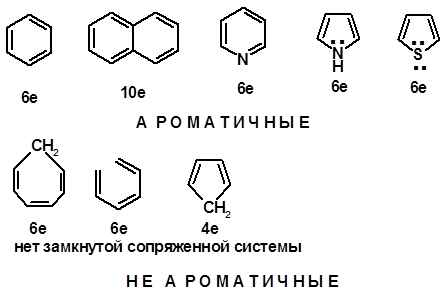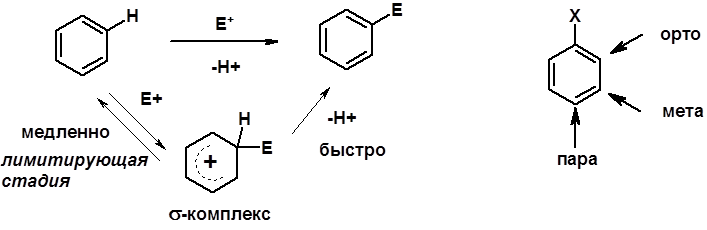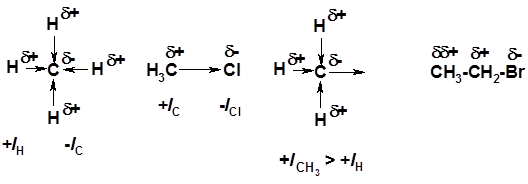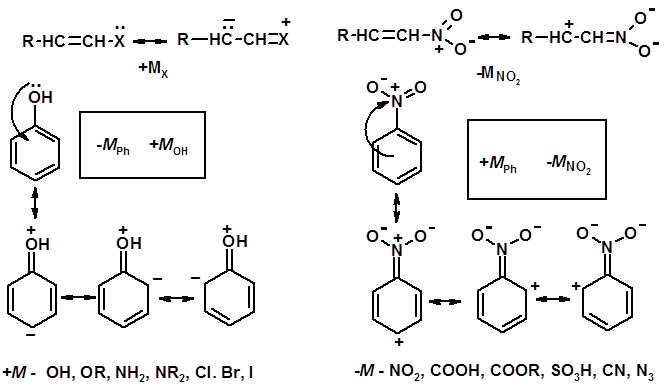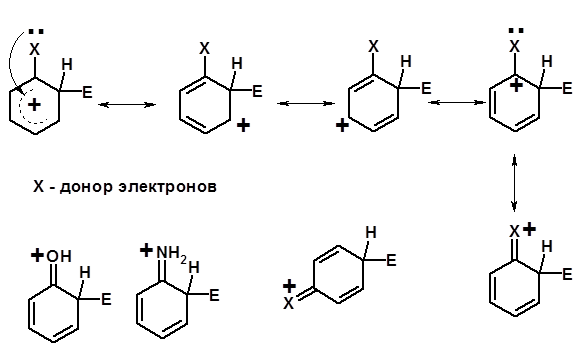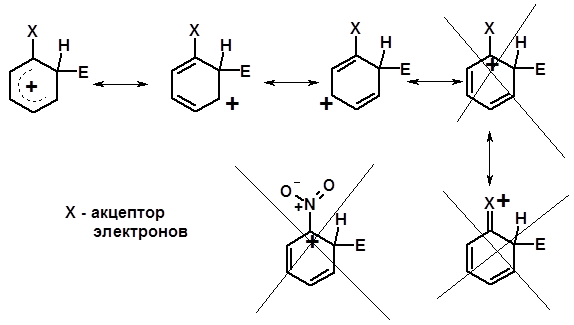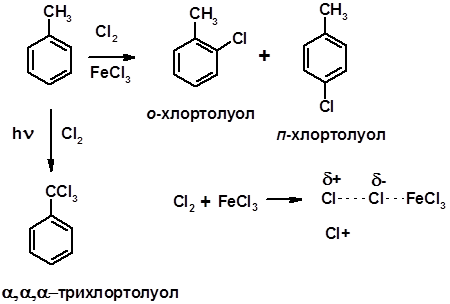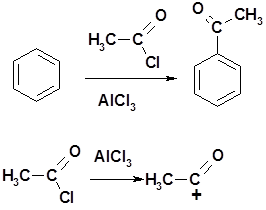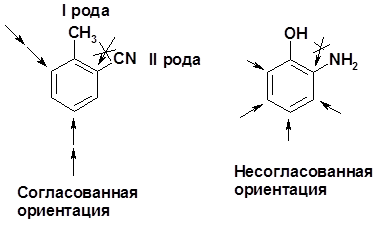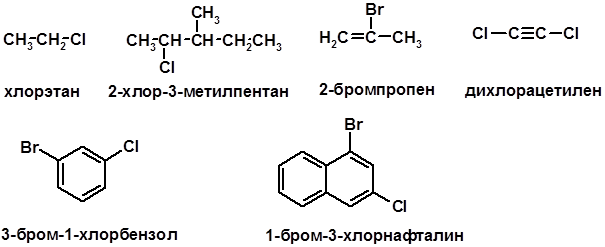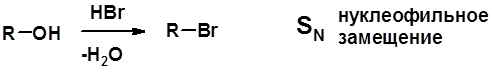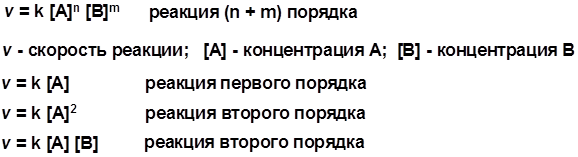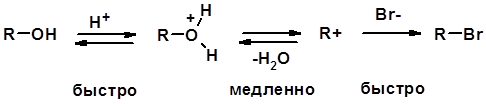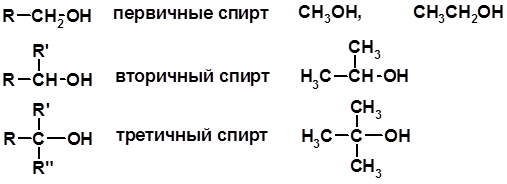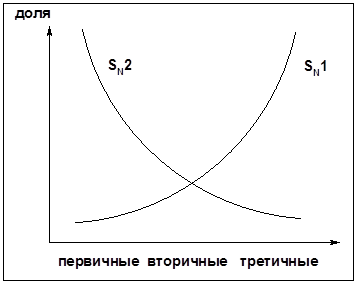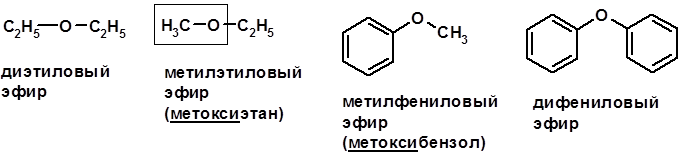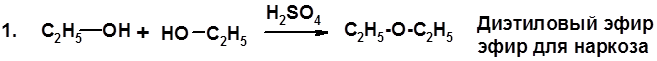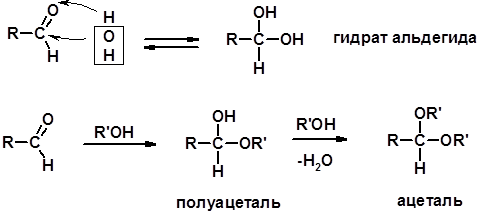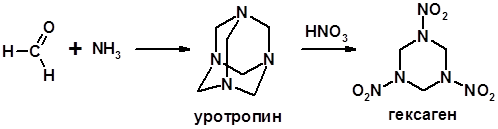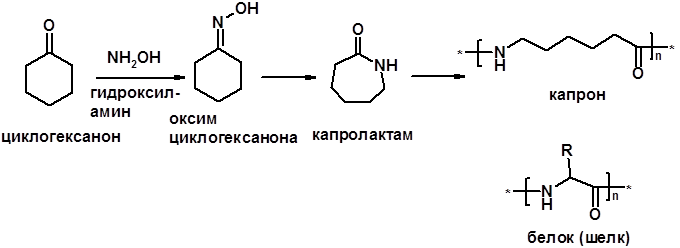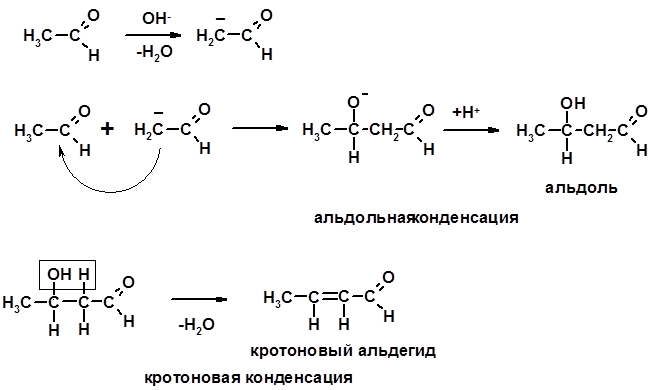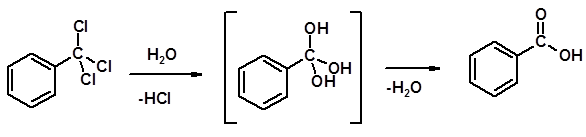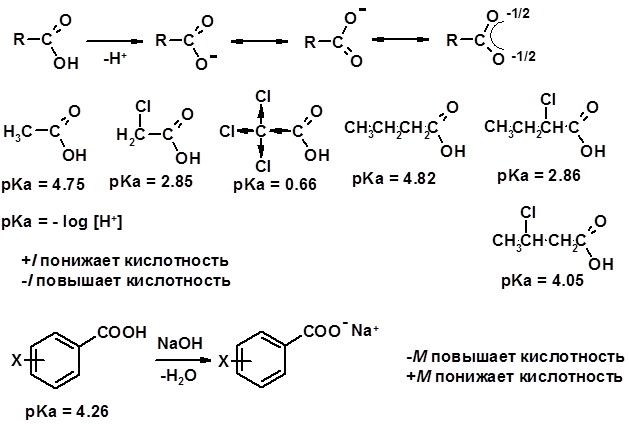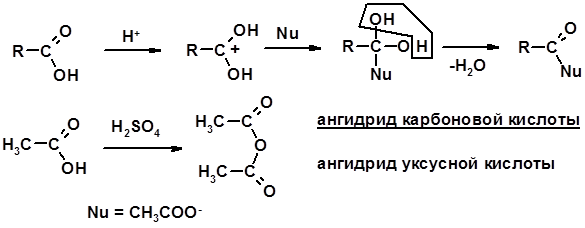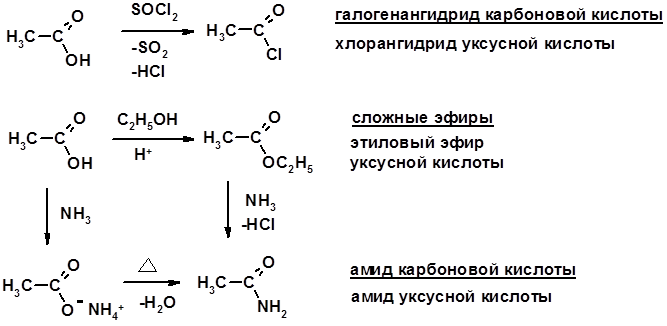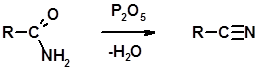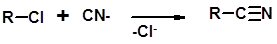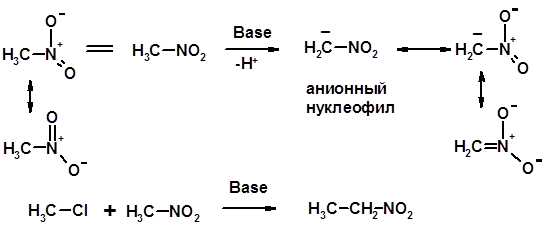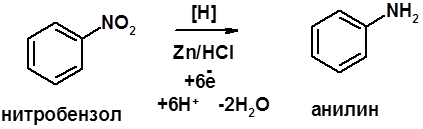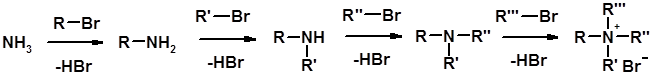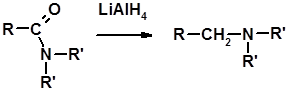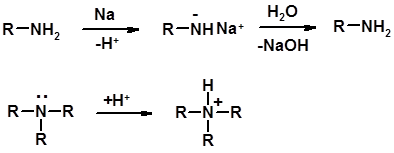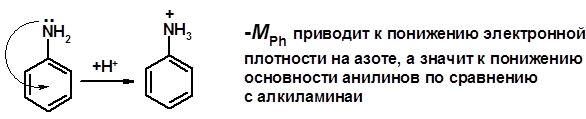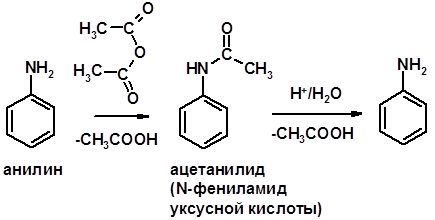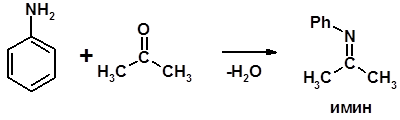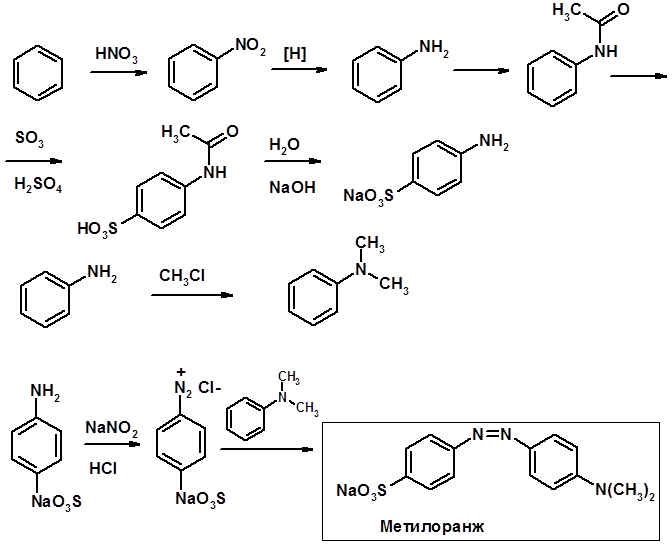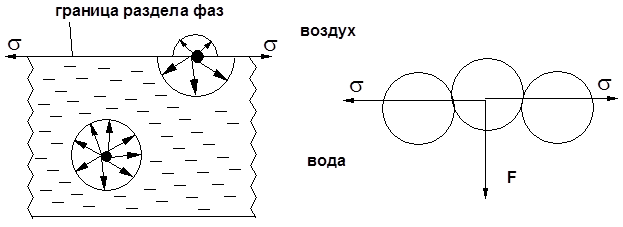Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Внутримолекулярная реакция ВюрцаСтр 1 из 4Следующая ⇒
Механизм реакции
Сульфохлорирование
Cульфоокисление Нитрование Горение
Управляемое окисление
Циклоалканы CnH 2 n
Получение Внутримолекулярная реакция Вюрца
Хим. свойства см. алканы Реакции присоединения (для напряженных циклов С3-С4)
АЛКЕНЫ С n H 2 n ненасыщенные углеводороды с двойной связью Номенклатура - Двойная связь sp 2 -гибридизация
Пространственная изомерия относительно двойной связи
Способы получения Дегидратация спиртов
Дегидрогалагениерование галогеналканов
Дегалагениерование 1,2-дигалогеналканов
Дегидрирование алканов
Химические свойства Реакция присоединения Гидрирование
Присоединение галогеноводорода
Гидратация
4. Окисление KMnO4
Озонолиз
Алкадиены
Классификация диенов
Особенности хим. свойства сопряженных диенов, по сравнению с алкенами Присоединение
Диеновый синтез (реакция Дильса-Альдера)
АЛКИНЫ
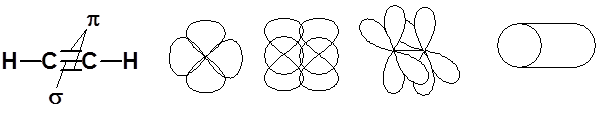
Sp - гибридизация углерода при тройной связи
Методы получения 1. Дегидрогалогенирование 1,1- и 1,2-дигалогеналканов
Химические свойства Гидрирование
Галогенирование
3. Гидрогалогенирование
Винилирование
5. Кислотность алкинов с концевой тройной связью
6. Циклизация Ароматические углеводороды (арены)
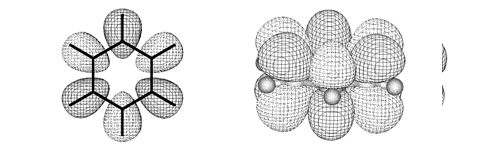
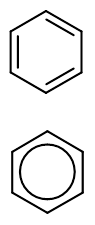
Углерод в ароматическом ядре – sp 2 -гибридизован Принцип ароматичности – принцип Хюккеля Замкнутая циклическая система сопряженных p -электронов 2) Количество p -электронов – 4 n +2 (n = 0, 1, 2...)
Сопряжение
Химические свойства Электрофилы (Е+) – акцепторы электронной плотности E+ = R+ (H3C+) – карбокатионы, NO2+, Br+, SO3, и др. Нуклеофилы (Nu-) – доноры электронной плотности Nu- = R- (H3C-) – карбанион, ОН-, RO-, NH2-, Br-, HOH, RNH2 и др. Электрофильное ароматическое замещение SEAr
Влияние заместителей в бензольном кольце на реакцию SEAr Электронные эффекты заместителей
Индуктивный эффект (I – эффект) – изменение распределения электронной плотности в молекуле из=за разницы электроотрицательности атомов.
Мезомерный эффект (М – эффект) – возникает в сопряженных системах (заместитель связан с sp 2 - или sp -гибридизованным углеродом)
Заместители I рода – направляют реакцию в орто - и пара -положение СН3 (R), OH, OR, NH 2, NR 2 (ускоряют реакцию), Cl, Br, I (замедляют) + I или + М - I, но + M
Заместители I I рода – направляют реакцию в мета -положение и замедляют реакцию NO2, NO, СООН, COOR, SO3H, CN, N3, C С l3 - M и/или - I
Хлорирование
Нитрование
3. Сульфирование
Алкилирование по Фриделю-Крафтсу
Ацилирование по Фриделю-Крафтсу
Согласованная ориентация
ГАЛОГЕНУГЛЕВОДОРОДЫ (Hal = F, Сl, Br, I) Способы получения 1. Галогенирование алканов (см. алканы) 2. Гидрогалогенирование алкенов и алкинов (см. алкены, алкины) 3. Присоединение галогенов к алкенам и алкинам (см. алкены, алкины) 4. Реакции спиртов с галогеноводородами
Два основных механизма реакции нуклеофильного замещения: Уравнение скорости реакции: A + B ® C SN1 v = k [R-OH]
Лимитирующая стадия – образование карбокатиона, значит протекание всей реакции зависит от стабильности самого карбокатиона
SN2 v = k [R-OH] [Hal-]
Химические свойства 1. Отщепление галогеноводорода (см. получение алкенов и алкинов) 2. Реакция Вюрца (см. получение алканов) 3. Нуклеофильное замещение галогена (для алифатических галогенуглеводородов)
Реакцию можно рассматривать как введение остатка алифатического углеводорода (алкила) в другую молекулу – реакция алкилирования, а галогенуглеводород – алкилирующий агент
4. Ароматическое нуклеофильное замещение - возможно только для активированных сильными акцепторами (нитро-группа) аренов
5. Получение магнийорганических соединений (реактивов Гриньяра)
СПИРТЫ и ФЕНОЛЫ (ОН – гидроксил или гидрокси-группа) (приставка для обозначения гидроксила – гидрокси, суффикс – ол)
Методы получения Получение спиртов Получение фенолов Химические свойства Простые эфиры
Методы получения
Методы получения Химические свойства 1. Реакции с водой и спиртами
Реакции с аммиаком
3. Реакции с аминами и их производными (присоединение-отщепление)
4. Конденсации СН-кислотность – карбонильные соединения способны отдавать протон от a -углеродного атома
Если нет протона в a-положении, то происходит реакция Каниццарро
5. Окислительно-восстановительные реакции
Карбоновые кислоты
Методы получения 1. Окисление первичных спиртов и альдегидов 2. Гидролиз трихлорметильных производных аренов
3. Гидролиз сложных эфиров (омыление)
Химические свойства Карбоновых кислот 1. Кислотность (образуют соли в реакциях даже со слабыми основаниями)
2. Реакции с нуклеофилами
Углерод карбоксильной группы малоактивен по отношению к нуклеофилам (по сравнению с карбонильной группой) из-за + М гидроксила, для активации карбоновых кислот применяют протонирование, вносящее положительный заряд
Получение Дегидратация амидов
Цианирование галогеналканов
Гидролиз нитрилов
Хим. свойства СН-кислотность нитроалканов
Восстановление нитроаренов
Амины
Методы получения Алкилирование аммиака
Восстановление амидов
Восстановление нитрилов
Кислотно-основные сойства
ü Основность – способность принимать протон или отдавать пару электронов ü Основность амина тем выше, чем выше электронная плотность на азоте. ü Донорные заместители у азота повышают электронную плотность на азоте, а значит повышают основность амина. ü Акцепторные заместители у азота понижают электронную плотность на азоте, а значит понижают основность амина.
Ацилирование
4. Реакции с карбонильными соединеиями (образование иминов)
Первичные амины
Синтез метилоранжа
Синтетические полимеры Полимер – макромолекула, построенная из одинаковых повторяющихся фрагментов (мономерных единиц). Мономер – исходное для полимера низкомолекулярное вещество – определяет строение всего полимера. Полимерная цепь может состоять из повторяющихся фрагментов одного типа или нескольких разных типов. В последнем случае говорят о сополимере.
Типы полимеров: - Термопласт – полимер, способный легко менять форму при нагревании (полиэтилен, полипропилен, полиэтилентерефталат, полистирол ….) - Эластопласт – способен растягиваться в несколько раз и обратимо восстаннавливать форму после снятия деформирующего усилия (каучуки, резины) - Реактопласт – полимер, в котором при обработке протекают необратимые реакции дополимеризации, что делает невозможность их дальнейшей термической деформации (обработки) Химия поверхностно-активных веществ (ПАВ)
Механизм реакции
Сульфохлорирование
Cульфоокисление Нитрование Горение
Управляемое окисление
Циклоалканы CnH 2 n
Получение Внутримолекулярная реакция Вюрца
Хим. свойства см. алканы Реакции присоединения (для напряженных циклов С3-С4)
АЛКЕНЫ С n H 2 n ненасыщенные углеводороды с двойной связью Номенклатура - Двойная связь sp 2 -гибридизация
Пространственная изомерия относительно двойной связи
Способы получения Дегидратация спиртов
|
|||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 192; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.224.59.231 (0.09 с.) |
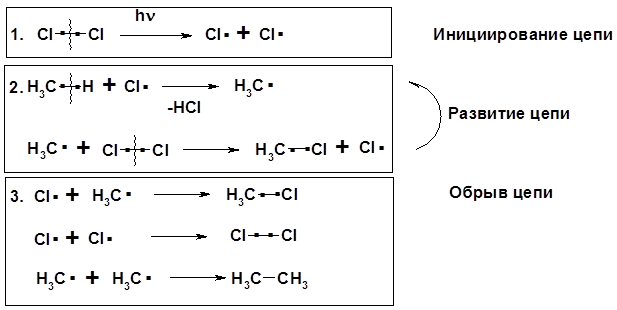

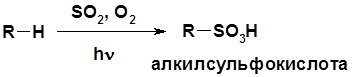
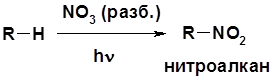
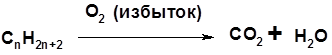
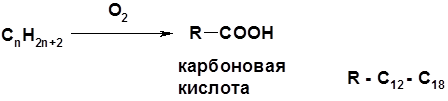
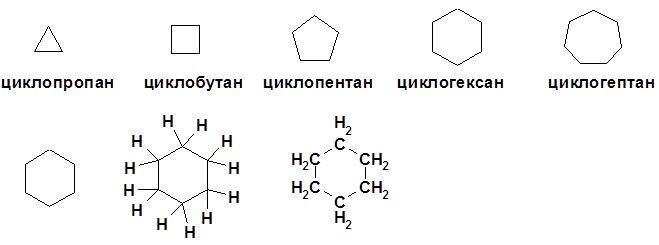

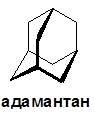
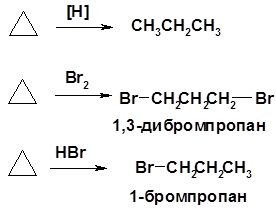

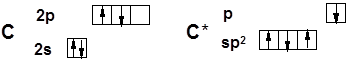
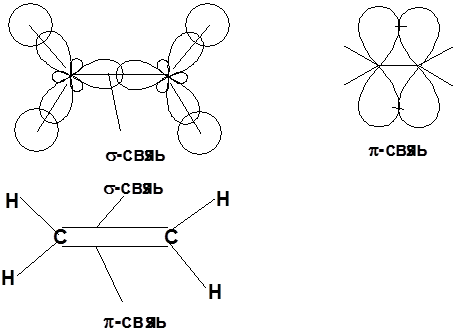

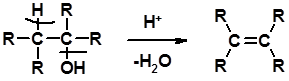
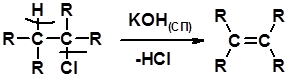
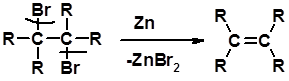
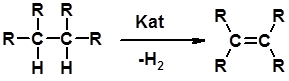

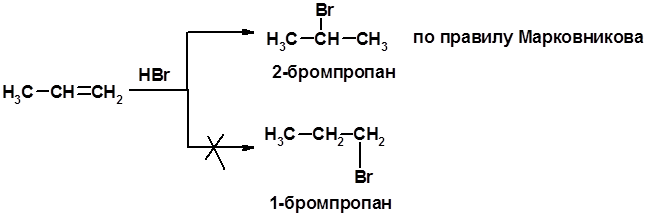

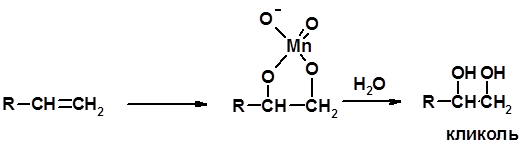

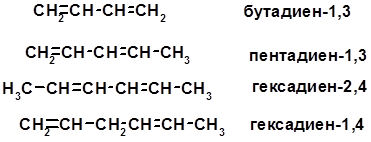
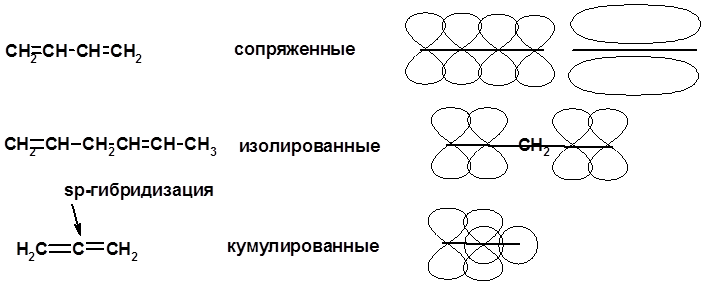
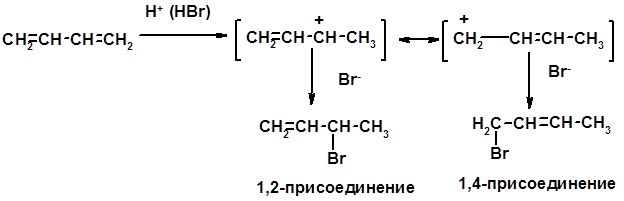
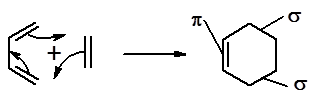 Из 3 p -связей образуется новые 1 p - и 2 s -связи
Из 3 p -связей образуется новые 1 p - и 2 s -связи
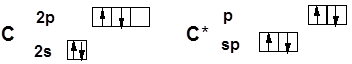


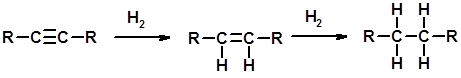

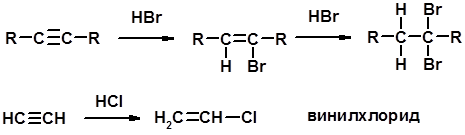
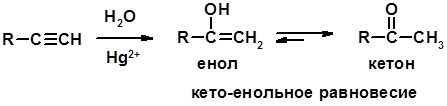
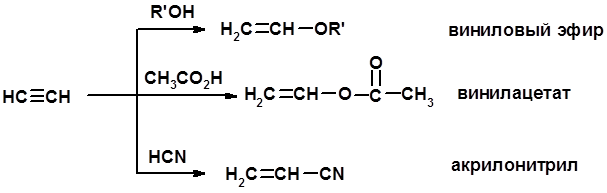
 Соли алкинов – ацетилениды
Соли алкинов – ацетилениды