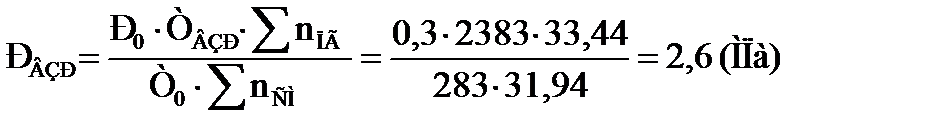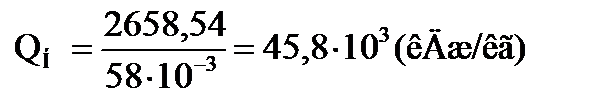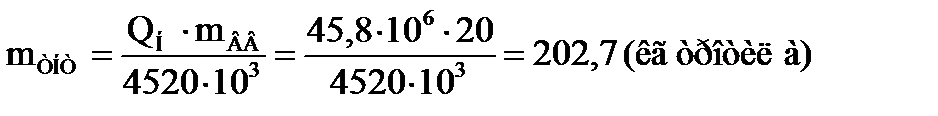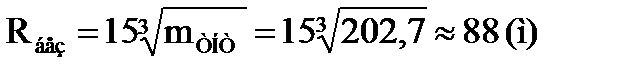Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема 1. Физико-химические основы горенияСтр 1 из 14Следующая ⇒
Тема 1. Физико-химические основы горения Цель: дать обучающимся современные, целостные взаимосвязанные знания о физико-химической природе процессов горения и взрыва и механизме химического взаимодействия при этих явлениях, изучить классификацию процессов горения и взрыва. Учебные вопросы: 1. Общие сведения о горении и взрыве. 2. Механизм химического взаимодействия при горении. Энергия активации. Методические рекомендации по изучению темы Данная тема дает общие представления об основных физических и химических процессах, протекающих при горении, знакомит обучающихся с различными видами и режимами горения. 1. Изучите данную тему с использованием материала лекций и учебной литературы. 2. Заучите определения основных понятий (см. опорные термины, словарь терминов расположен в конце данных методических указаний). 3. Горение – основной процесс на пожаре, поэтому изучение явления горения следует начинать с рассмотрения механизма протекания элементарных реакций. Следует вспомнить законы химической кинетики, которые изучались в курсе общей химии (влияние температуры, концентрации реагирующих веществ и наличия катализаторов/ингибиторов на скорость химической реакции). Обратите внимание на условия возникновения горения, механизмы его протекания. Упомянутые вопросы из раздела химической кинетики важны для объяснения понятий концентрационных пределов воспламенения, механизма действия огнетушащих веществ и т.д. 4. Разберите классификацию процессов горения. Классифицируйте горение костра (свечи, газовой горелки, газового фонтана, жидкости в резервуаре) по всем параметрам. Результаты удобно записать в виде таблицы.
Изучив тему, обучающийся должен: З нать: - физико-химическую природу возникновения горения и взрыва; - структуру пламени; - химизм взаимодействия горючего вещества и окислителя; - типы взрывов. Уметь: - составлять уравнения химических реакций горения веществ в воздухе;
- классифицировать процессы горения. Владеть: - научной терминологией, изученной в рамках темы.
Вопросы для самоконтроля 1. Дать определение процессам горения и взрыва. 2. Перечислите условия, необходимые для возникновения горения. 3. Какие явления сопровождают процесс горения? 4. Назовите поражающие факторы дыма. 5. Какие виды источников зажигания вы знаете? 6. Назовите способы передачи тепла от пламени к горючему веществу. 7. Классификация процессов горения по механизму распространения зоны горения по горючей смеси и по агрегатному состоянию горючего вещества и окислителя. 8. Классификация процессов горения по соотношению скорости смесеобразования и скорости реакции горения и по газодинамическому состоянию компонентов смеси. 9. Классификация процессов горения по полноте сгорания. Приведите примеры продуктов полного и неполного сгорания. Что влияет на полноту горения, почему? 10. Понятие энергии активации. Опорные термины по теме «Физико-химические основы горения»: горение, окислитель, восстановитель, пламя, взрыв. Тесты для самоконтроля 1. Окисление, протекающее с высокой скоростью, и выделением большого количества тепловой и световой энергии называется. a. свечением b. подогреванием c. горением d. взрывом e. дроблением 2. Для возникновения горения необходимо наличие следующих факторов… a. источник зажигания b. взрыв c. горючее вещество d. окислитель e. восстановитель 3. При значениях Re < 2300 режим горения? a. ламинарный b. переходный c. турбулентный d. вихревой e. волнистый 4. Какие продукты образуются при полном сгорании веществ? a. СО2 b. СО c. N Н3 d. НС l e. Н2О
5. Экзотермическая реакция окисления вещества сопровождающаяся, по крайней мере, одним из трёх факторов: пламенем, свечением, выделением дыма - это? a. свечение b. горение c. подогревание d. взрыв e. брожение 6. Процесс, при котором массообмен и перенос осуществляются не только за счет молекулярной, но и турбулентной диффузии, в результате макроскопического вихревого движения газовых слоев горючей смеси - это?
a. Диффузионное горение b. Турбулентное горение c. Кинетическое горение d. Гомогенное горение e. Ламинарное горение
7. При значениях 2300 < Re < 10000 режим горения является … a. переходный b. вихревой c. турбулентный d. ламинарный e. волнистый 8. Быстропротекающий, окислительно-восстановительный, экзотермический, самоподдерживающийся процесс, часто сопровождающийся образованием пламени - это? a. свечение b. взрыв c. тление d. горение e. брожение
9. При значениях Re > 10000 режим горения? a. турбулентный b. переходный c. волнистый d. вихревой e. ламинарный
10. Горение, при котором передача тепловой энергии к свежей горючей смеси осуществляется за счет излучения и теплопроводности (скорость движения тепловой волны по горючей смеси от 0,5 до 50 м/с) - это? a. Дефлаграционное горение b. Турбулентное горение c. Кинетическое горение d. Детонационное горение e. Ламинарное горение 11. При неполном сгорании образуются продукты? a. СО2 b. СО c. Н2О d. НСN e. N Н3
12. Процесс взаимодействия горючего и окислителя, находящихся в зоне химической реакции в одинаковом агрегатном состоянии - это? a. Гомогенное горение b. Гетерогенное горение c. Кинетическое горение d. Диффузионное горение e. Ламинарное горение
13. Газовый объём, в котором непосредственно происходит реакция горения называется…
a. Горение b. Взрыв c. Пламя d. Свечение e. Энтропия
14. Минимальная энергия реагентов, достаточная для того, чтобы они вступили в химическую реакцию, то есть преодолели барьер на поверхности потенциальной энергии, через который должна пройти система в ходе элементарного акта химического превращения - это? a. Энергия дезактивации b. Энергия Гиббса c. Энергия ядер в атомах d. Энергия активации e. Энергия разрыва химической связи
15. Процесс взаимодействия горючего и окислителя, находящихся в различных агрегатных состояниях, горение происходит на поверхности раздела фаз - это? a. Гомогенное горение b. Гетерогенное горение c. Кинетическое горение d. Диффузионное горение e. Ламинарное горение
для самостоятельной подготовки по теме Основная: 1. Корольченко А.Я. Процессы горения и взрыва. – М.: Пожнаука, 2007. – 266с., ил. (стр. 8 - 19) 2. Корольченко А.Я., Корольченко Д.А.. Пожаровзрывоопасность веществ и материалов и средства их тушения. Справочник: в 2-х ч. – 2-е изд., перераб. и доп. – М.: Асс. Пожнаука, 2004. – Ч.I. – 713 с. Дополнительная: 3. Марков В.Ф., Маскаева Л.Н., Миронов М.П., Пазникова С.Н. Физико-химические основы развития и тушения пожаров: Учебное пособие для курсантов, студентов и слушателей образовательных учреждений МЧС России / Под ред. Маркова В.Ф.. Екатеринбург: УрО РАН. 2009. 274 с.
Вопросы для самоконтроля 1. Классификация взрывов. 2. Какие правила необходимо соблюдать при составлении реакций горения? 3. Какие вещества называют горючими, трудногорючими и негорючими? 4. Как определить горючесть вещества по коэффициенту горючести? 5. Избыток воздуха, коэффициент избытка воздуха. 6. Какие вещества называются сложными? 7. Дать определение индивидуальным химическим соединениям. 8. Сформулируйте закон Гесса и следствие из закона Гесса. 9. Теплота сгорания, ее виды.
10. Дайте определение калориметрической температуре сгорания. 11. Какие факторы влияют на температуру горения? 12. Для чего необходимо знать температуру горения? 13. Как определяют температуру горения? Почему действительная температура горения, как правило, оказывается ниже калориметрической, адиабатической и теоретической? 14. Строение ламинарного диффузионного пламени. 15. Изложите в общем виде методику расчета объема воздуха, необходимого для сгорания индивидуальных химических соединений и сложных веществ. Опорные термины по теме «Материальный и тепловой баланс процесса горения»: температура горения, температура внутреннего пожара, температура наружного пожара, теплота сгорания, низшая теплота сгорания, высшая теплота сгорания.
По формуле Д.И. Менделеева А) Для сложного вещества переменного состава. Для сложных веществ переменного состава, находящихся в твёрдом и жидком агрегатных состояниях, а также химических соединений, для которых отсутствует справочное значение теплоты образования, теплоту сгорания рассчитывают по формуле Д. И. Менделеева. В этом случае вычисления проводят с использованием массовых долей элементов в горючем веществе: Qн = 339,4×wС + 1257×wН – 108,9(wО + wN – wS)– 25,1(9×wН + wW), кДж/кг где wW - массовая доля влаги в горючем веществе, %. wС, wН, wO, wS, wN - содержание в горючем веществе углерода, водорода, кислорода, серы, азота, масс. %;
Б) Для индивидуального химического соединения. 1. Рассчитываем молярную массу горючего вещества. 2. Рассчитываем массовую долю элементов в соединении по формуле
где ni и Ari – число атомов и относительная атомная масса i-элемента в молекуле горючего вещества, М - молярная масса горючего вещества. 3. Подставляем полученные значения в формулу Д.И. Менделеева Тесты для самоконтроля
1. В зависимости от механизма распространения зоны химической реакции горения по горючей смеси выделяют следующие режимы горения: a. дефлаграционное и детонационное; b. ламинарное и турбулентное; c. диффузионное и кинетическое.
2. Какие из ниже перечисленных продуктов горения являются продуктами полного сгорания: a. СО2; b. N Н3; c. Н Cl; d. Н2О; e. СО.
3. Укажите, какие из представленных ниже уравнений реакции горения веществ являются верными: a. С2Н5 N + 6,25 О2 + 6,25 ´ 3,76 N 2 ® 7СО2 + 2,5 Н2О + 6,25 ´ 3,76 N 2; b. С2Н3 Cl + 2,5 О2 + 2,5 ´ 3,76 N 2 ® 2СО2 + Н2О + HCl +2,5 ´ 3,76 N 2;
c. С4Н10О + 6 О2 + 6 ´ 3,76 N 2 ® 4СО2 + 5 Н2О + 6 ´ 3,76 N 2.
4. Как называются вещества, состав которых можно выразить химической формулой? a. простые вещества; b. индивидуальные химические соединения; c. сложные вещества.
5. Горение паров, поднимающихся со свободной поверхности жидкости, является: a. гетерогенным; b. гомогенным.
6. Если коэффициент горючести бутанола равен 24, то это вещество: a. трудногорючее; b. горючее; c. не горючее.
7. По газодинамическому состоянию компонентов горючей смеси горение подразделяется на: a. полное и неполное; b. ламинарное и турбулентное; c. гомогенное и гетерогенное. 8. Для возникновения горения необходимы следующие условия: a. наличие горючего вещества, окислителя и флегматизатора; b. наличие источника зажигания и горючего вещества; c. наличие горючего вещества, источника зажигания и окислителя.
9. Какие из ниже перечисленных факторов влияют на температуру горения: a. полнота сгорания; b. величина избытка воздуха; c. объем сосуда; d. начальная температура горючего вещества и воздуха; e. скорость химической реакции.
10. С помощью какого прибора определяется температура горения? a. прибор МакHИИ; b. прибор Маккея; c. СТС-2; d. ОППИР-017; e. ПВHЭ. 11. Какая температура называется температурой внутреннего пожара: a. максимальная температура дыма в помещении, где происходит пожар; b. минимальная температура дыма в помещении, где происходит пожар; c. средняя температура зоны горения в помещении, где происходит пожар; d. максимальная температура зоны горения в помещении, где происходит пожар; e. средняя температура дыма в помещении, где происходит пожар.
12. Какая температура называется температурой наружного пожара: a. температура дыма; b. температура пламени; c. температура продуктов горения; d. температура окислителя; e. температура горючего вещества. 13. Коэффициент горючести вещества равен 1. Данное вещество является: a. горючим; b. негорючим; c. трудногорючим. 14. Какие различают температуры горения? a. оптическую, теоретическую, действительную; b. тепловую, теоретическую, действительную; c. калориметрическую, теоретическую, действительную; d. отопительную, теоретическую, действительную; e. цепную, теоретическую, действительную.
15. Как называется коэффициент "К". a. коэффициент дымообразования; b. коэффициент горючести; c. коэффициент теплопроводности; d. коэффициент теплопередачи; e. стехиометрический коэффициент.
Вопросы для самоконтроля 1. Основы тепловой теории академика Н.Н. Семёнова. 2. Тепловое и цепное самовоспламенение, условия их возникновения. 3. Примеры (схемы) разветвляющейся и не разветвляющейся цепной реакции. 4. Температура самовоспламенения, её практическое значение. Методы определения. 5. Огнепреградители. Принцип работы, область применения. 6. Влияние объема и формы сосуда на температуру самовоспламенения. 7. Влияние состава газовой смеси на температуру самовоспламенения.
8. Влияние давления, наличия катализаторов на температуру самовоспламенения. 9. Сущность процесса самовозгорания, его отличие от самовоспламенения и воспламенения 10. Тепловое самовозгорание масел. 11. Способы определения склонности масел, жиров и олиф к самовозгоранию. Йодное число. Меры профилактики самовозгорания промасленных материалов. 12. Самовозгорание каменных углей. Профилактика самовозгорания. 13. Причины самовозгорания сульфидов металлов. Способы предупреждения самовозгорания сульфидов металлов. 14. Микробиологическое самовозгорание. Профилактика самовозгорания. 15. Самовозгорание химических веществ, при контакте с кислородом воздуха, режим их хранения. 16. Самовозгорание веществ при контакте с водой, способы их хранения. 17. Способы тушения щелочных металлов, карбидов и гидридов щелочных и щелочноземельных металлов. 18. Вещества, самовозгорающиеся при контакте с окислителями. 19. Факторы, влияющие на самовозгорание материалов. Опорные термины по теме «Условия возникновения и развития процессов горения»: самовоспламенение, температура самовоспламенения, самовозгорание, йодное число, пирофорные вещества. Смеси газов 1. Находим нижний и верхний концентрационные пределы распространения пламени веществ, входящих в состав смеси, при стандартных условиях. 2. Расчет нижнего и верхнего концентрационных пределов распространения пламени смеси нескольких паров или газов ведут по формуле Ле-Шателье, которая выражает правило смешения. В основу формулы положено предположение, что несколько газов, находящихся на Н(В)КПР, при смешении образуют смесь, также находящуюся на нижнем (верхнем) пределе воспламенения. Формула Ле-Шателье справедлива для подавляющего большинства смесей веществ, не вступающих в химическую реакцию.
где
Задача. Рассчитать концентрационные пределы распространения пламени смеси, состоящей из 30 об. % пропана и 70 об. % этана. Дано: Обозначим С3Н8 цифрой 1, С2Н6 – 2. j1 = 30 %; j2 = 70 %. Найти: Решение: 1. Составляем уравнения реакции горения пропана и этана в воздухе: С3Н8 + 5(О2 + 3,76N2) ® 3СО2 + 4Н2О + 5×3,76N2 b=5 С2Н6 + 3,5(О2 + 3,76N2) ® 2СО2 + 3Н2О + 3,5×3,76N2 b=3,5
2. Рассчитываем нижний и верхний концентрационный пределы распространения пламени пропана при стандартных условиях.
Так как b = 5, что меньше 7,5, то для расчета ВКПР по таблице выбираем: а = 1,55 и b = 0,56
Рассчитываем нижний и верхний концентрационный пределы распространения пламени этана при стандартных условиях.
Так как b = 3,5, что меньше 7,5, то для расчета ВКПР по таблице выбираем: а = 1,55 и b = 0,56
3. Рассчитываем нижний и верхний концентрационные пределы распространения пламени смеси пропана и этана по формуле Ле-Шателье:
Ответ: расчётное значение концентрационных пределов распространения пламени пропана 2,08 – 12,03 % (об.), этана 2,85 – 16,71 % (об.); концентрационные пределы смеси, состоящей из 30% (об.) пропана и 70% (об.) этана 2,57 – 14,97 % (об.). Задача. Рассчитать концентрационные пределы распространения пламени метана в г/м3 при температуре 134 0С. Дано: СН4 - метан. Найти: Решение: 1. Составляем уравнения реакции горения метана в воздухе. СН4 + 2(О2 + 3,76N2) ® СО2 + 2Н2О + 2×3,76N2 b=2
2. Рассчитываем нижний и верхний концентрационный пределы распространения пламени метана при стандартных условиях.
Так как b = 2, что меньше 7,5, то для расчета ВКПР по таблице выбираем: а = 1,55 и b = 0,56
3. Рассчитываем нижний и верхний концентрационные пределы распространения пламени метана при температуре 134 0С:
4. Рассчитываем молярную массу метана: М = 12 ∙ 1 + 1 ∙ 4 = 16 кг/кмоль. 5. Определяем объем занимаемый 1 кмоль газа при заданной температуре:
6. Рассчитываем концентрационные пределы распространения пламени метана в г/м3 при температуре 134 0С:
Ответ: расчётное значение концентрационных пределов распространения пламени метана при температуре 134 0С 19,88 – 148,4 г/м3. Пламени жидкостей (ТПР) 1. По справочнику А.Я. Корольченко находим значения концентрационных пределов распространения пламени вещества. 2. Рассчитываем давление насыщенного пара на нижнем и верхнем температурных пределах распространения пламени по формуле:
где Робщ - атмосферное давление при нормальных условиях, (101325 Па); φн(в) - нижний (верхний) КПР. 3. Определяем температурные пределы распространения пламени по уравнению Антуана:
где tН(В) – нижний (верхний) температурные пределы распространения пламени;
А, В, С – константы, определяемые по табл. 10 Приложения 2.
Для определения ТПР можно использовать также табл. 9 приложения 2 с зависимостями давления насыщенного пара жидкостей от температуры. В этом случае величины ТПР рассчитываются методом линейной интерполяции температуры по давлению. Тесты для самоконтроля
1. В чем состоит сущность процесса самовоспламенения? a. Возникновение горения за счет самонагревания вещества без воздействия источника зажигания. b. Возникновение горения от нагретых веществ под действием источника зажигания. c. Возникновение горения за счет нагревания вещества под воздействием источника зажигания.
2.Температура самовоспламенения бывает: a. Стандартная и максимальная. b. Стандартная и минимальная. c. Минимальная и максимальная. d. Расчетная и минимальная.
3.Температуру самовоспламенения рассчитывают по: a. Температуре окружающей среды. b. Агрегатному состоянию вещества. c. Давлению в реакционной массе. d. Средней длине углеродной цепи в молекуле.
4.Температура поверхности технологического оборудования составляет: a. Hе более 80 % от температуры самовоспламенения. b. Более 80 % от температуры самовоспламенения. c. Hе выше температуры самовоспламенения. d. Hе более 20 % от температуры самовоспламенения.
5. Пожарная опасность веществ возрастает, если температура самовоспламенения: a. Увеличивается. b. Уменьшается. c. Постоянна. d. Температура самовоспламенения не является показателем пожарной опасности.
6. Какое вещество более пожароопасно? a. Изобутилбензол (Т самовоспламенения 428 0С). b. Ветинон (Т самовоспламенения 281 0С). c. Винилацетат (Т самовоспламенения 427 0С) d. Винилбутерат (Т самовоспламенения 410 0С). e. Гептан (Т самовоспламенения 223 0С). 7. Назовите условие теплового самовоспламенения? a. Тепловыделение значительно превышает теплоотвод. b. Теплоотвод значительно превышает тепловыделение. c. Тепловыделение равно теплоотводу. d. Теплоотвод незначительно превышает тепловыделение. e. Тепловыделение незначительно превышает теплоотвод.
8.Какое из веществ менее пожароопасно? a. Метиловый спирт (Тсв. = 287 оС). b. Бутиловый спирт (Тсв. = 387 оС). c. Изобутиловый спирт (Тсв. = 381 оС). d. Амиловый спирт (Тсв. = 315 оС). e. Этиловый спирт (Тсв. = 215 оС).
9. Дайте определение температуре самовоспламенения? a. Наименьшая температура источника зажигания, при которой в условиях специальных испытаний наблюдается самовоспламенение. b. Наибольшая температура окружающей среды, при которой в условиях специальных испытаний наблюдается самовоспламенение. c. Наибольшая температура источника зажигания, при которой в условиях специальных испытаний наблюдается самовоспламенение. d. Наименьшая температура окружающей среды, при которой в условиях специальных испытаний наблюдается самовоспламенение.
10. Для чего предназначен прибор СТС? a. Для определения температуры в зоне горения. b. Для определения коэффициента горючести. c. Для определения стандартной температуры самовоспламенения. d. Для определения температуры горения. e. Для определения температуры воспламенения. Вопросы для самоконтроля 1. Дайте определение нижнему и верхнему концентрационным пределам распространения пламени, области воспламенения. 2. Раскройте влияние на область воспламенения мощности источника зажигания, турбулентности, температуры давления смеси. 3. Проанализируйте влияние объема и диаметра сосуда, примесей негорючих газов на область воспламенения веществ. 4. Раскройте влияние дисперсности и адсорбционной способности пыли на ее пожароопасность. 5. Влияние химической активности и склонности к электризации на пожароопасность пыли. Способы электризации пыли. 6. Какие условия должны быть обеспечены для быстрого протекания реакции горения пыли? 7. В чем сходство и отличие горения пыли и горения газо-воздушных смесей? 8. Классификация пылей по пожароопасности. 9. В чем заключаются основные меры предупреждения пожаров и взрывов пылей в производственных условиях? 10. Какие факторы влияют на скорость распространения пламени при горении пыли? 11. Какой показатель лежит в основе классификации жидкостей по пожароопасности? 12. Температура вспышки бутанола равна 350С. К какому разряду ЛВЖ он относится? 13. К какому разряду ЛВЖ относится этиловый спирт, если его температура вспышки равна 130С? 14. Может ли температура вспышки жидкости иметь отрицательное значение? 15. Какую температуру вспышки в закрытом тигле имеют горючие жидкости (ГЖ)? 16. Какое вещество принимается за «А» при расчете температуры вспышки смеси жидкостей? 17. Для чего следует знать и применять значение температуры вспышки, температуры воспламенения и температурных пределов распространения пламени?
Опорные термины по теме «Пожаровзрывоопасные газо-, паро- и пылевоздушные смеси»: Нижний/верхний концентрационный предел распространения пламени, минимальное взрывоопасное содержание кислорода, минимальная флегматизирующаяконцентрация флегматизатора, температура вспышки, температура воспламенения, температурные пределы распространения пламени.
Тесты для самоконтроля
1. При какой температуре следует вести технологический процесс, связанный с применением жидкостей, для обеспечения его пожаробезопасности? a. ниже НТПР на 5 0С или выше ВТПР на 10 0С; b. ниже НТПР на 10 0С или выше ВТПР на 15 0С; c. температура технологического процесса должна быть равна НТПР.
2. Какая из ниже перечисленных жидкостей наиболее пожароопасна? a. ацетон (НТПР = -18 0С, ВТПР = 6 0С); b. бензин (НТПР = -350С, ВТПР = 17 0С); c. 1,4-дихлорбензол (НТПР = 650С, ВТПР = 950С).
3. Как называется наименьшая температура горючего вещества, при которой в условиях специальных испытаний вещество выделяет горючие пары или газы с такой скоростью, что после их зажигания возникает устойчивое горение?
a. температура взрыва; b. температура вспышки; c. температура самовозгорания; d. температура воспламенения; e. температура кипения.
4. Как изменяется взрывчатость торфяной пыли с увеличением влажности воздуха? a. интенсивность взрыва увеличится; b. интенсивность взрыва уменьшится.
5. Какой из ниже перечисленных факторов не влияет на взрывчатость аэровзвесей? a. мощность источника зажигания; b. начальная температура пылевоздушной смеси; c. объем помещения; d. дисперсность пыли
6. Какая из указанных ниже пылей более взрывоопасна? a. мучная пыль – НКПР – 30,2 г/м3, b. угольная пыль – НКПР – 114 г/м3; c. эбонитовая пыль – НКПР – 7,6 г/м3.
7. НКПР сенной пыли равен 55,4 г/м3, к какому классу пожароопасности она относится? a. особо взрывоопасные; b. взрывоопасные; c. пожароопасные; d. особо пожароопасные.
8. НКПР молочного порошка равен 80 г/м3, к какому классу пожароопасности относится данная пыль? a. особо взрывоопасные; b. взрывоопасные; c. пожароопасные; d. особо пожароопасные.
9. Укажите наиболее важные свойства пыли, влияющие на ее пожарную опасность. a. дисперсность (измельченность); b. склонность к электризации; c. химическая активность; d. токсичность; e. адсорбционная способность.
Вопросы для самоконтроля 1. Классификация взрывов по типам химических реакций. 2. Классификация взрывов по плотности вещества. 3. Понятие взрывчатого вещества, условная классификация взрывчатых веществ. 4. Особенности горения взрывчатых веществ. 5. Изобразите график распределения давления в детонационной волне. 6. При каком соотношении теплоотвода и тепловыделения может произойти взрыв? 7. Понятие детонации, особенности детонационной волны по сравнению с дефлаграционным режимом горения. 8. Взрыв аэровзвесей твердых и жидких веществ. 9. Энергия и мощность взрыва. Тротиловый эквивалент. 10. Максимальное давление при взрыве, его практическое значение. Опорные термины по теме «Типы взрывов, классификация взрывов»: взрыв, ударная волна, источник инициирования взрыва, взрывчатое вещество, детонация. Для парогазовоздушной смеси 1. Составляем уравнение реакции горения вещества в воздухе. 2. Определяем общее число моль исходной смеси паров горючего вещества с воздухом по формуле:
где
3. Определяем общее число моль продуктов горения по формуле:
4. Рассчитываем максимальное давление взрыва паров вещества при заданных условиях:
где Р0 – давление паровоздушной смеси до взрыва, Па; ТВЗР – температура взрыва, К; Т0 - температура паровоздушной смеси до взрыва, К; Snпг - число моль продуктов горения, моль; Sncм - число моль исходной газовоздушной смеси, моль.
4. Используя данные табл. 3 Приложения 2 находим низшую теплоту сгорания вещества и переводим ее из кДж/моль в кДж/кг, разделив на молярную массу (кг/моль). 5. Рассчитываем тротиловый эквивалент возможного аварийного взрыва при взрыве в технологическом оборудовании по формуле:
где QН - низшая теплота сгорания взрывчатого вещества, Дж/кг; mВВ – масса горючего вещества в смеси, кг; 4520×103 – низшая теплота сгорания тринитротолуола (ТНТ), Дж/кг. 6. Рассчитываем размер безопасной зоны по действию давления ударной волны взрыва по формуле:
Задача. Рассчитать максимальное давление взрыва и безопасное расстояние по действию ударной волны взрыва смеси паров бутана (С4Н10) с воздухом при температуре 10 0С, начальном давлении 0,3 МПа. Температура взрыва 2110 0С. Концентрация исходной смеси стехиометрическая, масса вещества 20 кг. Дано: С4Н10, tо = 10 0С, t взр = 2110 0С, Ро = 0,3 МПа, m = 20 кг Найти: Р взр Решение: 1. Составляем уравнение реакции горения бутана. С4Н10 + 6,5(О2 + 3,76N2) = 4CО2 + 5Н2О + 24,44N2 2. По уравнению реакции горения определяем число моль газов до взрыва.
3. По уравнению реакции горения определяем число моль продуктов горения.
4. Переводим начальную температуру и температуру взрыва и градусов Цельсия в Кельвины: То = 273 + 10 = 283 К Твзр = 273 + 2110 = 2383 К 5. Рассчитываем давление взрыва паров бутана при заданных условиях.
6. Используя данные табл. 3 Приложения 2 находим низшую теплоту сгорания бутана: Qн = 2658,54 кДж/моль Переводим ее в кДж/кг, разделив на молярную массу (58 ∙ 10-3 кг/моль):
7. Рассчитываем тротиловый эквивалент возможного аварийного взрыва при взрыве в технологическом оборудовании:
7. Рассчитываем размер безопасной зоны по действию давления ударной волны взрыва:
Ответ: максимальное давление взрыва паров бутана при заданных условиях составляет 2,6 МПа, безопасное расстояние по действию ударной воздушной волны при взрыве в технологическом оборудовании будет равно 88 метров
Тесты для самоконтроля
1. Быстрое превращение вещества, сопровождающееся выделением энергии и сжатых газов, способных совершать работу, называется...? a. Горение b. Тление c. Взрыв d. Радиация e. Дуплексный f. Случайный 2. Процессы, приводящие к взрыву и не связанные с химическим превращением вещества, относятся к...? a. Химическим взрывам b. Нефтехимическим взрывам c. Квадратным взрывам d. Физическим взрывам e. Кинетическим взрывам f. Тротиловым взрывам 3. Какие взрывы относятся к физическим? a. Взрыв при взаимодействии расплавленной лавы с водой b. Взрыв при взаимодействии расплавленных металлов с водой c. Взрыв сосуда с газом под давлением d. Взрыв в результате разложения пероксида водорода e. Взрыв в результате разложения тринитротолуола f. Взрыв газо-воздушных смесей
4. Какие взрывы относятся к химическим? a. Взрыв при взаимодействии расплавленной лавы с водой b. Взрыв при взаимодействии расплавленных металлов с водой c. Взрыв сосуда с газом под давлением d. Взрыв в результате разложения пероксида водорода e. Взрыв в результате разложения тринитротолуола f. Взрыв газо-воздушных смесей 5. Какие из ниже перечисленных типов реакций лежат в основе химических взрывов? a. Окислительно-восстановительные реакции b.
|
|||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 251; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.140.198.43 (0.445 с.) |
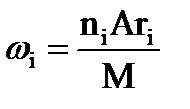 .
.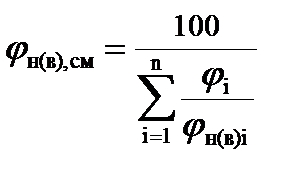 , % (об.)
, % (об.)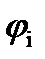 - концентрации горючих компонентов в смеси, об. %;
- концентрации горючих компонентов в смеси, об. %;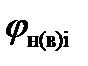 - НКПР или ВКПР каждого компонента в смеси, об. %.
- НКПР или ВКПР каждого компонента в смеси, об. %.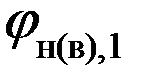 ,
, 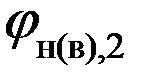 ,
, 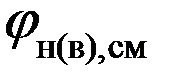 ?
?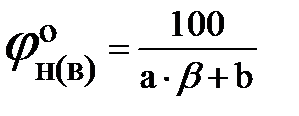 , об. %
, об. %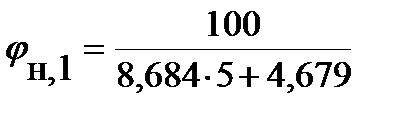 = 2,08 % (об.);
= 2,08 % (об.);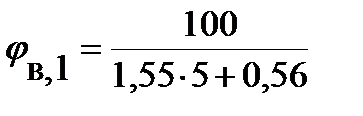 = 12,03 % (об.)
= 12,03 % (об.)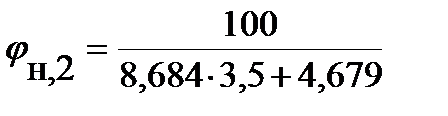 = 2,85 % (об.);
= 2,85 % (об.);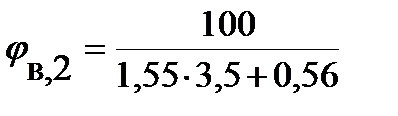 = 16,71 % (об.)
= 16,71 % (об.)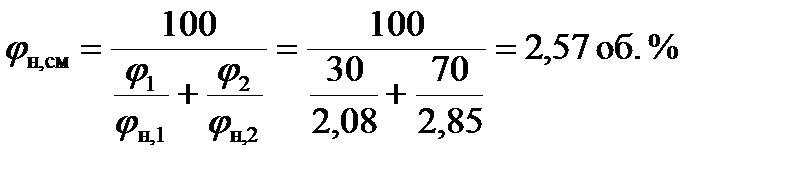
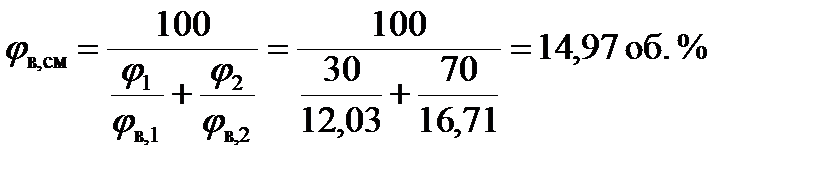
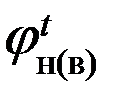 ,
, 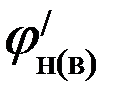 ?
?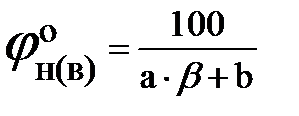 , об. %
, об. %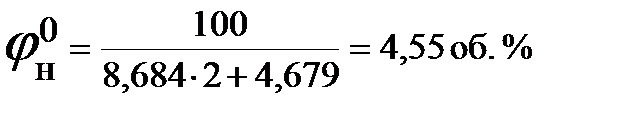
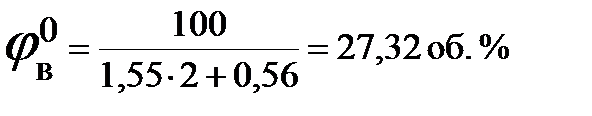
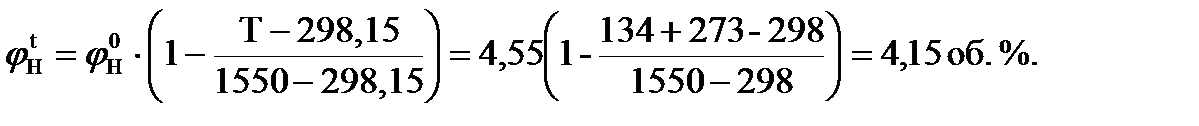

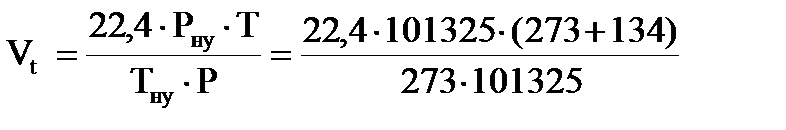 = 33,4 м3/кмоль.
= 33,4 м3/кмоль.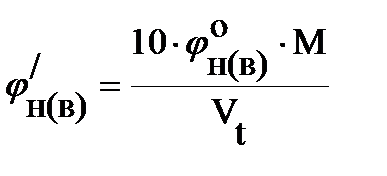 , г/м3
, г/м3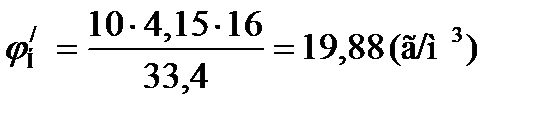
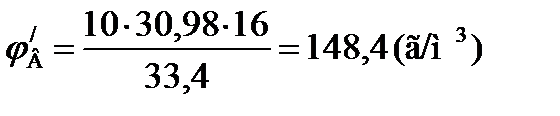
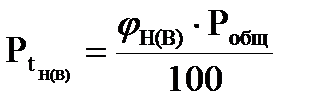
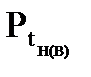 - давление насыщенного пара на нижнем (верхнем) температурном пределе распространения пламени, Па;
- давление насыщенного пара на нижнем (верхнем) температурном пределе распространения пламени, Па;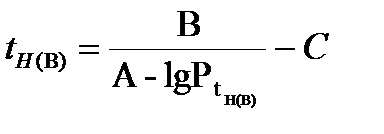 ,
,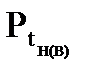 - давление насыщенного пара на нижнем (верхнем) температурном пределе распространения пламени, Па;
- давление насыщенного пара на нижнем (верхнем) температурном пределе распространения пламени, Па;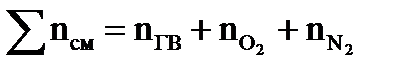 , моль
, моль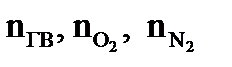 – соответственно число моль исходного (горючего) вещества, кислорода и азота.
– соответственно число моль исходного (горючего) вещества, кислорода и азота.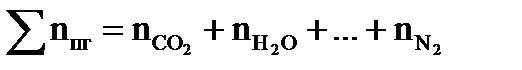 , моль
, моль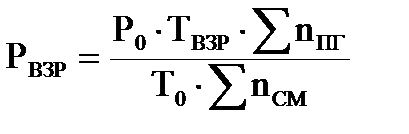
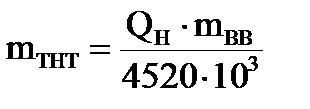
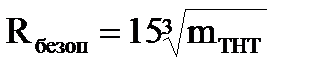 , м.
, м.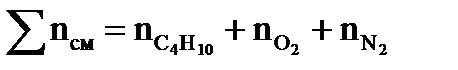 = 1 + 6,5 + 24,44 = 31,94 (моль)
= 1 + 6,5 + 24,44 = 31,94 (моль)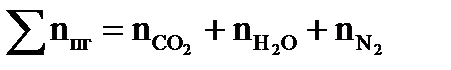 = 4 + 5 + 24.44 = 33,44 (моль)
= 4 + 5 + 24.44 = 33,44 (моль)