
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Идеальная растворимость твердых веществ в жидкости. Уравнение Шредера.
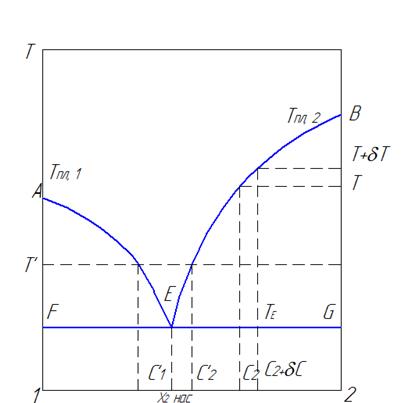
Диаграмма растворимости твердого вещества в жидкости представлена на рисунке (1). Рассмотрим растворение вещества, дающего с растворителем идеальный жидки раствор, а в твердом состоянии эти два компонента не взаимодействуют и не растворяются друг в друге.
Рис. 1. Диаграмма растворимости твердого вещества в жидкости
При изменении температуры на бесконечно малую величину dT, концентрация также изменяется на величину dC. Так как диаграмма строится в изобарных условиях, то химический потенциал будет зависить только от двух переменных С и Т.
Преобразуя слагаемые данного уравнения получим уравнение Шредера в дифференциальном виде:
Интегрирование уравнения Шредера проводится в предположении, что Зависимость растворимости компонента в совершенном растворе от температуры при неопределенном интегрировании выражается уравнением:
Если проводят определенное интегрирование, то уравнение принимает вид:
где xi - молярная доля растворенного вещества в насыщенном растворе (растворимость); Уравнение Шредера для предельно разбавленных растворов имеет вид:
где ∆ T - понижение температуры кристаллизации раствора (расплава) концентрации ИДЕАЛЬНЫЕ РАСТВОРЫ. ЗАКОН РАУЛЯ. Давление насыщенного пара i-го компонента над раствором (Pi) прямо пропорционально его мольной доле в растворе (
где
БЕСКОНЕЧНО РАЗБАВЛЕННЫЕ РАСТВОРЫ. ЗАКОН ГЕНРИ
Растворы, в которых концентрации растворенных веществ бесконечно малы называются предельно разбавленными или бесконечно разбавленными. В предельно разбавленных растворах для растворенного вещества справедлив закон Генри:
парциальное давление пара растворенного вещества прямо пропорционально его мольной доле в растворе. Если пар нельзя считать идеальным газом, то в уравнение закона Генри давление заменяется на летучесть.
ИДЕАЛЬНЫЙ БИНАРНЫЙ РАСТВОР
|
|||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 376; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.223.172.224 (0.004 с.) |
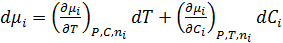 (1)
(1)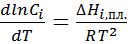 (2)
(2) не зависит от температуры, т.е. является величиной постоянной.
не зависит от температуры, т.е. является величиной постоянной. (3)
(3) , (4)
, (4)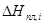 - молярная теплота плавления растворенного вещества;
- молярная теплота плавления растворенного вещества; 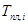 - температура плавления чистого растворенного вещества; Т - температура начала кристаллизации насыщенного раствора концентрации xi.
- температура плавления чистого растворенного вещества; Т - температура начала кристаллизации насыщенного раствора концентрации xi.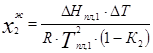 , (5)
, (5) ;
; 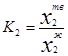 ;
; 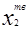 - концентрация растворенного вещества в твердом растворе;
- концентрация растворенного вещества в твердом растворе; 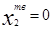 и К2 = 0.
и К2 = 0.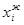 )
)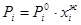 , (1)
, (1)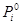 - коэффициент пропорциональности, равный давлению насыщенного пара над чистым i-м компонентом. В соответствии с законом Рауля графическая зависимость Pi =f(
- коэффициент пропорциональности, равный давлению насыщенного пара над чистым i-м компонентом. В соответствии с законом Рауля графическая зависимость Pi =f(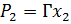 (1)
(1)


