Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Кто может обесцвечивать бромную воду и что это значит. (алкены, алкины, диены, фенол, анилин, стирол почему именно они)
Обесцвечивать бромную воду – это значит взаимодействие с бромом Br2 растворенным в воде при обычных условиях.
Алкены (также стирол) алкины и диены могут реагировать с бромной водой, присоединять бром с разрывом кратных связей, при этом бурая вода обесцвечивается. Также циклопропан и циклобутан может присоединять бром, при этом цикл разрывается, так как они имеют очень слабый цикл.


Анилин и фенол могут обесцвечивать бромную воду, вступают в реакции замещения с бромом, при этом бурая вода обесцвечивается и выпадают белые осадки.
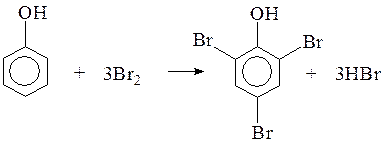
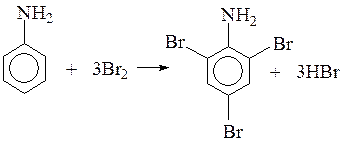
34. Правило Зайцева и Марковникова. (хим св-ва алкенов) Правило Марковникова: в реакциях гидрогалогенирования и гидратации водород присоединяется всегда к более гидрированному атому углерода при двойной связи(к атому углерода с большим числом атомов водорода).
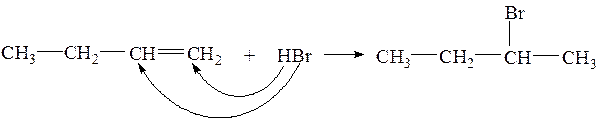
Правило Зайцева: в реакциях дегидратации и дегидрогалогенирования водород отщепляется от наименее гидрированного атома углерода по соседству с функциональной группой (-ОН или – Cl, к примеру) H2SO4(к), t > 1400 C
35. Гидратация алкенов и алкинов, в чем различие (реакция Кучерова)?
Гидратация алкенов протекает при температуре выше 1400 С в присутствии концентрированной серной кислоты H2SO4(к) согласно правилу Марковникова, при этом образуются спирты:

Гидратация алкинов протекает при нагревании в присутствии концентрированной серной кислоты H2SO4(к) и ионов ртути Hg2+ по правилу Марковникова. При гидратации алкинов образуются альдегиды и кетоны. Рассмотрим гидратацию этина (ацетилена):

При гидратации других алкинов образуются кетоны:

36. Окисление алкенов водным и подкисленным раствором KMnO 4. Жёсткое окисление Жёсткое окисление протекает при действии на алкены сильными окислителями, такими как бихромат калия K2Cr2O7 или перманганат калия KMnO4 в кислой среде. При этом происходит полный разрыв двойной связи с образованием карбоновых кислот, хотя при окислении этилена не происходит полного разрыва двойной связи. Как отмечалось раннее, реакции окисления часто записывают схематично:

+7 +2 СН3–СН=CH–CH3 + KMnO4 + HCl = 2CH3COOH + KCl + MnCl2 + H2O Окисление водным раствором перманганата калия KMnO 4 При окислении алкенов водным раствором KMnO4 образуются двухатомные спирты, при этом происходит обесцвечивание малинового раствора. Сначала запишем реакцию схематично:

+7 +4 СН2=СН2 + KMnO4 + H2O = HO–CH2–CH2–OH + MnO2 + KOH
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 169; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.96.146 (0.007 с.) |