
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гидроксиды металлов II группы главной подгруппы ⇐ ПредыдущаяСтр 3 из 3
Гидроксид бериллия – амфотерный гидроксид, практически нерастворим в воде, но легко растворяется под действием как кислот, так и щелочей: Be(OH)2 + 2H2SO4 = BeSO4 + H2O
Be(OH)2 + 2NaOH = Na2[Be(OH)4]
Гидроксид магния – типичное нерастворимое основание (Приложение Б). По образованию белого гидроксида магния, нерастворимого в щелочах, можно отличить соединения магния от соединений других металлов II группы главной подгруппы. Гидроксид кальция – сильное основание, малорастворимое в воде. Это соединение известно с давних времен и находит чрезвычайно широкое применение. Этим объясняется большое количество его тривиальных названий, приведем самые распространенные. Гашеная известь. Издревле известняк обжигали:
CaCO3
а продукт обжига обрабатывали – «гасили» водой:
CaO + H2O = Ca(OH)2
При гидратации выделяется большое количество теплоты, процесс напоминает гашение, поэтому оксид кальция называют негашеной известью, а гидроксид кальция – гашеной. В зависимости от количества воды, можно получить порошок – т.н. пушонку, известковое тесто, которое можно использовать в качестве кладочного раствора и штукатурки; если добавить больше воды, получается белая суспензия – известковое молоко. Если профильтровать известковое молоко, можно получить прозрачную известковую воду – насыщенный раствор гидроксида кальция. Раствор гидроксида кальция быстро мутнеет на воздухе, так как гидроксид кальция, как и другие сильные основания, реагирует с углекислым газом: Ca(OH)2 + CO2 = CaCO3↓ + H2O
Если специально пропускать углекислый газ через известковую воду, то вначале раствор помутнеет из-за образования белого осадка карбоната кальция, но при длительном пропускании газа осадок растворится – образуется кислая соль – гидрокарбонат кальция:
CaCO3¯ + CO2 + H2O = Ca(HCO3)2
При нагревании раствора гидрокарбонат снова разрушается и выпадает осадок карбоната кальция:
Ca(HCO3)2
Последние три реакции часто встречаются в заданиях повышенной сложности. Гидроксиды стронция и бария – сильные основания, Sr(OH)2 относительно малорастворим, Ba(OH)2 хорошо растворим в воде.
Аналитическое определение металлов II группы главной подгруппы
Бериллий и магний, в отличие от остальных металлов II группы, образуют с растворами щелочей нерастворимые гидроксиды, причем гидроксид бериллия растворяется в избытке щелочи (проявляет амфотерность). Соединения щелочноземельных металлов изменяют окраску пламени (рисунок 1).
Кальций и магний очень распространены в земной коре, приведем их важнейшие соединения: CaCO3 – в природе это мел, известняк, мрамор; CaCO3×MgCO3 – доломит; MgCO3 – магнезит; CaSO4×2Н2O – гипс.
Растворимые соли кальция и магния (преимущественно гидрокарбонаты, хлориды, сульфаты) обуславливают жесткость природной воды.
|
|||||
|
Последнее изменение этой страницы: 2021-04-20; просмотров: 67; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.248.149 (0.005 с.) |
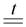 CaO + CO2↑
CaO + CO2↑ CaCO3↓ + CO2↑ + H2O
CaCO3↓ + CO2↑ + H2O


