Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Добування та дослідження властивостей етилену
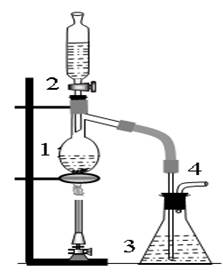
а) Добування етилену. Зібрати прилад, вказаний на рис. 2. В круглодонну колбу 1 помістити кілька шматочків пемзи або подрібненого фарфоруі з ділильної лійки 2 налити в колбу 20÷30 мл (не більше 1/3 її об’єму) заздалегідь приготованої суміші етилового спирту з концентрованою сульфатною кислотою в об’ємному відношенні С2Н5ОН: H2SO4 = 1: 3. Обережно нагрівати суміш на газовому пальнику до початку кипіння і пробуль-кування газу через 10%-ний розчин NaOH в конічній колбі 3. При цьому за рівнянням
утворюється етилен. Пропускання через розчин лугу необхідне для очищення етилену від продуктів побічної реакції окиснення спирту концентрованою H2SO4. Рис.2. Прилад для добування етилену
б) Властивості етилену. До трубки 4 під’єднати газовідвідну трубку і, продовжуючи нагрівання, вносити її кінець в заздалегідь приготовані пробірки з 0,5%-ним розчином KMnO4 та бромною водою. Після цього піднести до трубки 4 запалений сірник і спостерігати горіння етилену. Записати та пояснити спостереження, написати рівняння всіх реакцій, зробити висновки про властивості етилену.
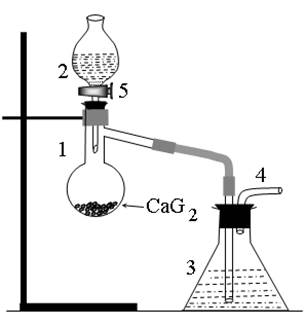
Добування та дослідження властивостей ацетилену Зібрати прилад, вказаний на рис. 2.3. В колбу 1 внести кілька кусочків кальцій карбіду, щільно закрити колбу пробкою із вставленою в неї крапельною лійкою 2, наполовину заповненою водою. Обережно відкриваючи кран 5, краплями додавати воду в колбу 1, де відбувається бурхлива реакція С ≡ С + Н2О → Н─С ≡ С─Н + Са(ОН)2 \ / Ca
Рис.2.3.
Очищений від домішок ацетилен (після проходження через 10%-ний розчин NaOH в конічній колбі 3) пропускати через 0,5%-ний розчин KMnO4 та бромну воду, як це описано для етилену, а також через розчини диаммінаргентум гідроксиду [Ag(NH3)2]OH та диаммінкупрум гідроксиду [Cu(NH3)2]OH, підпалити газ на виході із трубки 4. Записати спостереження, написати рівняння реакцій, назвати продукти. УВАГА! Сухі ацетиленіди купруму та аргентуму вибухонебезпечні, тому в пробірки, де вони утворилися, додати розведеної хлоридної кислоти для їх розкладу: Ag–С ≡ С–Ag + 2HCl → H–C ≡ C–H + 2Ag.
Лабораторна робота № 3. ДОБУВАННЯ ТА ВЛАСТИВОСТІ АРОМАТИЧНИХ ВУГЛЕВОДНІВ
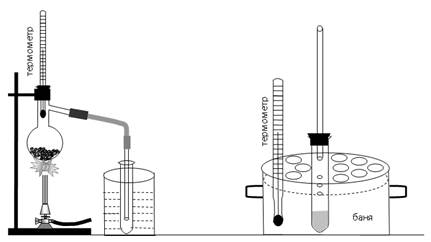
ЕКСПЕРИМЕНТАЛЬНА ЧАСТИНА 1. Добування бензену В фарфоровій ступці старанно розтерти суміш безводних, попередньо прожарених натрій бензоату та натронного вапна в співвідношенні 1:2. 10-15г одержаної суміші помістити в суху колбу Вюрца, щільно закрити колбу пробкою (можна зі вставленим в неї термометром). До бокового відводу колби приєднати трубку і опустити її в заздалегідь приготовану чисту пробірку-приймач, занурену в склянку з холодною водою, як показано на рис. 3.1. При нагріванні колби з сумішшю на газовому пальнику за рівнянням Na–O–H + C6H5 –COONa → C6H6 + Na2CO3, утворюється бензен, про що свідчить поява характерного запаху та конденсація рідини в пробірці-приймачі.
|
|||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 207; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.116.90.141 (0.006 с.) |
||||||||||||