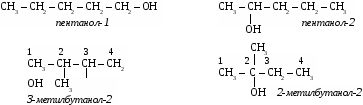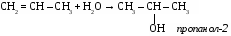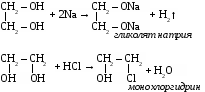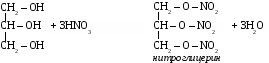Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Предельные одноатомные спирты. ⇐ ПредыдущаяСтр 7 из 7
Этиловый спирт. 1. Строение молекулы.
2. Физические свойства. Жидкость, бесцветная, прозрачная, с характерным запахом, смешивается с водой в любых соотношениях, обладает наркотическим действием. Температура кипения 78,4ºС.
3. Химические свойства. 3.1 горение С2Н5ОН + 3О2 → 2СО2 + 3Н2О 3.2 взаимодействие с металлическим натрием 2С2Н5ОН + 2Na → 2 С2Н5ОNa + 2H2 этилат натрия 3.3 взаимодействие с кислотами С2Н5ОН + HBr → С2Н5Br + H2O бромэтан 3.4дегидратация а) образование этилена
б) образование диэтилового эфира
4. Получение этилового спирта.
С6Н12О6 → 2С2Н5ОН + 2СО2
4.3 получение синтетического этилового спирта С2Н4 + Н2О → С2Н5ОН t = 280º – 300ºC P = 7-8 МПа Катализатор Н3РО4
5. Применение этилового спирта. Для получения бутадиенового каучука, в медицине, в парфюмерии, в лакокрасочной промышленности, в авиации, для приготовления спиртных напитков, для производства уксусной кислоты.
6. Действие этилового спирта на организм. Борьба с алкоголизмом. Гомологический ряд предельных одноатомных спиртов. Одноатомные спирты - органические вещества, молекулы которых содержат одну гидроксильную группу, соединенную с углеводородным радикалом. R - ОН общая формула одноатомных спиртов. Предельные углеводороды Одноатомные спирты СН4 метан СН3ОН метиловый,метанол С2Н6 этан С2Н5ОН этиловый, этанол С3Н8 пропан С3Н7ОН пропиловый, пропанол С4Н10 бутан С4Н9ОН бутиловый, бутанол С5Н12 пентан С5Н11ОН амиловый, пентанол С6Н14 гексан С6Н13ОН гексиловый, гексанол Изомерия и номенклатура спиртов. Дляспиртов возможна два вида изомерии: изомерия положения гидроксильной группы и изомерия углеродного скелета. В соответствии с правилами номенклатуры ИЮПАК выбирают самую длинную цепь атомов углерода и нумеруют ее с того конца, к которому ближе гидроксильная группа. Окончанием -ОЛ и цифрой после названия указывают наличие гидроксильной группы. Упражнение. Составить формулы четырех изомеров пентанола и назвать их.
Химические свойства одноатомных спиртов. 1. взаимодействие с активными металлами 2R–OH + 2Na → 2R–ONa + H2↑ алкоголет натрия 2.взаимодействие с кислотами
R–OH + HCl → R – Cl + H2O галогенпроизводные 3. взаимодействие с другими спиртами R1–OH + НО – R2 R1 – O–R2 + H2O простой эфир Общие способы получения спиртов. 1.гидратация этиленовых углеводородов
2. гидролиз галогенпроизводных СН3Cl + NaOH → CH3OH + NaCl Простые эфиры. Простые эфиры - органические вещества, в молекулах которых два углеводородных радикала соединены через атом кислорода. R1–O–R2 – общая формула простых эфиров Простые эфиры образуются при взаимодействии молекул одного и того же спирта или различных спиртов при нагревании в присутствии серной кислоты. Упражнение. Составьте уравнения реакций получения всех простых эфиров, образовавшихся при нагревании смеси метанола и этанола в присутствии серной кислоты, назовите их.
Задача. При сгорании 3,45 г вещества образовалось 6,6 г СО2 и 4,05 г воды. Плотность паров этого вещества по воздуху равна 1,59. Определить молекулярную формулу вещества.
МНОГОАТОМНЫЕ СПИРТЫ. 1. Отдельные представители. Номенклатура
2. Физические свойства этиленгликоля и глицерина. Этиленгликоль и глицерин бесцветные, прозрачные сиропообразные жидкости. Растворимы в воде, вкус сладкий. Этиленгликоль ядовит.
3. Химические свойства. Многоатомными спиртам называют производные предельных углеводородов, в молекулах которых содержатся две или более гидроксильные группы. Свойства многоатомных спиртов сходны со свойствами одноатомных. В реакцию может вступать одна или несколько гидроксильных групп. Многоатомные спирты реагируют с щелочными металлами с выделением водорода, вступают в реакции замещения с галогеноводородами.
Многоатомные спирты могут образовывать сложные эфиры по всем гидроксильным группам.
|
|||||
|
Последнее изменение этой страницы: 2021-02-07; просмотров: 124; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.192.3 (0.008 с.) |