Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Болезнь Паркинсона. Этиология, патоморфология, патогенез, клиника, диагностика, лечение.
Боле́знь Паркинсо́на (синонимы: идиопатический синдром паркинсонизма, дрожательный паралич) — медленно прогрессирующее хроническое неврологическое заболевание, характерное для лиц старшей возрастной группы[1]. Относится к дегенеративным заболеваниям экстрапирамидной моторной системы.
Этиология Этиологическими факторами риска считаются старение, генетическая предрасположенность, воздействие факторов окружающей среды
Патоморфология Нормальное старение сопровождается уменьшением числа нейронов чёрной субстанции и наличием в них телец Леви. Старению также сопутствуют нейрохимические изменения в стриатуме — снижение содержания дофамина и фермента тирозингидроксилазы, а также уменьшение числа дофаминовых рецепторов. С помощью позитронно-эмиссионной томографии доказано, что темпы дегенерации нейронов чёрной субстанции при болезни Паркинсона намного выше, чем при нормальном старении[2].
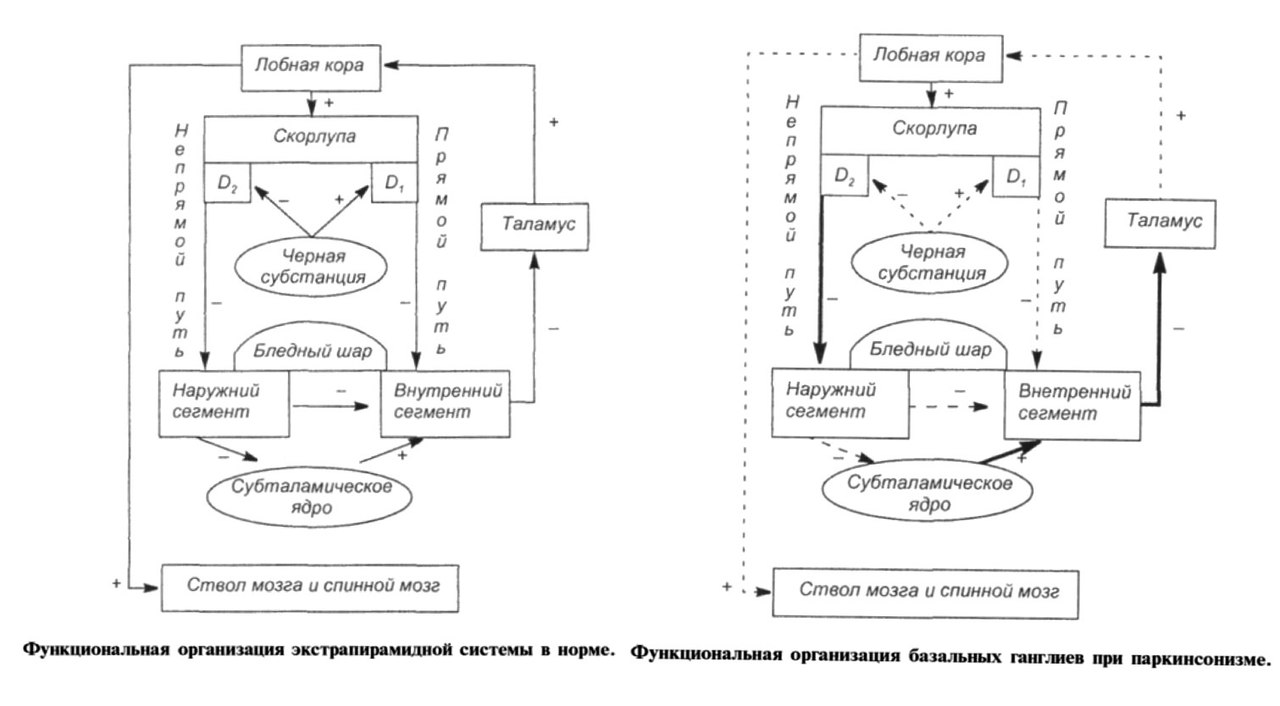
Патогенез Характер клинических проявлений болезни зависит от того, какая часть стриопаллидарной системы поражена — стриатум или паллидум. Если чрезмерно тормозящее влияние стриатума, возникает гипокинезия — бедность движений, амимия. Гипофункция стриатума приводит к возникновению избыточных непроизвольных движений — гиперкинезов[30]. Паллидум оказывает тормозящее воздействие на структуры стриатума. Для болезни Паркинсона характерно снижение тормозящего влияния паллидума на стриатум. Повреждение паллидума приводит к «торможению торможения» периферических двигательных нейронов[31]. В мозге существует несколько дофаминергических систем. Одна из них начинается в нейронах чёрной субстанции,аксоны которых через ножку мозга, внутреннюю капсулу, бледный шар доходят до полосатого тела (лат. corpus striatum). Терминальные отделы этих аксонов содержат большое количество дофамина и его производных. Дегенерация данного нигростриарного дофаминергического пути является основным причинным фактором развития болезни Паркинсона. Вторая восходящая дофаминергическая система — мезолимбический путь. Он начинается от клеток интерпедункулярного ядра среднего мозга и заканчивается в гипоталамусе и лобных долях головного мозга. Этот путь принимает участие в контроле настроения, поведении и контролирует начало двигательного акта и движений аффективной реакции (движений, которые сопровождают эмоции)
Клиника Акинезия (гипокинезия) проявляется замедленностью (брадикинезия), малоподвижностью и бедностью произвольных движений (олигокинезия) и представляет собой ведущий симптом паркинсонизма. Акинезия может выявляться при целом ряде произвольных движений: – Стояние. Больной иногда напоминает манекен, поскольку застывает в различных позах. При толчке он падает навзничь (симптом колонны или статуи). – Ходьба. Наиболее трудны первые движения и перемена положения. Больной идет мелкими, медленными шаркающими шажками. В то же время, в силу нарушения антиинерционной функции и равновесия, пациент не может резко остановиться и при этом делает несколько шагов вперед (пропульсия), назад (ретропульсия), в стороны (латеропульсия). Последние нарушения имеют отношение и к постуральной неустойчивости. – Речь становится медленной, тихой, монотонной, «затухающей» (палилалия). Снижается спонтанная речевая активность, ответы односложны и лаконичны. – Мимика становится бедной (гипомимия), отсутствует эмоциональная окраска. При выраженной гипокинезии появляется тоническая фиксация мимической реакции (мимика после того или иного аффекта медленно, с большим запозданием возвращается в исходное состояние). Наблюдается редкое моргание (симптом Мари). – Письмо медленное, буквы мелкие (микрография). Почерк становится небрежным и неразборчивым. – Асинкинезия – отсутствие физиологических синкинезий. – На фоне описанных проявлений акинезии нередко возникают парадоксальные кинезии, чаще в состоянии аффекта: больной может внезапно совершить ряд быстрых сложных движений (например, внезапно побежать за транспортом, танцевать под музыку), но после них снова, с еще большей выраженностью, проявляется акинетико-ригидный синдром. Для выявления ранней гипокинезии применяется ряд тестов: – тест Фурнье – пациенту предлагается максимально быстро совершить серию движений: встать, сесть, наклониться, повернуться и др.; при этом можно выявить признаки ранней стадии гипокинезии;
– тест постукивания большим и указательным пальцами – пациент в максимально возможном темпе и с максимальной амплитудой выполняет постукивания большим и указательным пальцами друг о друга поочередно обеими руками; – тест сжимания-разжимания кисти – пациенту предлагается максимально быстро сжимать и разжимать кисть. Мышечная гипертония (ригидность) характеризуется следующими особенностями: – повышение мышечного тонуса по пластическому типу. Мышечный тонус повышен уже в начальной фазе движения, сохраняется в процессе всего движения, выявляется одновременно в мышцах-флексорах и мышцах-экстензорах (агонистах – антагонистах), нарастает от движения к движению. Подобная мышечная ригидность часто обозначается в литературе как пластический мышечный гипертонус; – повышение мышечного тонуса по типу зубчатого колеса (феномен Негро). Выявляется в виде прерывности и ступенчатости сопротивления мышц на фоне пластического гипертонуса; – характерна поза «просителя» – голова опущена, руки и ноги согнуты в локтевых и коленных суставах; – симптом «воздушной подушки» – после поднятия головы больного от подушки она застывает в этом положении; – положительный симптом Дылева – сила пассивного сопротивления значительно больше силы активных движений; – при выполнении теста маятникообразного качания ног – прекращение качания ног практически сразу же после выполнения теста. В сомнительных случаях пластическое повышение мышечного тонуса может быть спровоцировано следующими пробами: – пластическое повышение мышечного тонуса становится более отчетливым при одновременных активных движениях в другой руке или ноге (прием Нойки – Ганевой – активное поднятие ноги пациента в положении лежа помогает выявить скрытый пластический тонус в руках); – пластическое повышение мышечного тонуса нарастает при его исследовании в руках у пациента, поставленного предварительно в позу Ромберга с закрытыми глазами (симптом Форманна); – пластическое повышение мышечного тонуса становится более выраженным после повторных движений в исследуемой конечности; – нередко используется тест встряхивания за плечи – пациенту предлагают принять вертикальное положение и расслабиться, затем врач кладет ладони на его плечи и совершает быстрые попеременные вращательные полуповороты туловища больного вокруг вертикальной оси. Тест очень чувствителен для оценки степени мышечной гипертонии и гипотонии, он позволяет определить и симметричность мышечно-тонических изменений. Тремор покоя – мелкоразмашистый тремор, преимущественно начинающийся в руках («счет монет», «скатывание пилюль»), усиливается после эмоциональных нагрузок и исчезает во сне, а также при движениях. Постуральные нарушения – невозможность удерживать равновесие при ходьбе (повороты, остановки) и изменении положения тела (езда в транспорте и пр.). Сочетается с изменениями позы тела. ПЯТЬ СТАДИЙ. Наибольшее распространение получила классификация, предложенная в 1967 году Хеном и Яром: · 0 стадия — двигательные проявления отсутствуют · I стадия — односторонние проявления заболевания
· II стадия — двусторонние симптомы без постуральных нарушений · III стадия — умеренная постуральная неустойчивость, но пациент не нуждается в посторонней помощи · IV стадия — значительная утрата двигательной активности, но пациент в состоянии стоять и передвигаться без поддержки · V стадия — в отсутствие посторонней помощи пациент прикован к креслу или постели О: Болезнь Паркинсона. Наиболее частая нозологическая форма паркинсонизма, характеризуется гипокинезией, сочетающейся с постепенным развитием пластической гипертонии (обычно нисходящего типа – мускулатура шеи, верхних, затем нижних конечностей, туловища), тремором покоя с частотой 4–6 колебаний в секунду, а также постуральными нарушениями на развернутых стадиях болезни. Ригидность, начинаясь с мышц шеи и плечевого пояса, нередко сопровождается болью в вышеперечисленных областях, что приводит к ошибочной диагностике остеохондроза шейного отдела позвоночника и плечелопаточного периартрита. Тремор наблюдается у 70–80 % пациентов с болезнью Паркинсона. Особенность тремора при болезни Паркинсона – появление в состоянии покоя конечности и ослабление вплоть до исчезновения при ее движении, что отличает его от постурально-кинетического тремора, характерного для эссенциального тремора. Для идиопатического паркинсонизма характерен стойкий позитивный ответ на терапию препаратами леводопы. Выполнение нагрузочного теста с 200–250 мг леводопы также позволяет определить ответ организма на препараты леводопы и предположить, что у больного, во-первых, имеется поражение нигростриарной системы, а во-вторых, что стриарные нейроны, на которых расположены дофаминовые рецепторы, относительно сохранились. Распространение двигательных нарушений имеет определенную последовательность. Более чем в 90 % случаев наблюдается асимметричный дебют заболевания (стадия гемипаркинсонизма). В дальнейшем болезни свойственно постепенное прогрессирующее течение с вовлечением вначале ипсилатеральной нижней конечности, затем контралатеральной верхней и спустя еще некоторое время – контралатеральной нижней. Обычно двустороннее вовлечение конечностей наблюдается через 1,5–3 года после начала заболевания. Строго односторонняя симптоматика, сохраняющаяся в течение более 3 лет, чаще свидетельствует о другой природе паркинсонизма. На этапе двустороннего вовлечения конечностей в клинической картине болезни Паркинсона появляются отчетливые аксиальные симптомы: гипомимия, нарушения речи (диспросодия), изменения позы, более выраженные нарушения походки. Вскоре (обычно к 4–5 годам после начала болезни) присоединяется четвертый кардинальный симптом паркинсонизма – постуральная неустойчивость. Необходимым условием постановки диагноза является отсутствие в анамнезе возможных этиологических факторов вторичного паркинсонизма (прием нейролептиков, достоверно перенесенный энцефалит, инсульт, повторные или тяжелые черепно-мозговые травмы, интоксикации). На всех стадиях заболевания не наблюдается отчетливой мозжечковой и (или) пирамидной симптоматики, надъядерного паралича взора и окулогирных кризов. При этом для ранних стадий болезни нехарактерны грубые постуральные расстройства, выраженная прогрессирующая вегетативная недостаточность, деменция и психотические нарушения (галлюцинации, параноид, делирий). В начале болезни Паркинсона расстройства речи обычно невыраженные, при этом страдает модуляция речи (речь монотонная, приглушенная) и возможны пульсионные проявления в процессе разговора. Когнитивные нарушения появляются через 5–6 лет после начала заболевания и достигают уровня деменции примерно у 40–50 % больных через 10– 12 лет, на поздних стадиях. Эмоциональные расстройства составляют существенную долю (около 40–60 %) немоторных проявлений болезни. Из них наиболее часто встречаются депрессия, ипохондрия, тревога, апатия. Вегетативные нарушения при болезни Паркинсона довольно характерны. На ранних стадиях они слабо выражены, но по мере прогрессирования заболевания у 70–90 % пациентов наблюдаются никтурия, запоры, импотенция у мужчин, снижение массы тела, дистальный гипергидроз, повышенное выделение кожного сала. На поздних стадиях присоединяются слюнотечение, дисфагия и ортостатическая гипотензия, которая выявляется у 30 % пациентов и может значительно усложнять лечение. Вспомогательными инструментальными методами для уточнения характера вегетативных расстройств могут стать спектральный анализ ритма сердца и исследование вызванных кожных вегетативных потенциалов. При болезни Паркинсона мощность всех спектров снижена. При изучении вызванных кожных вегетативных потенциалов обнаруживается асимметрия амплитуд – уменьшение их на стороне с более выраженным двигательным дефектом. Болезнь Паркинсона дифференцируют от сосудистого, токсического, лекарственного, посттравматического и постэнцефалитического паркинсонизма.
Диагностика Диагностика болезни Паркинсона в большинстве случаев не вызывает затруднений — достаточно наличия у пациента гипокинезии и одного из симптомов: тремора покоя, ригидности, постуральных нарушений в сочетании с положительным эффектом от приёма леводопы[32]. На начальных этапах заболевания, когда проявления заболевания не выражены либо выражены слабо, правильной диагностике может способствовать выявление постуральных рефлексов(рефлексов положения). К ним относится феномен Вестфаля, а также феномен Фуа—Тевенара (либо феномен голени). Данные рефлексы возникают вследствие повышения пластического тонуса мышц. Феномен голени проявляется тем, что максимально согнутая в коленном суставе нога больного, который лежит на животе, опускается медленно и обычно разгибается не полностью[35].
Лечение О: Основу терапии составляют препараты, восстанавливающие уровень дофамина в стриатуме (препараты леводопы – наком, леводопа в сочетании с бенсеразидом – мадопар), и прямые агонисты дофаминовых рецепторов (прамипексол (мирапекс), пирибедил (проноран)). Также используют антагонисты N-метил-D-аспартатных (NMDA-) рецепторов для коррекции дискинезий (амантадин) и коррекции когнитивных нарушений (мемантин). Удлинить время действия разовой дозы препаратов леводопы могут ингибиторы катехол-О-метилтрансферазы (комбинированный препарат, содержащий леводопу, карбидопу и энтакапон) и ингибиторы моноаминоксидазы типа В (селегилин). При развитии деменции и психотических осложнений также применяют ингибиторы холинэстеразы (галантамин, ривастигмин) Наиболее эффективны препараты леводопы, восполняющие дефицит дофамина в головном мозге. Длительный приём этих лекарственных средств, особенно в высоких дозах, часто сопровождается осложнениями. Приём лекарства может вызывать у пациента непроизвольные движения (дискинезии). С такими побочными действиями приходится мириться, чтобы избежать скованности движений. В тяжёлых случаях, чтобы справиться с дискинезиями, прибегают к хирургическим вмешательствам: имплантации электродов в головной мозг. Это единственный случай, когда при болезни Паркинсона приходится прибегать к операции. Препараты других групп (агонисты дофамина, амантадины, ингибиторы КОМТ) обладают меньшей эффективностью, но их приём может отсрочить назначение леводопы, уменьшить осложнения, связанные с её приёмом. Подбор схемы лечения должен проводить врач-невролог, имеющий специальную подготовку и опыт ведения таких больных. Хир. лечение – стереотоксич. операции на подкорков. структурах.
|
|||||||||
|
Последнее изменение этой страницы: 2021-01-08; просмотров: 315; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.183.89 (0.014 с.) |