Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методы ионообменной хроматографии
Проявительный метод является наиболее распространённым методом ИОХ. Ионообменная проявительная хроматограмма аналогична хроматограмме адсорбционного анализа с той лишь разницей, что в этом случае все порции вытекающего из колонки раствора содержат противоион А+. Так, например, если анализ раствора каких-либо электролитов проводился на колонке, содержащей ионит с противоионом Н+, то все порции вытекающего из колонки раствора будут кислыми, а вымывание должно проводиться раствором кислоты. Вытеснительный метод в ИОХ применяется шире, чем в адсорбционной. Метод разделения смесей ионов на ионитах с применением комплексообразователей имеет очень широкие возможности. Следует только либо правильно выбрать соответствующий комплексообразователь для получения комплексов до хроматографирования и затем проводить хроматографическое разделение полученных комплексов, либо подобрать такой ионит, который обладал бы свойствами комплексообразователя и на нём проводить разделение смеси ионов. Успех разделения, как в том, так и в другом случае зависит от правильного выбора ионита и реагента. В качестве комплексообразователей наиболее часто наряду с галогенидами, сравнительно легко образующими комплексные соединения с ионами многих металлов, применяют лимонную, винную и молочную кислоты, аммиак, глицерин и т.д.
Иониты Свойствами ионитов обладает довольно большое число различных природных и синтетических соединений. Минеральные иониты. Природные минеральные иониты являются, как правило, кристаллическими силикатами, жёсткая решетка которых несёт избыточный заряд. Наиболее важными представителями этой группы ионитов являются целлиты, способные к обмену катионами. К ним относятся минералы анальцим, шабазит, гармотом, гейландит, натролит и некоторые другие. Синтетические неорганические иониты. К этому типу ионитов относятся плавленные и гелеобразные пермутиты, активированный оксид алюминия /алюминатный оксид алюминия/, иониты на основах циркония и титана. Пермутиты представляют собой гидратированные алюмосиликаты и являются катионитами. Иониты на основе углей. Сульфирование бурых, каменных углей и антрацитов дымящейся серной кислотой позволяет вводить в угли подвижные сульфогруппы, а также, после окисления, карбоксильные группы и превращать угли в ионообменники. Сульфирование способствует протеканию реакций поликонденсации и превращает уголь в гель. Благодаря этому иониты на основе сульфированных углей (сульфоуглей) приближаются по свойствам к синтетическим органическим ионитам. Для окисленных углей характерна высокая селективность.
Иониты на основе синтетических полимерных веществ - смол. Наибольшее практическое применение нашли синтетические органические иониты, получаемые на основе полимерных веществ – синтетических смол, что обусловлено прежде всего их большой химической стойкостью, механической прочностью, высокой обменной емкостью, а также большим разнообразием свойств, в частности, высокой селективностью. Различают четыре типа ионитов как для катионитов, так и для анионитов. 1 тип - иониты, проявляющие свойства сильных кислот или сильных оснований. Для катионитов этого типа характерна высокая степень диссоциации и связанная с этим легкость обмена протонов на катионы из раствора электролита. Обменная ёмкость этих катионитов практически не зависит от pH раствора. 2 тип - иониты, проявляющие свойства слабых кислот или слабых оснований. Для катионитов этого типа характерно, что при малых значениях pH раствора большинство катионов не вытесняет из них ионов водорода, т.е. их обменная ёмкость близка к нулю. При возрастании pH раствора и достижения некоторого его значения обменная ёмкость резко возрастает и затем достигает предельного значения. Значение pH раствора, при котором начинается резкое возрастание обменной ёмкости, зависит от концентрации катионов в растворе и природы катионита. 3 тип - иониты смешанного типа, проявляющие свойства смеси сильной и слабой кислот или, соответственно, оснований. Иониты этого типа обладают двумя предельными значениями обменной ёмкости в зависимости от pH или рОН раствора. Для катионитов первая величина предельной обменной ёмкости связана с присутствием в них сильнокислотных групп, а вторая обусловлена наличием слабокислотных остатков.
4 тип - иониты, обменная ёмкость которых с ростом pH или рОН раствора непрерывно возрастает. Иониты, относящиеся к этому типу, ведут себя подобно смеси нескольких кислот или оснований различной силы. Зависимость обменной ёмкости от pH или рОН раствора для ионита 4 группы близка к линейной. Для этого типа ионитов часто оказывается невозможным найти предельное значение обменной ёмкости. Примером ионитов 4 группы могут служить почвы, глины, некоторые минералы. Чтобы установить, к какому типу принадлежит тот или иной ионит, по экспериментальным данным строят график зависимости обменной ёмкости от pH (для катионитов) или рОН (для анионитов) раствора. Для получения такой зависимости прибегают к методу титрования и строят две кривые титрования какого-либо вещества, вступающего в обменную реакцию с ионами испытуемого ионита. Целлюлозоиониты. Так называются ионообменники, получаемые на основе производных целлюлозы, содержащих ионогенные группы и способных к ограниченному набуханию. Существенным отличием целлюлозоионитов от ионообменных смол является то, что ионный обмен в них протекает не внутри гранулы, как это имеет место у ионообменных смол, а на поверхности тончайших волокон. Из целлюлозоионитов наиболее часто применяют катиониты СЭ (сульфоэтилцеллюлоза), СМ (сульфометилцеллюлоза), Р(фосфориллированная целлюлоза) и КМ (карбоксиметилцеллюлоза). К анионитам относятся ТЭАЭ (триэтиламиноэтилцеллюлоза), ДЭАЭ (диэтиламиноэтилцеллюло-за), АЭ (аминоэтилцеллюлоза), ЭКТЕОЛА - продукт реакции эпи-хлоргидрина и триэтиламина с целлюлозой и т.д. Особо крупные органическое ионы (например, антибиотиков) не проникают во внутреннюю часть зерен малонабухающих (даже слабосшитых) сорбентов, в результате чего наблюдается состояние "ложного" равновесия. Поэтому для эффективной реализации таких процессов часто рекомендуют использовать так называемой поверхностно-слоистые сорбенты, в которых ионогенные группы расположены тонким слоем вблизи поверхности зерен. Обменная ёмкость ионитов К числу важнейших свойств ионитов относится их обменная ёмкость. Полная обменная ёмкость данного ионита является величиной постоянной и определяется, в первую очередь, числом фиксированных ионов в каркасе ионита. В этой связи, в идеальных условиях полная обменная ёмкость не зависит от состояния ионита и природы противоиона, а лишь от природы самого ионита. В реальных условиях, однако, она зависит от ряда факторов, в частности, от pH раствора. Это усложняет однозначное определение понятия обменной ёмкости. Кроме того, обменная ёмкость, определяемая в статистических условиях, отличается от величины, полученной в динамических условиях. Поэтому при определении обменной ёмкости необходимо указывать условия, при которых она определена. Различают два типа динамической обменной ёмкости: динамическую обменную ёмкость до проскока (ДОЕ), и полную динамическую обменную ёмкость (ПДОЕ). ДОЕ представляет собой ёмкость ионита, определяемую по появлению данного иона в вытекающем из колонки растворе. ПДОЕ определяется по полному насыщению ионита в колонке данным ионом.
Аппаратура и подготовка ионита Ионообменный хроматографический анализ может осуществляться в двух вариантах: колоночном и тонкослойном.
Важным условием успешного решения практических задач методом ИОХ является правильный выбор ионита, его подготовка, а также определение условий проведения опыта, особенно размеров колонны. Поэтому хроматографическому анализу должна предшествовать подготовка ионита, его испытание обменной ёмкости и других свойств, а также установление на их основе оптимальных размеров зёрен ионита и хроматографической колонки (её длины и диаметра). Соотношение диаметра колонки и размеров зёрен ионита не должно быть менее чем 40:1. В ИОХ применяют аппаратуру, аналогичную применяемой в жидкостной хроматографии. Большое значение имеет чистота применяемой при хроматографии воды, особенно при определении обменной ёмкости. Присутствие посторонних ионов может нарушить обмен и исказить его результаты. В особо точных измерениях следует применять бидистиллят, хранящийся в кварцевой или полиэтиленовой посуде. Важной стадией работы с ионитами является их подготовка к эксперименту и регенерация после отработки. Товарные иониты часто содержат различные примеси, особенно ионы железа. Поэтому иониты следует предварительно очищать. Кроме того, ионит должен быть доведен до набухания. Процесс обмена ионов включает пять последовательных стадий: перемещение сорбируемого иона к поверхности зерна сорбента (1) и внутри него (2), собственно ионный обмен (3), перемещение вытесняемого иона внутри зерна сорбента (4) и от его поверхности в растворе (5). Все стадии, кроме собственно химический реакции обмена, носят диффузионный характер. Уменьшение пути диффузии в результате уменьшения размера зёрен (соответственно и межзернового пространства) приводит к резкому увеличению скорости ионного обмена. Вследствие малой энергии активации диффузии скорость ионного обмена мало зависит от температуры. Большинство ионообменных процессов проводится в динамических условиях - пропусканием раствора через неподвижный слой сорбента в периодической процессах или противоточным движением раствора и сорбента в непрерывных процессах. На рис. 2 приведён типичный прибор для колоночной хроматографии. Преимущества динамического способа - глубокая очистка раствора от примесей (благодаря контакту со свежими порциями сорбента) и полное использование обменной ёмкости слоя (вследствие увода током раствора продуктов ионообменной реакции из сферы реакции).
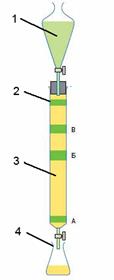
Рис. 2. Типичный прибор для колоночной хроматографии: 1 – капельная (делительная) воронка; 2 – хроматографическая колонка; 3 – сорбент; 4 – колба (сборник элюента). Перед проведением колоночной хроматографии необходимо подобрать элюент и сорбент при помощи ТСХ. Для эффективной очистки выделяемого компонента смеси примеси должны отличаться по Rf не менее чем на 0,15. Элюент для колоночной хроматографии должен быть менее полярным чем для ТСХ анализа. Для эффективного разделения смеси нескольких веществ можно использовать градиентное элюирование, т.е. начинать элюировать неполярными растворителями (пентан, гексан), далее постепенно увеличивать полярность смеси (смеси: гексан/этилацетат от 20:1 до 1:5) и, наконец, переходить к высоко полярным растворителям и смесям (метанол, смеси метанол/триэтиламин 20:1). Способы заполнения колонки сорбентом: 1. Сухой способ. Колонка заполняется сорбентом. После чего сразу наносят вещество и приступают к элюированию. Минус этого способа - частое растрескивание слоя сорбента - из-за чего плохое разделение. Данный способ подходит для флеш-хроматографии, т.е. отделения целевого вещества от примесей с Rf ~0. 2. Элюент затем сорбент. Колонку заполняют до половины длины элюентом, затем порциями засыпают сорбент, следя, чтобы он полностью смачивался. Минус этого способа - если сорбент достаточно мелкий, он слипается комками и падает на дно колонки в виде шариков. Способ часто применяют при работе с крупнозернистым силикагелем. 3. Сорбент в виде суспензии в элюенте. В колонку засыпают необходимое количество сухого сорбента, высыпают его из колонки в химический стакан. Заливают сорбент элюентом и перемешивают для равномерного смачивания. Через некоторое время суспензию взбалтывают и выливают при помощи химической воронки на колонку. Остатки сорбента смывают со стенок химического стакана элюентом. Способы нанесения вещества на колонку: 1. Сухой способ. Вещества наносятся в индивидуальном виде - твердом (просто насыпают на колонку) или жидком (переносят пипеткой на колонку). 2. В растворе. Вещество растворяют в минимальном количестве элюента или менее полярном растворителе, чем элюент и наносят пипеткой. Важно! Растворитель должен быть менее полярный, чем элюент, иначе вещество вытянется с колонки вместе с этим растворителем. Важно! Чем уже слой раствора с веществом - тем лучше разделение. 3. В виде твердой смеси с сорбентом. Вещество смешивают с сорбентом с добавлением небольшого количества растворителя. Растворитель удаляют на роторном испарителе. Сухой сорбент с веществом насыпают на колонку. Наносить вещество на колонку (жидкое или в растворе) следует по стенкам колонки, чтобы не размывать слой сорбента. Важно! Чем ровнее нанесено вещество, тем лучше его разделение. После нанесения вещества верхний слой сорбента на колонке можно накрыть ваткой или фильтровальной бумагой, чтобы при добавлении элюента не происходило размывание слоя сорбента. Важно! Чем ровнее слой сорбента, тем лучше разделение веществ.
Элюирование под давлением. В принципе, в большинстве случаев элюирование проводят при атмосферном давлении. Так как чем быстрее скорость элюирования - тем хуже разделение. Однако, при использовании мелкозернистых сорбентов без элюирования при избыточном давлении не обойтись из-за крайне низкой скорости процесса. В этих случаях применяют колбы Бунзена, в которые помещают хроматографические колонки и подключают к вакуумному насосу (наиболее подходит при проведении флеш-хроматографии на фильтре Шотта) или нагнетают давление при помощи груши. Важно! При проведении хроматографирования слой сорбента ни в коем случае не должен пересыхать, иначе может произойти его растрескивание, приводящее к снижению разделяющей способности. Вещество должно быть растворимо в применяемом элюенте, иначе произойдет его кристаллизация в колонке, что ухудшает разделение. Собранный элюент анализируют титриметрическими или физико-химическими методами.
|
|||||||||
|
Последнее изменение этой страницы: 2021-01-08; просмотров: 233; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.223.159.195 (0.025 с.) |