Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Нарушения сердечного ритма и проводимости: диагностика и лечение
5.1. Классификация антиаритмических средств и характеристика основных противоаритмических препаратов Классификация антиаритмических средств построена на основе вызываемых ими мембранных электрофизиологических эффектов. Наиболее широкое распространение кардиологов всего мира получила классификация, разработанная E. Vaughan-Williams (1984). Согласно ей противоаритмические препараты сгруппированы в четыре класса. Класс I – «мембранстабилизаторы» или препараты, непосредственно сами блокирующие быстрые натриевые каналы клеточной мембраны, т.е. тормозящие скорость начальной деполяризации клеток с быстрым электрическим ответом. По влиянию на рефрактерность миокардиоцитов после быстрой деполяризации I класс подразделяется на три подкласса (А, В, С): IA подкласс – препараты, удлиняющие рефрактерный период клеток за счет преимущественного угнетения кальциевого тока, IB подкласс – укорачивающие рефрактерный период за счет увеличения калиевого тока из клетки, IС подкласс – мало или не влияющие на рефрактерный период кардиомиоцитов. IA подкласс – хинидин, новокаинамид, дизопирамид, аймалин, проаймалин, цибензолин, применол. IВ подкласс – лидокаин, тримекаин, пиромекаин, токаинид, мексилетин, фенотоин, априндин, пентикаинид. IС подкласс – флекаинид, энкаинид, лоркаинид, индекаинид, этмозин, этацизин, аллапинин, пропафенон, никаинопрол, рекаинам, бронекор. Класс II – b-адреноблокаторы или препараты, ограничивающие нервно-симпатические воздействия на сердце путем угнетения b-адренорецепторов и обладающие антиаритмическим эффектом: пропранолол (анаприлин, индерал, обзидан), тимолол, надолол, метопролол, ацебуталол, эсмолол, флестолол и т.д. Класс III – препараты, блокирующие калиевые каналы и вызывающие равномерное удлинение фаз реполяризации и потенциала действия: амиодарон (кордарон), бретилий, соталол, клофилий, пранолий, бетанидин. Класс IV – препараты, блокирующие медленные кальциевые каналы клеточной мембраны, в том числе тормозящие деполяризацию клеток с медленным электрическим ответом: верапамил, дилтиазем, бепридил, галлопамил, тиапамил. Примечание: препараты IA подкласса тропны на 60-70% к миокарду предсердий и на 30-40% к миокарду желудочков. Поэтому они, соответственно, эффективны как для лечения наджелудочковых, так и желудочковых аритмий; препараты IB подкласса действуют только на миокард желудочков и эффективны для лечения только желудочковых аритмий; средства IC подкласса одинаково действуют на миокард предсердий и желудочков, поэтому они эффективны для лечения как желудочковых, так и наджелудочковых аритмий.
1 Характеристика основных антиаритмических препаратов. . Хинидин бисульфат (кинилентин, хинидин-дурулес). В настоящее время практически повсеместно используется хинидин пролонгированного действия. Форма выпуска таблетки по 200 мг. Биодоступность препарата составляет 90-95%. При приеме внутрь максимальная концентрация в крови достигается через 1-2 ч. Период полувыведения составляет 10-12 ч, метаболизируется в печени (70-80%), в неизмененном виде почками выводится 20% и с желчью – 5%. Основной путь метаболизма – окисление в печени с образованием 4 активных метаболитов, причем, за счет них продолжительность действия этого препарата увеличивается до 12 ч, при этом скорость образования основного метаболита – 3-оксихинидина зависит от активности окислительных ферментов. Терапевтическая концентрация в крови составляет 4-10 мкг/мл (потенциально токсическая – 10 мкг/мл). Показания. Препарат показан для купирования и профилактики мерцательной аритмии, пароксизмальной предсердной тахикардии, для лечения наджелудочковой и желудочковой экстрасистолии. Ускорение биотрансформации хинидина наблюдается при сочетании с рифампицином, дифенином, фенобарбиталом, а замедление – с цимитидином, метилдопой, сердечными гликозидами. Противопоказания. Повышенная чувствительность к хинидину, сердечная недостаточность II-IV функционального класса, выраженная кардиомегалия (когда кардио-торакальный индекс превышает 60-70%), шок и коллапс, тромбоэмболия, тяжелая почечная и печеночная недостаточность, интоксикация сердечными гликозидами, атриовентрикулярная блокада II-III степени, остро возникшие блокады ножек пучка Гиса, комбинация применения хинидина бисульфата с сердечными гликозидами (высокий риск развития аритмогенного эффекта).
Побочные действия и осложнения: у 15-30% пациентов при приеме хинидина в течение первых 1-3 суток наблюдается тошнота, рвота, артериальная гипотония, угнетение функции синусового узла, синоаурикулярная блокада II степени, блокады ножек пучка Гиса, реже встречается ускорение проведения по атриовентрикулярному узлу за счет холинолитического эффекта и возможным появлением трепетания предсердий (при купировании мерцательной аритмии) с проведением 1:1; в 0,5-4% случаев отмечается аритмогенный эффект препарата, наиболее выраженный у больных ИБС, постинфарктным кардиосклерозом – желудочковая экстрасистолия, желудочковая тахикардия, фибрилляция желудочков и асистолия. Поэтому для купирования и профилактики желудочковых аритмий у больных ИБС он противопоказан, а без ИБС – нежелателен. При длительном приеме в 5-10% случаев встречаются лихорадка, лейкопения, гемолитическая анемия и тромбоцитопения, локализованный или генерализованный зуд, дерматит, сосудистая пурпура, васкулиты. Следует отметить, что при резкой отмене препарата возможен «феномен отмены» - желудочковая тахикардия, вплоть до фибрилляции желудочков. В настоящее время в подавляющем числе случаев хинидин бисульфат используется для купирования пароксизмов мерцания предсердий, причем его эффект повышается в сочетании с верапамилом в дозе 120-160 мг. В возрасте до 60 лет первый день назначают 3 таблетки (600 мг), во второй – 5 таблеток (1000 мг), в последующие дни – дозу хинидина бисульфата увеличивают на 200 мг ежеденевно (3 день – 1200 мг, 4 – 1400 мг и т.д.) до купирования аритмии или до достижения максимальной суточной дозы 2000 мг. Следует отметить, что в дни приема хинидина бисульфата целесообразно принимать верапамил в дозе 60-80 мг с интервалом 12 ч., причем чтобы суточная доза этого препарата составляла 120-160 мг. Использование верапамила повышает эффективность хинидина бисульфата и предупреждает отрицательный холинолитический эффект. По нашим данным, среднесуточная доза хинидина бисульфата, необходимая для купирования мерцания предсердий, при его приеме по вышеуказанной схеме, составляет 1200-1600 мг в сутки, причем его концентрации в крови при достижении терапевтического эффекта составляет, согласно полученным нами данным, 7-9 мкг/мл (Олесин А.И. и соавт., 1996). Следует отметить, что после купирования мерцания предсердий поддерживающая доза препарата составляет 400-600 мг в сутки. . Прокаинамид (новокаинамид, пронестил). Форма выпуска: таблетки по 250 мг и ампулы, содержащие 10%-5,0 мл раствора этого препарата. Биодоступость препарата составляет 80-85%. В настоящее время практически повсеместно перорально новокаинамид не используется. Период полувыведения составляет 4-6 ч, метаболизируется в печени (40-50%), в неизмененном виде почками выводится до 50%. Основной путь биотрансформации препарата в печени – ацетилирование с образованием активных метаболитов, причем среди них наиболее эффективный, не уступающий по активности новокаинамиду, является N-ацетилновокаинамид. За счет метаболитов продолжительность действия этого препарата увеличивается до 6-8 ч, причем скорость образования основного метаболита – N-ацетилновокаинамида зависит от ацетилирующего фенотипа, т.е. активности ацетилирующих ферментов печени. Терапевтическая концентрация в крови составляет 4-10 мкг/мл (потенциально токсическая – 10 мкг/мл). При внутривенном введении среднетерапевтическая доза новокаинамида составляет 1,0 г, максимальная – 2,0 г.
Показания. Желудочковая экстрасистолия и желудочковая тахикардия, купирование пароксизмов мерцания предсердий. Замедление метаболизма и выведения новокаинамида наблюдается при сочетании с препаратами, тоже подвергающимися ацетилированию в печени таких, как сульфаниламиды, гидралазин и т.д. Противопоказания. Повышенная чувствительность к новокаинамиду, сердечная недостаточность II-IV функционального класса, шок и коллапс, тяжелая почечная и печеночная недостаточность, интоксикация сердечными гликозидами, атриовентрикулярная блокада II-III степени, остро возникшие блокады ножек пучка Гиса. Побочные действия и осложнения: · в 1,0-1,4% случаев при введении новокаинамида могут наблюдаться опасные для жизни осложнения, такие, как шок, полная атриовентрикулярная блокада, включая синдром Фредерика, желудочковая тахикардия и фибрилляция желудочков, асистолия;· неопасные для жизни осложнения (7-8% случаев) тошнота, рвота, диарея, брадикардия, гипотензия, эозинофилия, агранулоцитоз, уриткардия, а также при длительном приеме (более 1 года) могут развиваться признаки волчаночно-подобного синдрома в результате образования антинуклеарных антител (Метелица В.И., 1987). Следует отметить, что в большинстве случаев артериальная гипотензия (но не шок) обусловлена скоростью введения препарата, т.е. при введении новокаинамида со скоростью более 75-100 мг/мин «запрограммирован» гипотензивный эффект (Олесин А.И. и соавт., 1983, 1988, Недоступ А.В. и соавт., 1986, Егоров Д.Ф., 1998). Поэтому преимущественно на догоспитальном этапе врачи скорой помощи вводят этот препарат с 0,1-0,3 мл 1% раствора мезатона. Однако при одновременном введении этих препаратов могут индуцироваться желудочковые аритмии, в частности, желудочковая экстрасистолия и пробежки (по 3-6 и более комплексов) желудочковой тахикардии, в результате развития ишемии миокарда из-за спазма мелких коронарных артериол вследствие воздействия мезатона. Поэтому целесообразно вводить новокаинамид медленно, в среднем со скоростью, 25-75 мг/мин или в нагрузочной дозе 10-12 мг/кг в течение 30-40 минут без мезатона, но в сочетании с препаратами калия (например, вместе с внутривенным введением 1,0-2,0 г хлорида калия в разведении на 100,0-200,0 мл физиологического раствора), который повышает антиаритмический эффект новокаинамида, в частности, при купировании пароксизмов мерцания предсердий на догоспитальном этапе, до 94% (Олесин А.И. и соавт., 1983, 1988, 1996). Кроме того, при введении более 1,0 г этого препарата (максимальная однократная доза 2,0 г) для профилактики развития возможных осложнений (брадикардия, атриовентрикулярная блокада) показано использование атропина в дозе 0,5-1,0 мг (Олесин А.И. и соавт, 1988, 1996). Для предупреждения возникновения остальных осложнений при использовании новокаинамида нами разработаны прогностически неблагоприятные критерии их развития (см. ниже, раздел лечение пароксизмов мерцания предсердий).
. Дизопирамид (ритмодан, ритмилен, норпейс). Форма выпуска таблетки и капсулы по 100 –200 мг. Препарат обладает хинидиноподобным действием. Биодоступность дизопирамида составляет 70-85%, период полувыведения – 5-6 ч, терапевтическая концентрация в крови (3-8 мкг/мл) после приема препарата достигается через 0,5-3 ч и сохраняется в течение 4-5 ч. С почками выводятся 50-60% препарата в неизмененном виде, а также его метаболиты, обладающие слабой антиаритмической активностью (моно-N-деалкилированные метаболиты – 30%, неиндентифицированные метаболиты – 10%). Показания. Желудочковая экстрасистолия, тахикардия, аритмии при синдроме WPW. Ускоряют метаболическую биотрансформацию дизопирамида рифампицин, дифенин, фенобарбитал, а карбамазепин, спиронолактон – уменьшают его концентрацию в крови. Противопоказания. Повышенная чувствительность к дизопирамиду, сердечная недостаточность II-IV функционального класса, тяжелая почечная и печеночная недостаточность, выраженная кардиомегалия (когда кардиоторакальный индекс і 60%), атриовентрикулярная блокада II-III степени, артериальная гипотония, глаукома, аденома предстательной железы, синдром слабости синусового узла, синоаурикулярная блокада II степени, интоксикация сердечными гликозидами. Побочные действия и осложнения. В 50% случаев наблюдается сухость во рту, тошнота, рвота, задержка мочи, распирающие боли в животе, нарушение зрения, внутрипеченочный холестаз, кожная эритема, фотосенсибилизация, гипотония, парастезии, конечностей, импотенция, а также в 1-6% случаев аритмогенный эффект – желудочковая экстрасистолия, пробежки желудочковой тахикардии, фибрилляция желудочков, прогрессирование атриовентрикулярной блокады II-III степени. Дизопирамид применяется первоначально в нагрузочной дозе 300 мг, а затем по 100-200 мг 4 раза в день. Максимальная суточная доза 800 мг. . Аймалин (гилуритмал). Форма выпуска – таблетки 0,05 и ампулы 2,0 мл 2,5% раствора. Аймалин плохо всасывается при приеме внутрь, поэтому преимущественно вводится внутривенно. Период полувыведения препарата 15 ч, терапевтическая концентрация в крови – 200-300 мкг/мл. Активный метаболит аймалина – проаймалин (таблетки по 20 мг) хорошо всасывается при приеме внутрь, а антиаритмическое действие сходно с аймалином.
Показания. Желудочковая экстрасистолия, желудочковая тахикардия, пароксизмальные аритмии при синдроме WPW. Следует отметить, что при пароксизмах мерцания и трепетания предсердий, аритмиях, обусловленных интоксикацией сердечными гликозидами, препарат малоэффективен. Противопоказания. Повышенная чувствительность к аймалину, слабость синусового узла, сердечная недостаточность II-IV функционального класса, атриовентрикулярная блокада II-III степени, артериальная гипотония, интоксикация сердечными гликозидами. Побочное действие и осложнения. В 15-25% случаев встречаются экстракардиальные побочные эффекты: головная боль, головокружение, тошнота, рвота, внутрипеченочный холестаз, ощущение жара при внутривенном введении; в 10-15% случаев - кардиальные осложнения: синоаурикулярная и атриовентрикулярная блокады, асистолия, фибрилляция желудочков и желудочковая тахикардия, артериальная гипотония. . Этмозин. Форма выпуска – таблетки 0,025 и 0,1, ампулы 2,5% раствора 2,0 мл. Биодоступность этмозина при приеме внутрь составляет 40-70%, период полувыведения - 2-4 ч (в зависимости от окислительного фенотипа пациента), причем, терапевтическое действие, с учетом активных метаболитов, увеличивается до 6-8 ч. Терапевтическая концентрация в крови составляет от 4 до 6 мкг/мл. Биотрансформация этмозина достаточно сложна: она происходит в печени с образованием большого количества активных метаболитов, причем среди них наибольшим антиаритмическим эффектом обладает этацизин. Показания. Желудочковая экстрасистолия, желудочковая тахикардия. Замедляется метаболическая биотрансформация этмозина при одновременном приеме с ингибиторами моноаминооксидазы. Противопоказания. Повышенная чувствительность к этмозину, тяжелые поражения печени, синдром слабости синусового узла, синоаурикулярная блокада II степени, интоксикация сердечными гликозидами, нарушения внутрижелудочковой проводимости. Побочные действия и осложнения. В 10-15% случаев наблюдается сухость во рту, тошнота, рвота, головокружение, нарушение зрения, гипотония, а также в 1-2% случаев аритмогенный эффект – желудочковая экстрасистолия, пробежки желудочковой тахикардии, синоаурикулярная блокада, а при длительном применении - возможен агранулоцитоз. Этмозин применяется внутрь в нагрузочной дозе 300 мг, а затем по 0,15-0,2 – каждые 8 ч. Внутривенно вводят по 50-150 мг раствора (2-6 мл 2,5 раствора). . Этацизин. Форма выпуска – таблетки 0,05 и ампулы 2,5% раствора 2,0 мл. Биодоступность этмозина при приеме внутрь достигает 20-30%, период полувыведения - 2-4 ч (в зависимости от окислительного фенотипа пациента), терапевтическая концентрация в крови составляет от 4 до 6 мкг/мл. Биотрансформация этмозина происходит в печени. Показания. Купирование мерцания предсердий (эффективен сублингвальный прием в дозе 150 мг в первые 3 ч от начала пароксизма этой аритмии), желудочковой экстрасистолии, желудочковой тахикардии при медленном внутривенном введении. В качестве противорецидивной терапии пароксизмов мерцания предсердий этот препарат преимущественно эффективен в сочетании с кордароном, при длительном приеме для профилактики желудочковых аритмий часто (до 40%) наблюдаются осложнения или аритмогенный эффект. Замедляется метаболическая биотрансформация этацизина при одновременном приеме с ингибиторами моноаминооксидазы. Противопоказания. Повышенная чувствительность к этацизину, синдром слабости синусового узла, синоаурикулярная блокада II степени, атриовентрикулярная блокада II-III степени, нарушения внутрижелудочковой проводимости. Побочные действия и осложнения. В 10-15% случаев наблюдается сухость во рту, тошнота, рвота, головокружение, нарушение зрения, гипотония, а также в 1-6% случаев при внутривенном введении аритмогенный эффект – желудочковая экстрасистолия, пробежки желудочковой тахикардии или фибрилляция желудочков, синоаурикулярная блокада. Этацизин применяется внутрь по 50 мг 3 раза в день. Внутривенно вводят по 50-100 мг этого препарата (2-6 мл 2,5% раствора) в разведении на 100 мл физиологического раствора. . Лидокаин (ксилокаин). Форма выпуска ампулы 10%-2,0 мл. Период полувыведения после однократной инъекции лидокаина в дозе 100-120 мг – 1-2 ч, терапевтическая концентрация в крови 2-6 мкг/мл. С почками выводятся 70% введенного препарата в виде метаболитов, 3% - в неизмененном виде, а остальная часть - определяется в системном кровообращении. Показания. Желудочковая экстрасистолия, желудочковая тахикардия. Ускоряют метаболическую биотрансформацию лидокаина изопротеренол, глюкагон, а замедляют - b-адреноблокаторы, цимитидин. Противопоказания. Повышенная чувствительность к лидокаину, сердечная недостаточность II-IV функционального класса, тяжелая почечная недостаточность, атриовентрикулярная блокада II-III степени, артериальная гипотония, синдром слабости синусового узла, синоаурикулярная блокада II степени, сочетание с новокаинамидом, хинидином, синдром WPW (ускоряет проведение по дополнительным пучкам). Побочные действия и осложнения в большинстве случаев развиваются при внутривенном введении лидокаина со скоростью более, чем за 2 минуты (тогда концентрация в крови препарата может превысить 6 мкг/мл): появляется тошнота, рвота, судороги, парастезии, дезориентация, эйфория. Лидокаин вводится внутривенно первоначально в нагрузочной дозе 100-120 мг, а затем - внутривенно капельно со скоростью 1 мг/мин или внутримышечно по 400-600 мг каждые 3 ч. . Мексилетин (мекситил). Форма выпуска – капсулы 0,05 и 0,2, а также ампулы по 250 мг (10 мл). Биодоступность мекситила составляет 80-90%, причем, при пероральном приеме максимальная концентрация в крови достигается через 2 ч, период полувыведения препарата 10-12 ч, терапевтическая концентрация в крови – 0,5-2,5 мкг/мл. 90% препарата метаболизируется в печени путем ароматического и алифатического гидроксилирования с образованием 8 активных метаболитов, которые представляют собой окисленные соединения и спирты. 10% мекситила выводится с почками в неизмененном виде. Показания. Желудочковая экстрасистолия, желудочковая тахикардия. Ускоряют метаболическую биотрансформацию мекситила рифампицин, дифенин, курение табака. Противопоказания. Повышенная чувствительность к мекситилу, слабость синусового узла, сердечная недостаточность II-IV функционального класса, тяжелая почечная и печеночная недостаточность, паркинсонизм, артериальная гипотония. Побочное действие и осложнения. В 65% случаев встречаются побочные токсические эффекты: нистагм, тремор, головная боль, головокружение, тошнота, рвота, судороги, атаксия, артериальная гипотензия, остановка синусового узла, синоаурикулярная блокада, причем, у 20% больных приходится прерывать лечение этим препаратом; в 7-10% случаев наблюдается аритмогенный эффект – асистолия, фибрилляция желудочков и желудочковая тахикардия. Мекситил применяют перорально в виде нагрузочной дозы 0,4-0,6 г, а затем по 0,20-0,25 г через каждые 8 ч. Внутривенно мекситил вводят в течение 5 минут в дозе 2-3 мг/кг (150-250 мг), затем 250 мг в течение 30 минут, в последующем 250 мг в течение 2,5 ч, 0,5 г – 8 ч, поддерживающая доза составляет 0,5-1,0 г в течение 24 ч. . Пропафенон (ритмонорм, проликофен). Форма выпуска – таблетки по 0,05 и 0,15 г, а также ампулы по 75 мг активного препарата (10 мл). Пропафенон хорошо всасывается при приеме внутрь, его биодоступность составляет 50-60%, максимальная концентрация в крови при пероральном приеме достигается через 3 ч. Период полувыведения препарата составляет от 4 до 8-10 ч, терапевтическая концентрация в крови – 0,075-0,34 мкг/мл. 97-99% введенного препарата метаболизируется в печени, а остальная часть - почками в неизмененном виде. Показания. Желудочковая экстрасистолия, желудочковая тахикардия, купирование пароксизмов мерцания предсердий, наджелудочковая тахикардия, обусловленная синдромом WPW. Ускоряют метаболическую биотрансформацию пропафенона рифампицин, дифенин. Противопоказания. Повышенная чувствительность к пропафенону, слабость синусового узла, сердечная недостаточность II-IV функционального класса, тяжелая печеночная недостаточность, печеночный холестаз, атриовентрикулярная блокада II-III степени, обструктивные заболевания легких. Побочное действие и осложнения. В 14-18% случаев встречаются побочные токсические эффекты: головная боль, головокружение, тошнота, рвота, потеря аппетита, артериальная гипотония, остановка синусового узла, синоаурикулярная блокада, расширение комплекса QRS, интервала P-Q, расщепление зубца Р, причем у 10% больных приходится прерывать лечение пропафеноном; в среднем в 6-7% случаев наблюдается аритмогенный эффект – фибрилляция желудочков и желудочковая тахикардия, желудочковая экстрасистолия. Пропафенон применяют перорально 0,2-0,6 г в сутки, средняя поддерживающая доза составляет 0,3-0,4 г в сутки, максимальная суточная доза - 0,8 г в сутки. . Флекаинид (трамбакор). Форма выпуска – таблетки по 0,2 г. Флекаинид хорошо всасывается при приеме внутрь, его биодоступность составляет 95%, максимальная концентрация в крови при пероральном приеме достигается через 2-4 ч. Период полувыведения препарата составляет от 12 до 26 ч (в среднем 19 ч), терапевтическая концентрация в крови – 0,3-1,0 мкг/мл. В среднем 70% препарата метаболизируется в печени (метаболиты неактивны), а остальная часть - почками в неизмененном виде. Показания. Желудочковая экстрасистолия, желудочковая тахикардия, купирование пароксизмов мерцания предсердий, аритмии, обусловленные синдромом WPW. Противопоказания. Повышенная чувствительность к флекаиниду, слабость синусового узла, сердечная недостаточность II-IV функционального класса, тяжелая печеночная недостаточность, атриовентрикулярная блокада II-III степени, артериальная гипотония. Побочное действие и осложнения. В 4-5% случаев встречаются побочные токсические эффекты: головная боль, головокружение, тошнота, рвота, парастезии, артериальная гипотония, нарушение функции синусового узла, синоаурикулярная блокада, расширение комплекса QRS, причем, у 1-2% больных приходится прерывать лечение флекаинидом; в среднем, в 3-9% случаев наблюдается аритмогенный эффект – фибрилляция желудочков и желудочковая тахикардия, желудочковая экстрасистолия (Zipes D. et al., 1988). Флекаинид применяют перорально 0,2-0,6 г в сутки, средняя поддерживающая доза составляет 0,3-0,4 г в сутки, максимальная суточная доза 0,8 г. . Аллапинин. Форма выпуска – таблетки по 0,025 и 0,05. Аллапинин хорошо всасывается при приеме внутрь, его биодоступность составляет 40-50%, максимальная концентрация в крови при пероральном приеме достигается через 1 ч. Период полувыведения препарата составляет от 1 до 1,5 ч, терапевтическая концентрация в крови – 0,08-0,4 мкг/мл. 90% введенного препарата метаболизируется в печени, причем 3 активных метаболита удлиняют терапевтическую эффективность препарата до 6-8 ч, а остальная часть - выводится почками в неизмененном виде. Показания. Желудочковая экстрасистолия, желудочковая тахикардия, предупреждение пароксизмов мерцания предсердий. Противопоказания. Повышенная чувствительность к аллапинину, слабость синусового узла, тяжелая печеночная и почечная недостаточность, атриовентрикулярная блокада II-III степени, внутрижелудочковые блокады. Побочное действие и осложнения. В 20-40% случаев встречаются побочные токсические эффекты: головная боль, головокружение, тошнота, рвота, потеря аппетита, диплопия, атаксия, артериальная гипотония, остановка синусового узла, синоаурикулярная блокада, расширение комплекса QRS, интервала P-Q; в 1-4% случаев наблюдается аритмогенный эффект – желудочковая экстрасистолия и пробежки желудочковой тахикардии (по 3-6 и более комплексов). Аллапинин применяют перорально 0,025 г 3 раза в сутки, затем – по 0,05 г 3-4 раза в день, максимальная суточная доза 0,25 г в сутки. . Амиодарон (кордарон). Форма выпуска – таблетки по 0,2 г и ампулы по 150 мг. Амиодарон всасывается при приеме внутрь в среднем за 6,5 ч, его биодоступность составляет 40-50%, максимальная концентрация в крови при пероральном приеме достигается через 1 ч. Период полувыведения препарата составляет при однократном введении - от 8 до 12 ч, при приеме в течение 7 дней – 14 суток, а в течение 1 месяца (в поддерживающей дозе) – 36 суток. Терапевтическая концентрация в крови – 1,0-2,5 мкг/мл. 98% введенного амиодарона метаболизируется в печени, где от его молекулы отщепляется йод. Препарат выводится желчью, в меньшей степени с мочой. Показания. Желудочковая и наджелудочковая экстрасистолия, желудочковая тахикардия, предупреждение пароксизмов мерцания предсердий, наджелудочковых тахикардий, в том числе, аритмиях, обусловленных синдромом WPW. Угнетают метаболическую биотрансформацию амиодарона сердечные гликозиды, b-адреноблокаторы, антагонисты кальция, дифенин. Противопоказания. Повышенная чувствительность к амиодарону, слабость синусового узла, тяжелая печеночная недостаточность, атриовентрикулярная блокада II-III степени, артериальная гипотония, удлинение интервала Q-T на 20% и более от исходных данных, скорректированное по частоте сердечного ритма, нарушение функции щитовидной железы (гипо- и гипертиреоз), беременность и кормление грудью. Побочное действие и осложнения. В 20-40% случаев встречается интерстициальный пневмонит, нарушение функции щитовидной железы, микроотложения желто-коричневой зернистости в роговице, фотосенсибилизация и фотодерматит (эритема, отек кожных покровов), артериальная гипотония, нарушение функции синусового узла, синоаурикулярная блокада, удлинение интервала Q-T; в 1-5% случаев наблюдается аритмогенный эффект – желудочковая экстрасистолия и пробежки желудочковой тахикардии (по 3-6 и более комплексов). Амиодарон применяют перорально в насыщающей дозе 0,2 г 2-3 раза в сутки (400-600 мг в сутки) в течение 7-10 дней, затем – по 0,2 г 2 раза в день в течение 5-7 дней; поддерживающая доза - 200-400 мг с перерывом 1-2 дня в неделю. . Соталол (соталекс, сотагесал). Форма выпуска – таблетки по 0,08, 0,16 и 0,24 г. Соталол всасывается при приеме внутрь, в среднем, за 0,5-1 ч, его биодоступность составляет практически 100%, максимальная концентрация в крови при пероральном приеме препарата достигает через 2-3 ч, период полуэлиминации при однократном введении - от 7 до 10 ч. Терапевтическая концентрация в крови – 1,8-3,0 мкг/мл. 70% введенного соталола метаболизируется в печени, где образуются активные метаболиты. Оставшаяся часть соталола выводится в неизмененном виде почками. Показания. Желудочковая и наджелудочковая экстрасистолия, желудочковая тахикардия, предупреждение пароксизмов мерцания предсердий, наджелудочковых тахикардий, в том числе аритмий, обусловленных синдромом WPW. Противопоказания. Повышенная чувствительность к соталолу, удлинение интервала Q-T на 20% и более от исходных величин, скорректированное по частоте сердечного ритма, а остальные противопоказания те же, что и для b-адреноблокаторов. Побочное действие и осложнения. В 10-12% случаев встречается синусовая брадикардия, усугубление сердечной недостаточности, удлинение интервала Q-T, гипокалиемия; в 0,1-1% случаев наблюдается аритмогенный эффект – двунаправленная желудочковая тахикардия (Singh B. et al., 1987, Zipes D. et al., 1988). Соталол применяют перорально два раза в день, минимальная доза 40 мг в сутки, среднетерапевтическая – 120-160 мг в сутки (по 60-80 мг два раза в день), максимальная суточная – 480 мг в сутки. b-адреноблокаторы и антагонисты кальция. Характеристика b-адреноблокаторов и антагонистов кальция представлена в главе 1.
5.2. Экстрасистолия
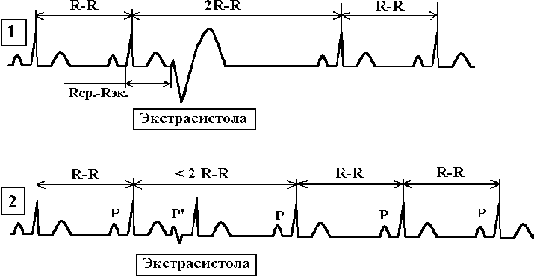
5.2.1. Электрокардиографическая диагностика желудочковой и наджелудочковой экстрасистолии Общим признаком желудочковой и наджелудочковой экстрасистолии является преждевременное сокращение (предэкстрасистолический интервал) с последующей после нее паузой (постэкстрасистолической интервал). Наджелудочковая экстрасистолия наблюдается только на синусовом ритме, в то время как желудочковая – на синусовом ритме (90-95%) и при мерцании или трепетании предсердий (5-10%). r Признаки желудочковой экстрасистолии (см. рис. 5.1.). 1. Комплекс QRS преждевременного сокращения (экстрасистолы) і 0,12 сек.; 2. Зубец Р до и после преждевременного сокращения отсутствует; 3. Сумма интервалов до преждевременного сокращения (предэкстрасистолический интервал) и после него (постэкстрасистолической интервал) равна 2R-R синусового ритма, что обозначается как полная компенсаторная пауза. Желудочковая экстрасистолия без компенсаторной паузы называется вставочной или интерполированной; 4. Зубец Т и сегмент S-T расположен дискордантно к наибольшему комплексу QRS преждевременного сокращения. Следует отметить, что сходную электрокардиографическую картину, как при желудочковой экстрасистолии, может иметь желудочковая парасистолия, которая характеризуется следующими критериями: · Отсутствие устойчивого интервала между синусовыми и следующими за ними парасистолическими комплексами; · Правило общего делителя. Это правило означает, что кратчайший интервал между двумя последовательными парасистолами кратна в сравнении с другими более продолжительными межэктопческими интервалами; · Сливные комплексы. Для парасистолии характерно их «наслаивание» на синусовые комплексы.
r Признаки наджелудочковой экстрасистолии (см. рис. 5.1.). 1. Комплекс QRS преждевременного сокращения (экстрасистолы) Ј 0,11 сек или он такой же, как предшествующий QRS синусового ритма; 2. Сумма интервалов до преждевременного сокращения (предэкстрасистолический интервал) и после него (постэкстрасистолической интервал) < 2 R-R синусового ритма, что обозначается как неполная компенсаторная пауза; 3. Интервал P-Q укорочен в сравнении с соответствующим интервалом синусового ритма; 4. Волна Р положительная (+) или двухфазная (±) перед QRS преждевременного комплекса – предсердная экстрасистолия, волна Р отрицательная (-) перед QRS преждевременного комплекса – экстрасистолия из верхней трети атриовентрикулярного узла, волна Р отсутствует до и после QRS преждевременного комплекса – экстрасистолия из средней трети атриовентрикулярного узла, волна Р отрицательная после QRS преждевременного комплекса – экстрасистолия из нижней части атриовентрикулярного узла (см. рис. 5.2.); 5. Если волна Р перед предсердной экстрасистолой положительная или двухфазная во всех отведениях – это экстрасистола из правого предсердия, а если волна Р перед экстрасистолой отрицательная в I, aVL, V4 -V6 и положительная в III, aVF, V1-V3 отведениях – это экстрасистола из левого предсердия; 6. Если предсердная экстрасистола появляется близко к предшествующему комплексу QRS синусового ритма, то она застает желудочек в состоянии относительной рефрактерности. При этом желудочковый комплекс экстрасистолы может быть уширен и деформирован. Подобная экстрасистолия получила название абберантной, т.е. предсердная экстрасистолия с нарушением внутрижелудочковой проводимости. В тех случаях, когда после зубца Р предсердной экстрасистолы комплекс QRS отсутствует, такая экстрасистолия называется блокированной. Алгоритм для диагностики экстрасистолии представлен на рис. 5.3.
Рис. 5.3. Алгоритм диагностики экстрасистолии
Синусовый ритм Я Преждевременное сокращение с последующей паузой Я Экстрасистола Я QRS преждевременного сокращения Я ____________________________________________________ Ї Ї Ј0,11 сек і 0,12 сек Я Ї ___________________________________________ Волна Р Ї Ї Ї Ї отсутствует Волна Р Волна Р (-) Волна Р Волна Р Ї (+) или (±) перед отсутствует после QRS Желудочковая перед QRS QRS до и после (между QRS экстрасистолия* QRS и волной Т) Ї Ї Ї Ї ПЭ НЭ из верхней НЭ из средней НЭ из нижней части АВ узла части АВ узла части АВ узла
Примечание: * - желудочковая экстрасистолия может быть на синусовом ритме, а также при мерцании и трепетании предсердий; ПЭ – предсердная экстрасистолия, НЭ – наджелудочковая экстрасистолия, АВ – атриовентрикулярный узел.
|
|||||||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 75; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.84.106 (0.092 с.) |