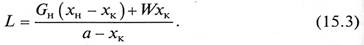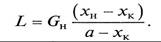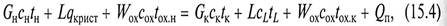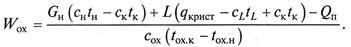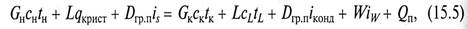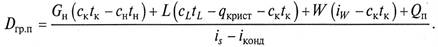Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Стадии процесса. Технические способы получения кристаллов заданного размера. Устройство кристаллизаторов.
КРИСТАЛЛИЗАЦИЯ Кристаллизация – массообменный процесс перехода вещества из раствора (или расплава) в твердую фазу. Особенностью процесса кристаллизации является возможность получения распределяемого компонента в чистом виде, связанная с различной растворимостью выделяемого вещества и примесей, которые остаются в растворе. Кристаллизация сопровождается явлениями полиморфизма, образования кристаллогидратов и изоморфизма. Полиморфизм – явление образования при различных термодинамических условиях одними тем же веществом разных по симметрии и форме кристаллов. Кристаллогидраты – кристаллы, содержащие в структуре химически связанные молекулы воды, причем одно и то же вещество в зависимости от условий кристаллизации и хранения может включать различное число молекул воды. Изоморфизм – явление образования смешанных кристаллов из химически однотипных и сходных по кристаллографическим признакам веществ. Кристаллизация осуществляется вследствие изменения растворимости кристаллизуемого компонента в исходной смеси. Растворы, находящиеся в равновесии с твердой фазой при определенной температуре, называют насыщенными. Вещества, у которых растворимость увеличивается с ростом температуры, называют веществами с положительной растворимостью. Вещества с растворимостью, понижающейся с увеличением температуры, называются веществами с обратной растворимостью. Если концентрация вещества превышает его растворимость, растворы называются пересыщенными и являются нестабильными, легко переходя в состояние насыщения. При этом из них выпадает часть твердой фазы. Растворимость в зависимости от свойств растворенного вещества и растворителя в определенном температурном интервале характеризуется кривой растворимости. На диаграмме состояния (рис. 15.1) растворов нанесены линии растворимости некоторого вещества в зависимости от температуры. Область А называется неустойчивой, или лабильной; область Б – относительно устойчивой, или метастабильной, и область В - область ненасыщенных растворов. Пересыщенные растворы с концентрациями, соответствующими лабильной области, кристаллизуются мгновенно, в метастабильной же области эти растворы какое-то время остаются без изменения.
Границы метастабильной области зависят от температуры раствора, скорости его охлаждения, перемешивания и других факторов. Скорость процесса кристаллизации зависит от температуры раствора, степени его пересыщения, скорости образования зародышей кристаллов, интенсивности перемешивания и других факторов. Зародыши (или центры) кристаллизации образуются из пересыщенных или переохлажденных растворов самопроизвольно. Скорость их образования может быть увеличена повышением температуры, перемешиванием, встряхиванием, присутствием примесей (например, ПАВ*), ультразвуковым воздействием и др. Различают две стадии образования кристалла: возникновение в пересыщенном растворе центра кристаллизации (зародыша); рост кристалла на основе этого зародыша (при условии его термодинамической устойчивости). Размеры получаемых кристаллов зависят в первую очередь от условий кристаллизации и времени осуществления процесса. Кроме

этого, на их гранулометрический состав влияют скорость зародышеобразования, скорость роста кристаллов, дробление частиц в ходе процесса в результате соударения друг с другом столкновения со стенками аппаратуры, агрегации и т. д. Различают кристаллизацию из растворов, наиболее часто используемую в технологических процессах, и кристаллизацию из расплавов. Одновременное получение большого числа кристаллов, частности в производстве минеральных удобрений, называется массовой кристаллизацией. Кристаллизацию из растворов осуществляют изогидрическим способом – изменением температуры (для веществ с прямой растворимостью – понижением температуры; для веществ с обратной растворимостью – повышением температуры) или изотермическим способом – удалением части растворителя испарением или вымораживанием; добавлением в раствор веществ, связывающих растворитель. Кристаллизация из расплава, осуществляемая постепенным его охлаждением с целью получения отливок, монокристаллов, пластинок, гранул и др. Комбинированные способы кристаллизации, к которым относятся вакуум-кристаллизация, кристаллизация с испарением части растворителя в потоке носителя (чаще всего воздуха) и фракционная кристаллизация, используемая для разделения бинарных многокомпонентных расплавов на индивидуальные компоненты или фракции, содержащие определенные компоненты.
Материальный баланс Материальный баланс потоков, участвующих в процессе кристаллизации, записывается в общем виде уравнением
где G н – количество раствора, поступающего на кристаллизацию; G к – количество маточного раствора после кристаллизации; L – число образовавшихся кристаллов; W – количество удаленного растворителя. Баланс кристаллизующегося вещества записывается в виде
где х н, хк — массовые доли растворенного вещества в исходном и маточном растворах; а – массовая доля безводного вещества в кристаллогидрате. Совместное решение уравнений (15.1) и (15.2) позволяет получить уравнение для определения числа образовавшихся кристаллов в процессе изотермической кристаллизации
Для изогидрической кристаллизации (W = 0) уравнение (15.3) упрощается:
Тепловой баланс процесса изогидрической кристаллизации может быть записан в виде
где с н, с к, сL, с ох – теплоемкости исходного и маточного растворов, кристаллов и охлаждающего агента; tн, tк, t L, tox. н, toх. к – температуры исходного и маточного растворов, кристаллов, начальная и конечная охлаждающего агента; W ох – поток охлаждающего агента; qкрист – теплота кристаллизации; Q п – потери теплоты. Уравнения (15.4) и (15.1) позволяют определить расход охлаждающего агента для осуществления процесса изогидрической кристаллизации
Тепловой баланс процесса кристаллизации методом удаления растворителя при нагревании раствора глухим паром может быть записан в виде
где Dгр. п – расход греющего пара; iS, i конд, iW — энтальпии греющего пара, конденсата и удаленного в виде пара растворителя соответственно. По уравнению (15.6) определяют необходимый расход греющего пара
|
||||||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 187; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.128.39 (0.01 с.) |