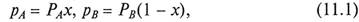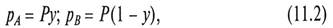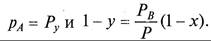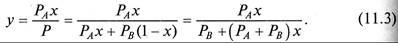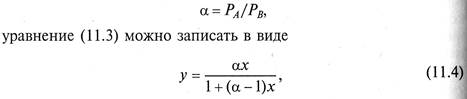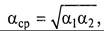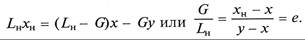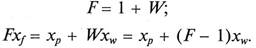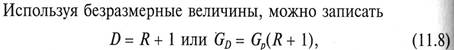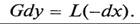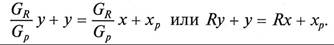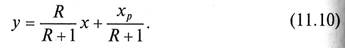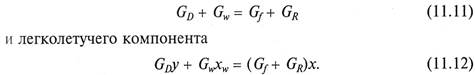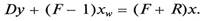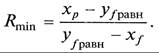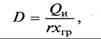Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема 3. 4. Дистилляция и ректификация 10ч. , в Т. Ч. Лаб. Раб. И практ. Занят 6ч.
Студент должен: знать: - физические основы процессов дистилляции и ректификации; - графическое и аналитическое выражение условий равновесия между паром и жидкостью; - принципы составления материального и теплового балансов, уравнение рабочих линий; - схему установок и устройство аппаратов, принципы их расчета; - виды тарелок и насадок, их сравнительную характеристику; - методы образования орошения и парового потока; уметь: - составлять и рассчитывать материальный и тепловой балансы процессов; - определять расходы нагревающих и охлаждающих агентов. Назначение процессов дистилляции и ректификации. Графическое и аналитическое выражение условий равновесия между паром и жидкостью. Простая и фракционная дистилляция. Схемы дистилляционных установок. Материальный баланс простой перегонки, определение среднего состава дистиллятора. Принципы и области применения молекулярной дистилляции. Ректификация. Физические основы и особенности кинетики ректификационных процессов. Схемы установок для непрерывного и периодического процессов ректификации. Графоаналитический расчет непрерывной ректификации. Материальный баланс. Уравнение и построение рабочих линий. Минимальное и рабочее флегмовое число. Тепловой баланс ректификационной установки. Экстрактивная и азеотропная ректификация. ДИСТИЛЛЯЦИЯ И РЕКТИФИКАЦИЯ Дистилляция (перегонка) и ректификация получили широкое распространение во многих отраслях промышленности для разделения однородных жидких смесей с различной температурой кипения образующих их жидкостей. Дистилляцией называется процесс частичного испарения разделяемой смеси жидкостей и последующей конденсации образующихся паров, осуществляемой однократно или многократно. Составы жидкой и паровой фаз, образующихся при этом, заметно различаются, однако с помощью дистилляции нельзя получить компоненты исходного раствора в практически чистом виде. Получение практически чистых компонентов может быть осуществлено с помощью ректификации – разделения однородных жидких смесей, не находящихся в термодинамическом равновесии, на составляющие вещества или группы составляющих веществ в результате противоточного взаимодействия паровой и жидких фаз.
Состав паров в процессах дистилляции и ректификации определяется различной летучестью компонентов при одной и той же температуре. Исходя из этого различают низкокипящие (легколетучие) и высококипящие (труднолетучие) компоненты. Низкокипящий компонент имеет наибольшее давление паров при данной температуре по сравнению с давлением паров любого другого компонента смеси и соответственно наименьшую температуру кипения при одинаковом для всех компонентов давлении. Компонент, обладающий наименьшим давлением или наивысшей температурой кипения, называется высококипящим компонентом. Согласно правилу фаз Гиббса (В. 4), учитывая то, что число компонентов, участвующих в массообменном процессе, равно двум, фаз также две (жидкость и пар), число степеней свободы равно двум. В соответствии с законом Рауля (10.4)
где р A, р B – парциальные давления компонентов А и В; х, (1 - х) –мольные доли компонентов А и В в исходной смеси; Р А, Р B – давления паров чистых компонентов А и В. В то же время, парциальные давления компонентов в системе по закону Дальтона (10.3)
где Р – общее давление в системе; у, (1 - у) – мольные доли компонентов А и В в паровой смеси. Для установившегося равновесия из уравнений (11.1), (11.2)
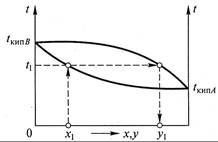
Поскольку процессы в аппаратах осуществляются практически всегда при изобарических условиях (Р= const), равновесную зависимость рассматриваемого процесса можно представить как функции двух переменных (по количеству степеней свободы) t – x, t – у и у – х. При этом графики t – у и t – x можно совместить (рис. 11.1). Нижняя ветвь на диаграмме (см. рис. 11.1) отвечает температурам кипения жидкой смеси, верхняя – температурам конденсации паровой смеси. tкип А и tкип B – температуры кипения чистых компонентов А и В соответственно. Используя диаграмму (см. рис. 11.1), можно по составу жидкой фазы х1 найти равновесный ей состав пара у1 и температуру в системе t1. Для идеальных смесей в соответствии с законами Рауля (11.1 и Дальтона (11.2) можно записать
Введя величину относительной летучести компонента А по от ношению к компоненту В
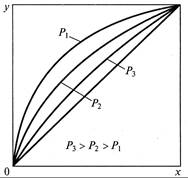
графическая зависимость которого для разных давлений в системе представлена на рис. 11.2.

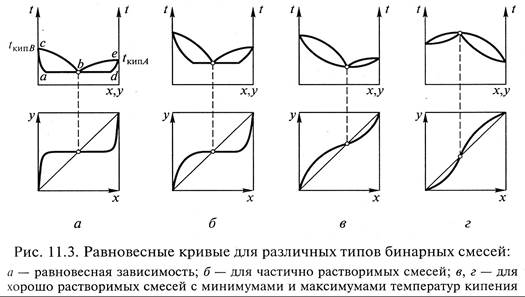
где α1 и α2 – относительные летучести компонентов А и В при tкип А и tкип В . В то же время следует учитывать, что равновесие в рассматриваемой смеси зависит от давления в системе (см. рис. 11.2). Кроме идеальных систем существуют реальные, к которым, например, относятся смеси компонентов А и В, полностью нерастворимых друг в друге. В этом случае силы взаимодействия молекул этих компонентов равны нулю, а каждый из них ведет себя независимо друг от друга. Рассматриваемая смесь закипает при давлении Р = РА + P В. При этом парциальное давление каждого компонента равно давлению насыщенного пара при той же температуре. Температура кипения смеси tcм остается постоянной независимо от состава жидкой смеси (линии abd на рис. 11.3, а). Так как в природе нет абсолютно нерастворимых друг в друге веществ, в интервалах незначительной растворимости одного компонента в другом температура кипения по линиям ас или d е будет
меняться до температуры кипения основного компонента смеси. В областях растворимости будет плавное изменение температур конденсации пара по линиям с b и eb. В точке b будет конденсироваться пар состава уb, причем значение этой величины равно уb = P A /P = const. На основе представленной диаграммы t – х, у можно построить равновесную зависимость в координатах y – x (см. рис. 11.3, а). Если рассмотреть поведение частично растворимых смесей, то для этих систем зона между линиями постоянных температур уже (рис. 11.3, б). Для неидеальных хорошо растворимых смесей характерны зависимости с явно выраженными минимумами (рис. 11.3, в) или максимумами (рис. 11.3, г) температур кипения смеси. На приведенных диаграммах имеются точки пересечения равновесной линии с диагональю, в которых состав пара равен составу жидкости. Это так называемые точки азеотропных составов, в которых системы находятся в термодинамическом равновесии, и разделение их методами дистилляции и ректификации невозможно. Дистилляция Дистилляция в технологических процессах может осуществляться следующими основными способами. Простая дистилляция (простая перегонка) производится путем постепенного испарения исходной смеси. Образующиеся пары конденсируются. Простая дистилляция осуществляется в тех случаях, когда летучести разделяемых компонентов резко различаются, и к получаемым продуктам не предъявляют высоких требований по чистоте. Простая дистилляция может осуществляться периодически и непрерывно, однократно и многократно, с дефлегмацией и фракционированием. Однократное испарение, или равновесная дистилляция, обычно осуществляется в непрерывном режиме. Исходная смесь нагревается в теплообменнике паром, топочными газами или электронагревом. Образовавшаяся парокапельная смесь поступает в сепарационную камеру, откуда пар направляется в конденсатор, где конденсируется и отводится в сборник дистиллята, а жидкость – в сборник кубового остатка.
Так как жидкость достаточно долго взаимодействует с образующимися парами, то можно считать, что между фазами достигается равновесие. Зная начальное количество смеси Lн, поступающей на разделение, а также ее начальную концентрацию хн, из уравнения материального баланса можно рассчитать количество получаемой паровой фазы G:
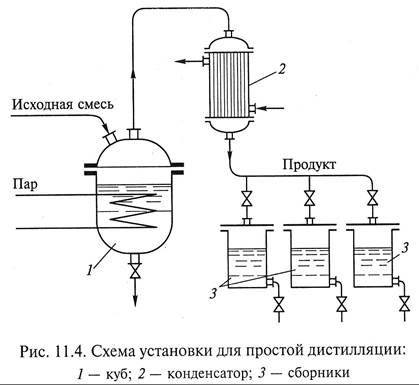
Здесь х и у – текущие концентрации легколетучего компонента в жидкой и паровой фазе, определяемой из условия равновесия либо путем подбора, либо графически; е – доля отгона легколетучего компонента в дистиллят, являющаяся отношением массы образовавшихся паров к массе исходной смеси. При простой дистилляции (однократном испарении) (рис. 11.4), проводимой периодическим способом, смесь загружается в куб 1, обогреваемый через змеевик или рубашку паром или дымовыми газами. После нагрева смеси образующиеся пары конденсируются в конденсате 2, и конденсат направляется в сборники 3. Остаток, обогащенный высококипящим компонентом, удаляется из куба 1 по окончании операции. Простая дистилляция может проводиться при атмосферном давлении или под вакуумом. По мере испарения, содержание легколетучего компонента в дистилляте непрерывно уменьшается, составляя максимальную величину в начале процесса и минимальную - в его конце. Отбор дистиллята различного состава в отдельные сборники позволяет получать несколько фракций разного состава. Такой способ называется фракционной перегонкой.
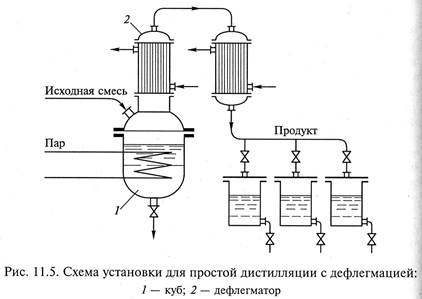
Степень разделения компонентов простой дистилляцией может быть повышена применением дефлегмации (рис. 11.5). По это схеме пары, покидающие куб 1, поступают в дефлегматор 2, в котором они конденсируются не полностью, а частично. При частичной конденсации конденсируется в основном менее летучий компонент, и пары обогащаются низкокипящим компонентом. Конденсат (называемый флегмой) из дефлегматора возвращается в перегонный куб и подвергается многократному испарению. Дистилляцию в токе водяного пара применяют в том случае, 4 когда компоненты исходной смеси нерастворимы в воде, что позволяет снизить температуру кипения смеси и тем самым избе жать разложения компонентов. Дистилляция с водяным паром применяется при переработке жирных кислот, эфирных масел, смол, а также для дезодорации – удаления веществ, обусловливающих неприятный запах масел, жиров и других продуктов. При осуществлении этого процесса исходная смесь загружается в куб, обогреваемый глухим паром через рубашку. Внутрь куба через барботер подают острый пар. Пары, выделившиеся при испарении смеси, направляют в конденсатор-холодильник. Образовавшийся конденсат поступает в сепаратор, где нерастворимые друг в друге жидкости расслаиваются.
Дистилляция с водяным паром протекает в неравновесных условиях. При этом острый пар выполняет две функции – теплоносителя и агента, снижающего температуру кипения. Таким обра зом, при расчете необходимого количества острого пара надо учитывать то, что его расход должен превышать количество, затрачиваемое на процесс отгонки выделенного вещества.
Недостатком метода является наличие влаги в продуктах перегонки. Дистилляция в токе инертного газа проводится с использованием азота, водорода, диоксида углерода. Пар заменяется инертным газом в том случае, когда дистилляции подвергаются компоненты, растворимые в воде. Преимуществом применения инертных газов является также отсутствие нижнего температурного предела проведения процесса, поскольку применяемые газы при этих условиях не конденсируются. Дистилляция в токе инертного газа имеет ряд недостатков: примесь газа в отгоняемом паре резко снижает коэффициент теплоотдачи при конденсации пара из парогазовой смеси, что приводит к увеличению размеров холодильника-конденсатора; при такой конденсации часто образуется туман, отделить который от газа весьма трудно, поэтому возникают потери дистиллята с инертным газом. Молекулярная дистилляция используется в технике для разделения компонентов, кипящих при высоких температурах и не обладающих необходимой термической стойкостью. Процесс проводится под глубоким вакуумом (остаточное давление 0,10... 1,0 Па). При таком разрежении молекулы легко преодолевают силы взаимного притяжения, число столкновений между ними значительно сокращается, а длина свободного пробега резко возрастает.
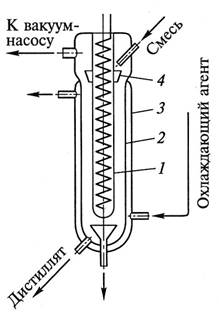
На рис. 11.6 представлена схема простейшего аппарата для молекулярной перегонки. Внутренний цилиндр 1 снабжен спиралью для электронагрева и является испарителем. Внешний цилиндр 2,
являющийся конденсатором, имеет рубашку 3, по которой движется охлаждающий агент. Исходная смесь вводится через патрубок в воронку 4 и стекает пленкой по наружной поверхности испарителя. Остаток и дистиллят, собирающийся на внутренней поверхности конденсатора, удаляются через патрубки в нижней части аппарата. В кольцевом пространстве между испарителем и конденсатором поддерживается требуемый вакуум при помощи насоса глубокого вакуума, присоединенного к верхнему патрубку.
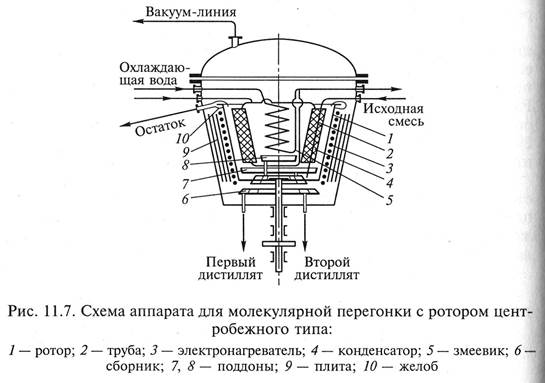
Более эффективным аппаратом для молекулярной перегонки является аппарат, схема которого представлена на рис. 11.7. Исходная смесь, подлежащая разделению, поступает в аппарат через трубу 2 на дно ротора центрифужного типа 1. Под действием центробежной силы поступающая жидкость поднимается по конусу (конусность 10...25°) и подвергается нагреву излучением от электронагревателя 3. Вырвавшиеся из жидкой фазы молекулы стремятся к конденсирующим поверхностям конденсатора 4 и змеевика 5. Первая представляет собой разрозненные секции, соединенные коллекторами для ввода и вывода охлаждающей воды, вторая – змеевик, охлаждаемый водой. Первая конденсирующаяся фракция стекает с элементов конденсатора 4 на поддон 7, а вторая конденсируется на змеевике 5 и стекает на поддон 8. Неиспаренная часть под действием центробежной силы выбрасывается с ротора 1 в отводной желоб 10 и удаляется из аппарата. Из поддона 7 дистиллят удаляется через периферийную секцию кольцево‑
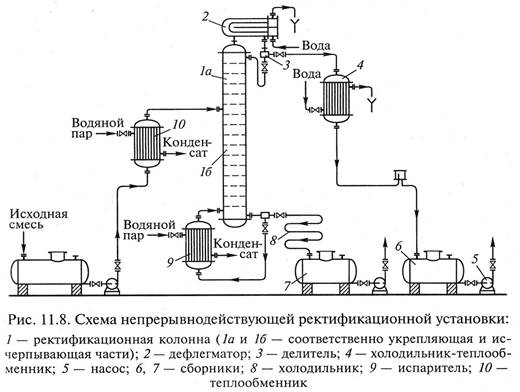
го сборника 6, а из поддона 8 дистиллят отводится по патрубку через центральную секцию кольцевого сборника. Для теплоизоляции установлены концентрические плиты 9. Ректификация Ректификация – способ разделения однородных жидких смесей, состоящий из нескольких компонентов, основанный на противоточном взаимодействии двух неравновесных фаз – жидкости и пара, образующихся из этой смеси. При этом пар при движении постоянно обогащается низкокипящим (легколетучим) компонентом, а жидкость – высококипящим (труднолетучим) компонентом. Процесс ректификации может осуществляться непрерывно и периодически под атмосферными избыточным давлением, а также под вакуумом. Непрерывнодействующая ректификационная установка (рис. 11.8) состоит из ректификационного массообменного аппарата – ректификационной колонны 1, представляющей собой вертикальный цилиндрический корпус, внутри которого расположены контактные устройства (насадка, тарелки). Снизу вверх по колонне движется поток пара, поступающий в ее нижнюю часть из испарителя 9, находящегося рядом или под самой колонной. Поступа‑
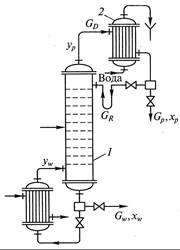
ющий в колонну пар по составу представляет собой практически чистый труднолетучий компонент. На каждой тарелке при его перемещении по колонне происходит конденсация поднимающегося пара, и за счет теплоты его конденсации – испарение находящегося в этой зоне легколетучего компонента. Таким образом, происходят постоянное удаление из выходящего пара труднолетучего компонента и обогащение его легколетучим. В результате из верхней части колонны выгружаются пары практически чистого легколетучего компонента, который конденсируется в дефлегматоре 2. Получаемая жидкость разделяется в делителе 3 на два потока. Первый поток – флегма, возвращается назад в колонну 1, создавая тем самым нисходящий поток жидкости, состоящий практически из чистого легколетучего компонента. Стекая вниз по колонне и взаимодействуя с восходящим паром, флегма постоянно обогащается конденсирующимся из нее труднолетучим компонентом, заменяющим постоянно испаряющийся легколетучий компонент. В результате жидкость, достигающая нижней части колонны и поступающая в испаритель 9, состоит практически из низколетучего компонента. Подаваемую на разделение исходную смесь подогревают до температуры кипения в теплообменнике 10 и подают в колонну, в зону (или на тарелку), положение которой определяют в результате расчета контактного ректификационного аппарата. Зона питания (или тарелка питания) делит колонну на две части. Верхняя, или укрепляющая, часть 1а обеспечивает наибольшее укрепление поднимающихся паров, т. е. обогащение их легколетучим компонентом. Нижняя, или кубовая (исчерпывающая), часть 1б, обеспечивает наибольшее удаление из жидкости легколетучего компонента. Второй поток жидкости, получаемый в дефлегматоре 2 и называемый дистиллятом, поступает в холодильник-теплообменник 4, затем в сборник 6, откуда перекачивается в качестве целевого продукта насосом 5. Жидкость, выходящая из нижней части колонны, также делится на два потока. Первый возвращается в испаритель 9, откуда в виде пара подается назад в колонну, второй, называемый кубовым остатком, после охлаждения в холодильнике 8 направляется сборник 7. Материальный баланс При описании и расчетах процессов, осуществляемых в ректификационных аппаратах при противоточном взаимодействии потоков жидкости и пара (рис. 11.9), принимают следующие допущения. 1. Мольные теплоты испарения компонентов одинаковы, т. е. при конденсации каждого киломоля пара испаряется такое же ко-

личество киломолей жидкости. Отсюда следует важный вывод о том, что количество пара, движущегося в аппарате снизу вверх, выраженное в киломолях, одинаково в любом сечении ректификационной колонны. 2. При конденсации пара в дефлегматоре изменения его состава не происходит, т. е. состав пара, выходящего из верхней части колонны, равен составу получаемого дистиллята и флегмы (ур = хр). 3. При испарении кубовой жидкости в испарителе изменение ее состава также не происходит, т. е. состав жидкости, выгружаемой из нижней части колонны, равен составу возвращаемого в колонну пара (уw = хw). 4/ Теплоты смешения компонентов разделяемой смеси равны нулю. Таким образом, легко видеть, что при расчетах ректификационных аппаратов количество и состав фаз удобно выражать в молярных величинах. Обозначим: G f - количество смеси, поступающей на ректификацию; Gp – количество получаемого дистиллята; Gw – количество получаемого кубового остатка; х f, хр, хw – содержание легколетучего компонента соответственно в исходной смеси, дистилляте и в кубовом остатке. Количественная размерность потоков – кмоли или кг; качественная размерность (состав) – мольные или массовые доли (проценты). Уравнение материального баланса при этом состоит из двух равенств: по входящими выходящим потокам
по легколетучему компоненту в этих же потоках
При описании процесса ректификации часто используют безразмерные отношения Gf / G p = F и G w/ G p = W, показывающие количества исходной смеси и кубовой жидкости, приходящиеся на 1 кг получаемого дистиллята. При использовании безразмерных отношений уравнения (11.5) и (11.6) запишутся в виде
Если количество паров, отбираемых из верхней части колонны 1 и направляемых в дефлегматор 2, составляет G D, а количество флегмы, возвращаемой после него назад в колонну, - GR, то материальный баланс узла дефлегмации запишется как
где D = G D /Gр; R= GR/Gр – флегмовое число. Поскольку легколетучий компонент, по которому обычно ведется расчет, переходит в процессе ректификации из жидкой фазы в паровую, дифференциальное уравнение материального баланса запишется в виде
Рассмотрим материальные балансы для верхней (укрепляющей) и нижней (исчерпывающей) частей ректификационной колонны. В этом случае все количественные расходы будут иметь размерность кмоль/с, а содержание в них компонентов – мольные доли. В верхней части расход пара, постоянный по высоте колонны (см. допущение 1), будет равен расходу флегмы и дистиллята (11.7). Поскольку мольный состав пара и флегмы будет меняться по высоте укрепляющей части, то
Подставим (11.7) в (11.9) и, записав потоки через отношение расходу дистиллята, получим
Выразив концентрацию легколетучего компонента в паре через концентрацию легколетучего компонента в жидкости в верхней части колонны, получим уравнение рабочей линии процесса ректификации в укрепляющей части колонны
В нижней (исчерпывающей) части при составлении уравнения баланса следует учитывать поток исходной смеси и отбор кубовой жидкости (кубового остатка)
Подставив G из уравнения (11.11) в (11.12) и записав потоки через отношение к расходу дистиллята, получим
Учитывая (11.8), получим выражение для рабочей линии процесса ректификации для исчерпывающей части колонны
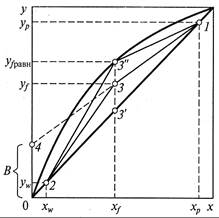
Легко видеть, что рабочие линии процесса ректификации (11.10) и (11.13) при соблюдении допущений 1 – 4 являются прямыми линиями с различными углами наклона. В то же время, положения рабочих линий в у – х-диаграмме зависят не только от состава исходной смеси и продуктов разделения, но также и от тепловых параметров исходной смеси. Теоретически возможны следующие случаи тепловых характеристик исходной смеси, подаваемой в ректификационный аппарат: · при температуре кипения; · при температуре ниже температуры кипения; · в виде смеси насыщенного пара и жидкости; · в виде насыщенного пара; · в виде перегретого пара. Все приведенные варианты могут быть реализованы в промышленности, но наиболее часто на разделение подают исходную смесь при температуре кипения. Для построения рабочих линий процесса ректификации для этого случая на оси абсцисс диаграммы у – х (рис. 11.10) откладывают заданные составы х f, х p, х w. В соответствии со вторым допущением (у p = хр) и третьем допущением (у w = х w) точки 1 и 2, принадлежащие концам рабочих линий для верхней и нижней частей колонны, располагаются на диагонали диаграммы. Точка 3 характеризуется значением х f, принадлежит обеим рабочим линиям и может перемещаться в диапазоне между точками 3' (диагональ диаграммы) и 3" (равновесная линия), в зависимости от значения флегмового числа R. В случае расположения рабочих линий на линии 1 – 3' – 2 они совпадут с диагональю и будут соответствовать уравнению у = х,что может произойти только в случае бесконечно большого флегмового числа (R → ∞). В этих условиях (уравнение (11.8)) ректификационный аппарат работает без отбора дистиллята (G p = 0), что может происходить при испытаниях и запуске установки. Данному случаю соответствует максимальная движущая сила. Второе предельное положение рабочих линий (1 – 3" – 2) характеризуется размещением точки 3" на равновесной линии. В этой точке движущая сила равна нулю, а, следовательно, для проведения процесса в ректификационном аппарате необходима бесконечно большая поверхность контакта фаз, что на практике неосуществимо. С увеличением ординаты точки 3 значение флегмового числа уменьшается и становится минимальным в точке 3". Значение минимального флегмового числа может быть найдено из уравнения (11.10) подстановкой у = у f равн, х = х f, где у f равн – состав пара, находящегося в равновесии с жидкостью, поступающей на ректификацию:
Положение рабочей линии 1 – 3 – 2 соответствует проведению реального процесса ректификации при некотором значении Rmin < R < R∞. В то же время необходимо отметить, что с увеличением флегмового числа увеличивается движущая сила массообменного процесса, но также увеличиваются затраты теплоты на парообразование, и наоборот.
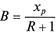 откладывают его на оси ординат, получая точку 4. Пересечение линии, соединяющей точки 1 – 4 и x = xf, определяет положение точки 3. Соединив точки 2 и 3, получают ломаную линию 1 – 3 – 2, отвечающую изменению рабочих концентраций в укрепляющей и исчерпывающей частях колонны. откладывают его на оси ординат, получая точку 4. Пересечение линии, соединяющей точки 1 – 4 и x = xf, определяет положение точки 3. Соединив точки 2 и 3, получают ломаную линию 1 – 3 – 2, отвечающую изменению рабочих концентраций в укрепляющей и исчерпывающей частях колонны.

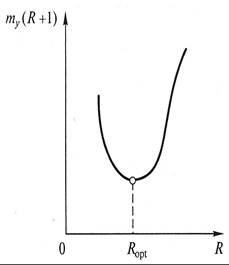
Оптимальное флегмовое число Ropt, для эксплуатации ректификационной установки выбирают чаще всего из условий минимального объема колонны. С этой целью задаются рядом значений Rmin < R < R∞, и на диаграмму у – х наносят соответствующие им рабочие линии процесса. Для каждого процесса методом графического интегрирования получают значения чисел единиц переноса т у, и строится график в координатах т у*(R + 1) - R (рис. 11.11), по минимуму которого определяется значение Ropt. В соответствии с (9.24) т у ≈ Н. По уравнению (11.8) выражение (R+ 1) ≈G D, которое, как любой расход, пропорционально площади сечения аппарата f a. Следовательно, произведение т у*(R+ 1) ~ Н f а ~ Va, где Vа – объем ректификационного аппарата. В ряде случаев оптимальное флегмовое число находится по минимуму приведенных затрат, включающих эксплуатационные расходы и капитальные затраты. Однако, как показывает практика, найденные разными методами оптимальные флегмовые числа отличаются незначительно. Тепловой баланс ректификационной колонны непрерывного действия (см. рис. 11.9) складывается из следующих частей:
где с f, с R, с W – теплоемкости исходной смеси, дистиллята и кубовой жидкости соответственно; t f, tp, t w – температуры исходной смеси, флегмы и кубовой жидкости; i D – энтальпия пара, выходящего из колонны. Из уравнения теплового баланса (11.14) обычно определяется расход греющего (первичного) пара в испарителе, необходимый для проведения ректификации,
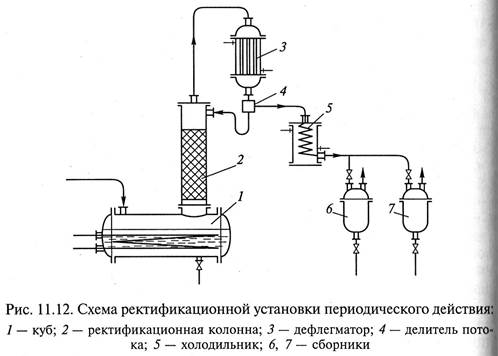
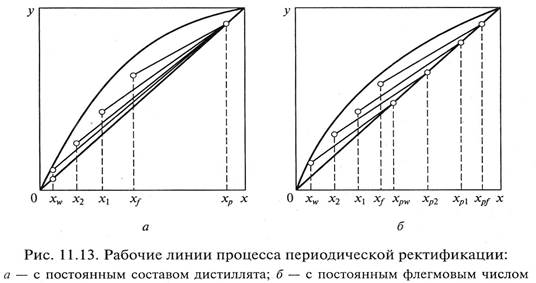
где r – удельная теплота конденсации (парообразования) греющего пара; хгр – степень сухости греющего пара. Периодически действующие ректификационные установки (рис. 11.12) представляют собой фактически укрепляющую часть ректификационного аппарата и работают по такому же принципу. Исходная смесь загружается в куб 1, где нагревается до температуры кипения и испаряется. Пары проходят через ректификационную колонну 2, взаимодействуя в противотоке с жидкостью, возвращаемой из дефлегматора 3. В дефлегматоре обогащенные легколетучим компонентом пары конденсируются, и конденсат j поступает в делитель потока 4. Флегма из делителя направляется на орошение ректификационной колонны, а дистиллят через холодильник 5 направляется в сборник 6 или 7. Эти установки могут работать в режимах постоянного расхода флегмы и постоянного состава дистиллята (рис. 11.13). Для обеспечения режима постоянного состава дистиллята (хp = const) (рис. 11.13, а) процесс ректификации необходимо проводить при непрерывно изменяющемся флегмовом числе, минимальном в начале процесса и максимальном в конце. Для концентраций х f и хр положение рабочей линии находится на основании уравнения рабочей линии для укрепляющей части колон ны (11.10). При этом по мере отгонки летучего компонента концентрация его в кубе уменьшается до х w, проходя через ряд промежуточных значений, например х1, х2 и т.д. Проведение процесса ректификации при режиме хр = const практически весьма затруднительно, поскольку для этого требуется непрерывное и четкое изменение питания колонны флегмой. По этой причине рассмотренный режим ректификации применяется в промышленности достаточно редко.
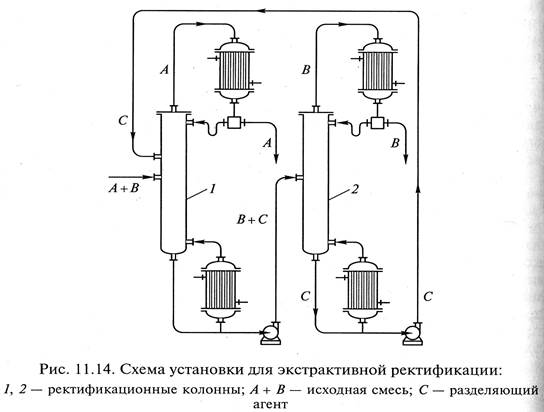
Более широкое распространение в промышленности получил режим периодической ректификации в условиях постоянного значения флегмового числа (R = const). Преимущество этого способа заключается в том, что с помощью одного ректификационного аппарата можно разделить смесь, состоящую из большого числа компонентов. При постоянном флегмовом числе наклон рабочих линий не зависит от концентраций. Пусть в первый момент ректификации концентрация летучего вещества в кубовой жидкости составляет величину х f, а в дистилляте - хр f (рис. 11.13, б). По мере осуществления процесса концентрация летучего компонента в кубовой жидкости будет уменьшаться и принимать значения х1, х2 и далее вплоть до конечного значения х w. Соответственно будет уменьшаться и концентрация летучего компонента в дистилляте: хр f, хр1 хp2 и т. д. В результате будет получен дистиллят среднего состава в пределах хр f – хрw, и остаток состава хw либо несколько продуктов с близкой, но постоянно уменьшающейся концентрацией в них легколетучего компонента. Экстрактивная ректификация предназначена для разделения смесей компонентов с близкими температурами кипения и очень низкой относительной летучестью (α ≤ 1,05). В этом случае в исходную смесь вводится третий компонент, предназначенный для резкого увеличения летучести основных компонентов. Вводимый компонент должен быть менее летуч, чем оба исходных компонента разделяемой смеси, и должен хорошо растворять низколетучий компонент разделяемой смеси. Установка для экстрактивной ректификации состоит из двух обычных ректификационных колонн 1 и 2 (рис. 11.14), в первую из которых поступает на разделение исходная смесь компонентов А и В. В укрепляющую часть колонны одновременно вводится разделяющий агент С. Выбор компонента С производят в соответствии с ранее приведенными условиями, чтобы он хорошо растворялся в компоненте В, в то время как А и С взаимно нерастворимы (или ограниченно растворимы). Летучести компонента А и смеси В + С становятся существенно различными, и в результате процесса ректификации в дистилляте получают практически чистый компонент А, а смесь В + С удаляется из первой колонны в виде кубового остатка и подается на разделение во вторую последовательно установленную колонну. В ней осуществляется разделение смеси на компоненты В и С.

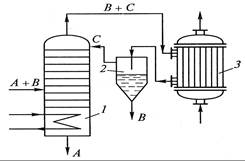
Компонент В является целевым и отбирается из установки, а регенерированный компонент С возвращается в первую колонну для повторного использования. Азеотропная ректификация смеси А и В, находящейся в термодинамическом равновесии, осуществляется аналогичным способом. К азеотропной смеси* добавляют третий компонент С, образующий садним из разделяемых компонентов новую (более летучую, чем исходная) азеотропную смесь. Эта азеотропная смесь выделяется в качестве дистиллята, а другой практически чистый компонент удаляется в виде кубового остатка. Вариант схемы азеотропной ректификации показан на рис. 11.15, когда образующаяся азеотропная смесь состоит из компонентов с резко отличающейся взаимной растворимостью при разных температурах. С этой целью после дефлегматора 3 установлен отстойник 2, где происходит разделение компонентов В и С. Компонент В отводится из установки, а компонент С возвращается в колонну 1. Примером такого процесса является разделение азеотропной смеси этиловый спирт – вода, где в качестве вводимого разделяющего компонента применяется бензол, образующий с водой и спиртом тройную азеотропную смесь с более низкой температурой кипения (64,8 °С), чем для азеотропной смеси спирта с водой (-78 °С). Ректификационные аппараты Для ректификации применяют практически исключительно аппараты колонного типа – насадочные и барботажные ректификационные колонны. По устройству они не отличаются от абсорберов аналогичного типа. Насадочные ректификационные колонны обычно применяют с кольцевой насадкой. Недостатки, присущие насадочным абсорберам, несущественны при ректификации, так как в этом процессе разделяются чистые однородные смеси, не требуется отвода теплоты, а количество орошающей жидкости обычно достаточно велика. В укрепляющей части колонны количество жидкости меньше количества поднимающихся паров на количество отводимого дистиллята, в исчерпывающей части колонны к
|
|||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-12-09; просмотров: 407; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.252.140 (0.109 с.) |