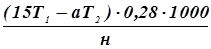Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение подвижных форм соединений макро- и микроэлементов
Определение легкогидролизуемого азота по Тюрину и Кононовой Значение анализа. Для оценки подвижности азота в почве важное значение имеет определение, наряду с нитратами и аммонием, легкогидро-лизуемых органических соединений этого элемента. При обработке почвы слабым раствором кислоты происходит переход аминокислот, амидов, аминосахаров и других легкогидролизуемых азотсодержащих органических соединений, а также минеральных форм азота (N-NO3 - + N-NO4-) в гидролизат. Поскольку легкогидролизуемые органические соединения быстро минерализуются, содержащийся в них азот рассматривается как ближайший резерв минерального азота в почве. Специальными исследованиями выявлена положительная корреляция между концентрацией легкогидролизуемого азота в почве, эффективностью азотных удобрений сельскохозяйственных культур. Принцип метода. Почву на холоде обрабатывают 0,5 н. раствором серной кислоты при соотношении почвы и раствора 5:5. В гидролизате определяют общий азот объемным методом после перевода его в аммонийную форму. Метод учитывает присутствующие в кислотной вытяжке минеральные формы азота (N-NO3- + N-NO4 -) и легкогидролизуемый органический азот (аминокислот, амидов, легкогидролизуемые группы белков). Ход анализа. На технических весах отвешивают 20 г воздушно-сухой почвы, просеянной через сито с диаметром отверстий 1 мм, из которой предварительно выбраны корешки. Навеску почвы помещают в коническую колбу емкостью 200 - 250 мл и приливают 100 мл 0,5 н. H2SO4. Встряхивают содержимое колбы в течение 3 мин и оставляют на 16 - 18 ч при комнатной температуре. Затем вытяжку фильтруют через сухой складчатый фильтр, давая фильтрату стечь полностью. В зависимости от предполагаемого содержания легкогидролизуемого азота пипеткой переносят 25 - 50 мл в коническую колбу емкостью 100 мл, прибавляют для восстановления нитратов до аммиака 0,5 г смеси цинковой пыли и восстановленного железа, закрывают воронкой и нагревают на закрытой электроплитке до слабого кипения и полного растворения прибавленной смеси. После охлаждения обмывают воронку дистиллированной водой, из бюретки приливают в колбу 5 мл концентрированной H2SO4 (плотностью 1,84) и выпаривают раствор на слабом газовом пламени или электрической плитке до появления белых паров воды с оксидами серы или побурения жидкости в колбе. Охладив колбу, добавляют 2 мл 20%-ного раствора хромовой кислоты или 2,5 мл 10 % раствора дихромата калия (К2Сг2О7), закрывают ее маленькой воронкой и кипятят в течение 10 мин до появления интенсивной зеленой окраски раствора.
Содержимое конической колбы после охлаждения переносят в отгонную колбу Кьельдаля емкостью 300 - 500 мл, обмывают коническую колбу несколько раз дистиллированной водой с таким расчетом, чтобы общий объем жидкости в колбе Кьельдаля составил 100 - 120 мл. В отгонную колбу опускают несколько гранул цинка или пемзу. Перед этим в стакан емкостью 250 - 300 мл наливают 15 мл 0,02 н H2SO4, прибавляют 5 капель индикатора конго красного или Гроага. Данный стакан и служит приемником для отгоняемого аммиака. В отгонную колбу приливают 20 мл 50 % NaOH и быстро присоединяют ее к каплеуловителю прибора, который соединен со стеклянной трубкой, опущенной в приемник с 15 мл 0,02 н H2SО4. В течение 30 минут - 1 часа ведут отгонку аммиака. Окончание отгонки азота определяют путем контрольной пробы с реактивом Несслера. Часть взятой в приемник кислоты идет на связывание аммиака; остаток же несвязанной H2SO4 оттитровывают 0,02 н щелочью (NaOH). При вычислении количества легкогидролизуемого азота в почве исходят из того, что 1 мл 0,02 н H2SO4 соответствует 0,28 мг азота. Содержание легкогидролизуемого азота (х) в миллиграммах на 1 кг почвы находят по формуле: Х = где 15 - количество 0,02 н H2SO4, взятой в приемный стакан при отгонке аммиака, мл; Т1 - поправка к титру Н2SO4, a - количество 0,02 NаОН, израсходованное на титрование несвязанной аммиаком кислоты в приемном стакане (за вычитанием контрольного анализа), мл; Т2 - поправка к титру NaOH; 0,28 - масса N, соответствующая 1 мл 0,02 н H2SO4, мг; 1000 - коэффициентдля пересчета результатов анализа на 1 кг почвы; н - навеска почвы, соответствующая объему анализируемого фильтрата (взятого для отгонки), г.
Реакции при гидролизе, отгоне и связывании аммиака. При обработке почвы 0,5 н H2SO4 происходит гидролиз органических соединений, в результате чего в раствор переходит, наряду с нитратами и аммонием, некоторое количество азота аминокислот, амидов и простых белков. При взаимодействии амидов с серной кислотой образуются органические кислоты и выделяется аммиак, который сразу же связывается избытком H2SO4;
R-CO-NH2+H2O+ H2SO4 = R-COOH + (NH4)2SO4. Органические кислоты в дальнейшем окисляются дихроматом калия (К2Сг2О7) до СО2 и Н2О. Дихромат калия окисляет также аминокислоты по следующей схеме: R - COO (NH 2)- CO О H + К2С г 2О7 + H 2 SO 4 = Cr 2 (SO 4)3 + (NH)2 S 04 + СО2 + Н2О. В сильнокислой среде шестивалентный хром восстанавливается до трехвалентного, что сопровождается изменением красно-оранжевого цвета раствора дихромата калия в зеленый, присущий сульфату хрома. 2 К 2 С r2 О 7 + 8H2SO4 = 2K2SO4 + 2Cr2(SO4)3 +8H2O + + ЗО 2 Пары кипящей серной кислоты распадаются на серный ангидрид и воду: H 2 SO 4 = SO 3 + Н2О. В свою очередь, серный ангидрид распадается на диоксид серы и кислород: 2 SO 3 = 2 SO 2 + О2 Кислород участвует в окислении углерода тех органических соединений, которые перешли из почвы в кислотную вытяжку, до углекислого газа и воды, соответственно, а диоксид серы переводит азот аминогрупп (NН2) в аммиак, который связывается серной кислотой 2 NH 3 + H 2 SO 4 = (NH 4)2 SO 2. Нитраты, находящиеся в вытяжке, при добавлении смеси цинка и железа восстанавливаются до аммиака: H 2 SO 4 + Fe = FeSO 4 +Н2О HNO 3 + Н2 = Н N О2 + Н2О: HNO2 + 3H2 = NH3+ 2H2O 2NH3 + H2SO4 = (NH4)2SO4. Аммиак вытесняется из сульфата аммония в отгонной колбе щелочью и вновь связывается кислотой в приемнике. (NH4)2SO4 + 2NaOH = Na2SO4 + 2NH4OH; 2NH4OH= 2NH3 + 2H2O; 2NH3 + H2SO4 = (NH4)2SO4. Использование результатов анализа. Полученные данные по содержанию легкогидролизуемого азота в почве позволяют оценить обеспеченность почвы подвижным азотом и ориентировочно прогнозировать эффективность азотных удобрений.
|
||||||
|
Последнее изменение этой страницы: 2020-11-11; просмотров: 147; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.254.231 (0.006 с.) |