
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Обоснование способа производства
Получение серной кислоты из сероводорода (мокрый катализ) на Пермском нефтеперерабатывающем заводе является малотоннажным производством (65тыс. тонн в год). В основном, это производство создано для того, чтобы снизить выбросы серосодержащих газов и максимально перерабатывать сырье, которое в данном случае является отходом процесса гидроочистки нефти. Помимо использования сероводорода, в процессе получения серной кислоты протекают 3 реакции: Н2S + 1,5О2 = SО2 + Н2О SО2 + 0,5О2 <=> SО3 SО3 + Н2О <=> Н2SО4 Эти три реакции протекают с выделением значительного количества тепла, которое используется для различных нужд цеха производства серной кислоты и в различных целях предприятия: получение пара, который используется в данном производстве, получение пара высокого давления, который используют другие установки, подогрев воздуха, поступающий в котлы для сжигания сероводорода и в контактный аппарат. Преимущество получения серной кислоты из сероводорода заключается в том, что данный процесс максимально использует и сероводород, и диоксид серы, что в значительной мере снижает выбросы в атмосферу, при проведении процесса, состоящего из 3 реакций, используются невысокие температуры и атмосферное давление, что значительно снижает энергозатраты по сравнению со схемой, которая применяет высокое давление. С учетом того, что в результате технологического процесса выделяется большое количество тепла, процесс, благодаря этому, протекает автотермично.
Стадии и химизм процесса Процесс получения серной кислоты методом "мокрого" катализа состоит из следующих основных стадий. 1. Получение сернистого ангидрида (SO2) путем сжигания сероводородсодержащего газа по следующей реакции:
2H2S + 3O2 = 2SO2 + 2 H2O
2. Охлаждение дымовых газов и утилизация тепла реакции горения сероводорода в котле-утилизаторе с получением водяного пара. 3. Окисление сернистого ангидрида до серного ангидрида (SO3) на ванадиевом катализаторе в контактном аппарате (конвертере) R-104 по следующей реакции:
2SO2 + O3 = 2 SO3
4. Получение серной кислоты (H2SO4) путем конденсации в конденсаторе WSA У-109 по реакции:
SO3 + H2O = H2SO4
5. Для получения улучшенной серной кислоты (содержание окислов азота N2O3 менее 0,5 ppm) предусмотрена схема подачи гидразингидрата в поток серной кислоты, поступающей на участок концентрирования серной кислоты.
Гидразинсульфат, полученный при добавлении гидразина к серной кислоте, взаимодействует с нитрозилсернистой кислотой, обуславливающей содержание N2О3 в продуктовой кислоте:
Избыток гидразина окисляется с образованием элементарного азота:
Химический состав серной кислоты выражается формулой H2SO4. Структурная формула серной кислоты выглядит следующим образом:
Относительная молекулярная масса серной кислоты - 98,08 кг/кмоль. Безводная серная кислота содержит 100 % H2SO4 или 81,63 % SO3 и 18,37 % мас. H2O. Это бесцветная маслянистая жидкость не имеющая запаха с температурой кристаллизации 10,37 ºС. Температура кипения безводной серной кислоты при давлении 1,01·105 Па (760 мм рт.ст.) составляет 298,2 ºС. Плотность при 20 ºС составляет 1830,5 кг/м3. С водой и сернистым ангидридом серная кислота смешивается в любых пропорциях. В процессе производства серной кислоты для окисления сернистого ангидрида в серный применяются ванадиевый катализатор. Он представляет собой пористое вещество, на которое нанесено активное комплексное соединение, содержащее пятиокись ванадия V2O5. В данном случае применяется катализатор марки VK-WSA фирмы "Хальдор Топсе". Температура зажигания катализатора 400-430 ºС. При температуре выше 620 ºС активность катализатора быстро снижается, т.к. при этом распадается активный комплекс, содержащий пятиокись ванадия (V2O5), а также разрушается структура носителя, что приводит к разрушению катализатора и образованию пыли. Срок службы катализатора не менее 4 лет. Термодинамический анализ Расчет теплового эффекта реакции окисления SO 2 в SO 3:
2SO2 + O2 = 2 SO3
Q=-ΔН=196,6 кДж
Реакция экзотермическая – протекает с выделением тепла.
ΔS= ΔG=ΔH-TΔS=-196,6-298*17,66=-5459,28
Энергия Гиббса значительно меньше нуля. Это значит, что реакция термодинамически возможна. Расчет теплового эффекта реакции конденсации SO 3:
SO3 + H2O = H2SO4
Q=-ΔН=174,26 кДж
Реакция экзотермическая- протекает с выделением тепла.
ΔS= ΔG=ΔH-TΔS=-174,26-298*-288,07=-86019,12
Энергия Гиббса значительно меньше нуля. Это значит, что реакция термодинамически возможна.
Таблица 1 Значения термодинамических величин
Таблица 2 Значения Кр для реакции окисления SO2 при различных температурах
Вывод: реакция окисления SO2 наиболее полно протекает при невысоких температурах. Из этого следует, реакцию окисления SO2 целесообразно проводить при невысоких температурах. Повышение давления, по принципу Ле-Шателье, влияет положительно.
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-03-14; просмотров: 184; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.216.229 (0.01 с.) |
 4NOSO3H + N2H4· H2SO4 3N2 + 5H2SO4
4NOSO3H + N2H4· H2SO4 3N2 + 5H2SO4 N2H4·H2SO4 + O2 N2 +2H2O + H2SO4
N2H4·H2SO4 + O2 N2 +2H2O + H2SO4 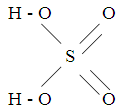
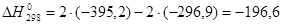 кДж
кДж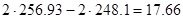
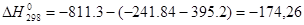 кДж
кДж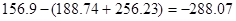 Дж
Дж


