
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Процес и окис н е нн я вуглеводнівСтр 1 из 10Следующая ⇒
Процес и окис н е нн я вуглеводнів Зміст Вступ Характеристика процесів окиснення. Визначення і класифікація реакцій окиснення Окиснювальні агенти і техніка безпеки у процесах окиснення Окиснювальні агенти Молекулярний кисень Азотна кислота Пероксидні з’єднання Техніка безпеки процесів окиснення Енергетична характеристика реакцій окиснення Радикально-ланцюгове окиснення 3.1 Гідропероксиди 3.2 Карбонові кислоти 3.3 Альдегіди Кінетика і каталіз реакції радикально-ланцюгового окиснення Селективність окиснення Реактори процесів рідинофазного окиснення 4.1 Характеристика реакторів Окиснення вуглеводнів у гідро пероксиди Синтез фенолу та ацетону Отримання гідропероксидів Кислотне розкладання гідро пероксидів Окиснення парафінів Окиснення нижчих парафінів у газовій фазі Гетерогенно-каталітичне окиснення вуглеводнів та їх похідних 7.1 Теоретичні основи процесу Гетерогенні каталізатори окиснення і механізм реакцій Кінетика і селективність гетерогенно-каталітичного окиснення Реактори процесів гетерогенно-каталітичного окиснення Окиснення олефінів по насиченому атому вуглецю Окиснення пропілену в акролеїн Одержання акрилової кислоти Окисний амоноліз вуглеводнів Література
Вступ
Тема реферату «Процеси окиснення вуглеводнів» з дисципліни «Технологія нафтохімічного синтезу». Практичне значення процесів окиснення у виробництві основного органічного та нафтохімічного синтезу важко переоцінити. Їх першорядну роль обумовили наступні причини: 1.Велика цінність сполук, отриманих окисненням (спиртів, альдегідів, кетонів, карбонових кислот та їх ангідридів, a-оксидів, нітрилів та ін.) і проміжними продуктами органічного синтезу, розчинниками, мономерами і вихідними речовинами для виробництва полімерних матеріалів, пластифікаторів і т.д. 2.Широке різноманіття реакцій окиснення, до яких здатні багато органічних речовин, у тому числі вуглеводні всіх класів. Це дозволяє використовувати процеси окиснення для первинної переробки вуглеводневої сировини і робити на їх основі велику кількість коштовних речовин.
3.Приступність і низька вартість більшості окиснювачів, серед яких головне місце займає кисень повітря. Це визначає більш високу економічність синтезу деяких продуктів методами окиснення в порівнянні з іншими можливими методами їх виробництва. Окисні процеси одержали широке поширення в органічному синтезі, часто заміняючи менш економічні способи виробництва багатьох продуктів.
Окиснювальні агенти і техніка безпеки у процесах окиснення
Окиснювальні агенти У промисловості основного органічного синтезу використовуються дешеві окиснювачі і лише в окремих випадках застосовують агенти, здатні до реакцій, що не протікають у присутності інших окиснювачів.
Молекулярний кисень Найважливіший окисний агент використовується у виді повітря, технічного кисню, азотнокислих сумішей з невеликим вмістом кисню. Концентрований кисень робить більш сильну окиснюючу дію, але його застосування зв'язане з додатковими витратами на поділ повітря. При окисненні в газовій фазі, коли суміш азоту утрудняє виділення продуктів або їх рециркуляцію, використовують і технічний кисень. Меншу швидкість реакції при окисненні повітрям компенсують підвищенням температури або збільшенням загального тиску, що веде до росту парціального тиску кисню.
Азотна кислота Азотна кислота (рідше оксиди азоту) служить другим за масштабами застосування окисним агентом. Її дія нерідко супроводжується побічним нитруванням органічної сполуки, що підсилюється з підвищенням концентрації кислоти. З цієї причини для окиснення використовують 40-60 %-ву азотну кислоту. Азотна кислота як окиснювач ніколи не застосовується для реакцій з парафінами. Для неї найбільш типовими реакціями є реакції деструктивного окиснення циклічних з'єднань і речовин з ненасиченими зв'язками, що йдуть за участю азотної кислоти, із кращим виходом, чим при окиснюванні киснем.
—ОН
При окисненні азотною кислотою вона розкисняється до оксидів азоту (NO або N2O3). Економічність виробництва багато в чому залежить від можливості утилізації цих оксидів і регенерації неперетвореної азотної кислоти. Перша задача вирішується окиснюванням оксидів азоту повітрям у водному або азотнокислому розчині з утворенням азотної кислоти:
N2O3 + O2 + H2O ® 2HNO3 Пероксидні з’єднання Пероксидні з'єднання, головним чином пероксид водню і перуксусна кислота (а останнім часом і гидропероксиди), набутили застосування як окисні агенти в основному органічному та нафтохімічному синтезі порівняно недавно. Через відносну дорожнечу їх використовують тільки для таких реакцій, що не протікають під впливом молекулярного кисню або азотної кислоти. Це відноситься насамперед до процесів епоксидирування ненасичених з'єднань:
-ООН + RCH=CH2 ® -OH + RCH-CH2O
Пероксид водню звичайно застосовують у виді 30 %-вого водного розчину. Він дає з карбоновими кислотами відповідні пероксикислоти за реакціэю, аналогічною реакції етерифікації:
RСООН + Н2О2 «RСОООН + Н2О
Пероксикислоти утворюються, крім того, окисненням альдегідів. Так, перуксусна кислота виробляється цим шляхом у промисловому масштабі, а гідропероксиди одержують у промисловості окиснюванням вуглеводнів:
СН3-СНО + О2 ® СН3-СОООН С6Н5-СН(СН3)2 + О2 ® С6Н5-С(СН3)2 ООН
Гідропероксиди
Гідропероксиди– це первинні молекулярні продукти окиснення вуглеводнів. Ланка ланцюга при їх утворенні така:
R· + О2 ® ROO·, ROO· + RH ® ROOH + R· Гідропероксиди відносяться до числа досить нестабільних з'єднань, що перетворюються при окисненні в інші продукти. Тому їх концентрація в реакційній масі, особливо при каталітичному окисненні і при підвищених температурах, невелика. Найбільш нестабільні первинні гідропероксиди (RCH2OOН, ArCH2OOH) і навпаки, відносно стабільні третинні гідропероксиди, з яких гідропероксиди ізобутану (СН3)3СООН і ізопропілбензолу С6Н5С(СН3)2ООН є промисловими продуктами. З вторинних відносно стабільні гідропероксиди циклоалканів С8-С12, олефінів і алкілароматичних з'єднань. Спирти і карбонільні з'єднання є вторинними продуктами окиснення вуглеводнів. Спирти виходять тільки при окисненні парафінів і нафтенів:
спирт
 Алкан Алкан  гідропероксид ® гідропероксид ®
кетон
Гідропероксиди при розкладанні під дією підвищеної температури або каталізаторів окиснення дають спирти і карбонільні з'єднання. При одержанні спиртів ланка ланцюгу така:
ROOH + R· ® ROH + RO·, RO· + RH ® ROH + R·
Кетони утворюються з вторинних гідропероксидів через стадію радикал-гідропероксидів:
R2CHOOH + HO·
Третинні гідропероксиди при ланцюговому перетворенні дають крім спирту, з тим же числом вуглецевих атомів, також спирт і кетон, але з меншим числом атомів вуглецю за рахунок деструкції вуглець-вуглецевого зв'язку:
R3COOH + R· ® ROH + R3CO· R3CO· ® R2C=O + R·
Ці механізми реакції характерні для некаталітичного окиснення в рідкій фазі при помірних температурах. При високотемпературному окисненні в газовій фазі всі продукти утворюються через пероксидні радикали, минаючи гідропероксиди, причому відбувається значна деструкція за вуглець-вуглецевим зв'язком з утворенням спиртів і альдегідів:
СН3-СН2-СН2ОО· ® НСНО + СН3-СН2О· СН3-СН2ОН СН3-СН-СН3 ® СН3СНОСН3О·
ОО·
Зараз вважають, що при рідинофазному окисненні утворення продуктів відбувається через пероксидні радикали:
R2CH ® R2C· ® R2C=O + HO·OO· OOH
При каталізі солями металів перемінної валентності останні можуть давати комплекси з пероксидними радикалами, що перетворюються в координаційній сфері центрального іона, окисняючи його у вищий валентний стан:
Таким чином, спирти і карбонільні з'єднання можуть виходити при рідинофазному окисненні не тільки послідовно стосовно гідропероксиду, але і паралельно з ним.
Карбонові кислоти
Карбонові кислоти утворяться при окисненні вуглеводнів зі збереженням їх вуглецевого ланцюгу або з деструкцією за С-С-зв'язком. Перше можливо лише при перетвореннях первинних гідропероксидів і типово тільки лише для окиснення метильных груп алкілароматичних з'єднань через проміжну стадію альдегідів:
ArCH3
При окисненні парафінів і нафтенів карбонові кислоти утворяться з деструкцією вуглецевого ланцюгу. Безпосередніми попередниками кислот є кетони, які окиснюються легше, утворюючи кетопероксидний радикал і кетогідропероксид:
RCH2-COR¢ RCH-COR¢ ® RCHO + RCOOH Альдегіди
Альдегіди є найбільше легко окиснюємимі з'єднаннями, тому при окиснюванні вуглеводнів у рідкій фазі вони або утворяться в невеликій кількості, або їх узагалі не вдається знайти в продуктах реакції. При радикальному окисненні вони дають проміжні ацильний і пероксиацильний радикали і пероксикислоту:
RCOOO· + RCHO ® RCOOOH +
Крім пероксикислоти і карбонової кислоти
СН3-СОООН + СН3-СНО ® 2СН3-СООН
іншими продуктами окиснення є ангідриди. Їх утворенню сприяє застосування змішаного каталізатору (солі кобальту або марганцю із солями міді) і знижений парціальний тиск кисню.
Селективність окиснення
Селективність залежить від розвитку рівнобіжних і послідовних перетворень при утворенні цільових і побічних продуктів. Рівнобіжні перетворення можуть бути обумовлені двома факторами: реакціями по різних атомах вуглецю в молекулі вихідного реагенту або рівнобіжним утворенням речовин з різними функціональними групами. Перші реакції залежать від відносної реакційної здатності різних атомів водню при атаці пероксидним або іншим кисеньмістким радикалом. У цьому відношенні радикально-ланцюгове окиснення відрізняється порівняно високою селективністю, що залежить від малої активності пероксидних радикалів. Реакційна здатність атомів водню у третинного, вторинного і первинного атомів вуглецю відноситься приблизно як 100:10:1.
Рівнобіжне утворення речовин з різними функціональними групами (утворення спиртів і кетонов з вуглеводнів, карбонових кислот і ангідридів з альдегідів) можна регулювати, підбираючи відповідні параметри процесу. При послідовних перетвореннях, крім розглянутих раніше продуктів, можуть виходити оксикетони, дікетони, окси- і кетокарбонові кислоти та ін. Спостерігається і повне окиснення до СО2. Головним способом зниження ролі цих побічних реакцій є регулювання ступеня конверсії. Усі процеси радикально-ланцюгового окиснення підрозділяються на дві групи: 1.Процеси, що протікають з цільовим одержанням речовин, стійких до подальшого окиснення (нижчі ароматичні та аліфатичні кислоти), коли ступінь конверсії не грає істотної ролі для селективности (ступінь конверсії a = 95-99 %), проміжну речовину можна повертати на окиснення разом з неперетвореним реагентом. 2.Процеси, спрямовані на цільовий синтез проміжних речовин, схильних до подальшого розкладання або окиснення (одержання гідропероксидів, спиртів, кетонів, вищих карбонових кислот), коли ступінь конверсії відіграє важливу роль і її обмежують величиною 5-30 %. У цьому випадку істотні витрати на регенерацію і рециркуляцію неперетвореного реагенту, ці процеси потрібно оптимізувати з урахуванням змін селективності і ступеня конверсії. Великий вплив на селективність робить температура. Енергія активації побічних реакцій звичайно вище, тому роль останніх росте зі збільшенням температури, а селективність падає. У результаті кожен процес має деяку оптимальну температуру. Підвищення температури може відігравати роль у перекладі процесу в дифузійну або близьку до неї область протікання реакції: процес відбувається в прикордонній плівці, проміжні продукти не встигають продифундувати в об’єм рідини і переокиснюються. Тому важливу роль грає ефективна турбулізація реакційної суміші при барботируванні газу-окиснювача, що сприяє переходу процесу в кінетичну область, розвитку поверхні контакту фаз і інтенсифікації процесу. Таким чином, вибір оптимальних умов процесу є досить складним. окиснення вуглеводень кинетика каталіз Характеристика реакторів 1. Реактор періодичної дії з виносним охолодженням за рахунок циркуляції рідини через водяний холодильник. Циркуляцію можна здійснювати й у протилежному напрямку, у тому числі і природним шляхом – за рахунок розходження щільностей рідин у колоні та у циркуляційному контурі. Вихідний реагент завантажують в апарат по закінченні попередньої операції, підігрівають до потрібної температури (у цей час замість води в холодильник надходить пара) і починають надавати повітря. Розподільним пристроєм служить перфорована труба, сітчата або ґратчаста тарілка.
2. Безперервне проведення процесу в одиничній барботажній колоні можливе при цільовому одержанні продуктів, стійких до подальшого окиснення (оцтова кислота, ароматичні кислоти). Окиснюєму речовину і повітря надають у низ реактора (прямоток), а продукти відбирають зверху. Відвід тепла можна здійснювати циркуляцією через водяний холодильник або вбудовані внутрішні холодильники. 3. Якщо селективність процесу залежить від ступеня конверсії вихідної речовини, то одинична барботажна колона не вигідна для безперервного процесу через сильне перемішування рідини. Такий процес краще проводити в каскадних барботажних колонах: рідка реакційна маса послідовно перетікає з колони в колону, а повітря надають роздільно в кожну. Теплоотвід може здійснюватися за рахунок випару вуглеводню або розчинника. Їх пари конденсуються в зворотних холодильниках, що знаходяться над кожною колоною. 4. Тарілчаста колона. У ній рідина перетікає зверху вниз з однієї тарілки на іншу, а повітря рухається протитоком. Для охолодження в змійовиках, поміщені в шари рідини на кожній тарілці, пропускають воду. Можливе і виносне охолодження. В усіх реакторах періодичної і безперервної дії режим окиснення регулюють, змінюючи швидкість подачі окиснювача і вихідного органічного реагенту. Температуру звичайно замірять у декількох крапках по висоті реактора; реакційну масу періодично аналізують. При рідинофазному окисненні необхідно виключити утворення вибухонебезпечних сумішей у місцях, де мається суцільна газова фаза, тобто у верхній частині барботажних колон і в просторі над кожною тарілкою (рис. 1, г). Це досягається високим ступенем конверсії кисню в сукупності з вибором тиску в залежності від летучості вихідної органічної речовини. Іноді в простір над рідиною передбачена подача азоту і т.д.
Синтез фенолу та ацетону
Гідропероксиди застосовуються як проміжні продукти (наприклад, у виробництві фенолу та ацетону), ініціатори полімеризації, у процесах епоксидирування олефінів:
C6H5-CH(CH3)2
RH
Отримання гідропероксидів У промисловості в найбільш великих масштабах одержують гідропероксид ізопропілбензолу (кумолу), у менш значних – гідропероксиди мета- і парацимолу (ізопропілтолуолу) і мета- і парадіізопропілбензолу для їх наступного перетворення у фенол, мета- і пара-крезол, резорцин, гідрохінон. Для епоксидирування олефинів використовують, головним чином, гідропероксиди етилбензолу та ізобутану. Усі вони є відносно стабільними речовинами. При одержанні концентрованих гідропероксидів (80-95 %) потрібні спеціальні міри безпеки: відсутність перегрівів і каталізаторів розкладання – металів перемінної валентності та їх солей, кислот. При окисненні вуглеводнів гідропероксди утворюються за радикально-ланцюговим механізмом. Інгібітори (фенол, олефіни, сіркомісткі з'єднання) сильно гальмують процес, тому вихідні вуглеводні повинні бути ретельно очищені від небажаних домішок. Ізопропілбензол, отриманий алкілуванням у присутності твердого фосфорнокислого каталізатора, не придатний для окиснення. Для зменшення індукційного періоду у вихідну сировину додають гідропероксид. Солі металів перемінної валентності розкладають гідропероксиди, однак в окремих випадках їх невеликі добавки прискорюють реакцію. Такий же ефект робить мідь, навіть якщо вона присутня в складі металу, який йде на виготовлення апаратури. При одержанні гідропероксидів завжди утворюються побічні продукти: спирти, кетони, діметилфенілкарбінол, ацетофенон, моно- і дигідропероксиди. Підвищенню селективності сприяє зниження температури і ступеня конверсії, параметри підтримують на оптимальному рівні, що залежить від економічних факторів. Температура складає 100-1500С, корисно знижувати її по мірі нагромадження гідропероксиду, щоб сповільнити його розкладання. Ступінь конверсії складає від 30 до 10 %. Для одержання алкілароматичних гідропероксидів використовують реактори тарілчастого типу (рис. 1, г) або каскад окисних колон (рис. 1, в). Окислення ведуть повітрям при тиску 0,3-0,5 МПа для ізопропілбензолу і 5-8 МПа – для ізобутану (в останньому випадку тиск необхідний для підтримки суміші в рідкому стані). Отриманий розчин гідропероксиду і побічних продуктів у вихідному вуглеводні звичайно “зміцнюють” або концентрують шляхом відгону вуглеводню.
Окиснення парафінів
Існують три напрямки окисної переробки парафинів: 1.Окиснення в газовій фазі, для одержання нижчих спиртів і альдегідів. 2.Термічне окиснення в рідкій фазі в присутності борної кислоти для синтезу вищих вторинних спиртів. 3.Каталітичне окиснення в рідкій фазі для одержання карбонових кислот. Процес каталітичного окиснення в рідкій фазі має найбільше практичне застосування.
Теоретичні основи процесу
Одержання акрилової кислоти Для одержання акрилової кислоти використовується вісмут-молібденовий каталізатор з різними промоторами (Те, Со, Р та ін.), але умови реакції більш м'які: Т = 200-3000С, t = 0,5-2,0 сек. Побічно утвориться оцтова кислота, СО2 і СО, селективність складає 90 %. Для реалізації процесу одержання акрилової кислоти в промисловості комбінують окиснення пропілену в акролеїн і окиснення акролеїну в акрилову кислоту. На початку здійснили одностадійний процес прямого окиснення пропілену в акрилову кислоту в одному реакторі. Однак вихід її склав всего 70 %, оскільки сполучення двох стадій з різними для них оптимальними умовами не могло сприяти росту селективності. Зараз застосовується двостадійний процес одержання акрилової кислоти (рис. 4). У реактор першої стадії надають суміш, що містить 4-7 % пропілену, 50-70 % повітря, 25-40 % водяної пари; температура складає 300-4000С; каталізатор - Bi2O3×MoO3. У реакторі другої ступені температура складає 250-3000С, використовуваний каталізатор - Bi2O3×MoO3. Отриманий водний розчин містить 20-30 % акрилової кислоти з домішкою оцтової кислоти. Для виділення цільового продукту застосовують екстракцію низкокиплячим органічним розчинником. Його відганяють з екстракту і повертають на витяг, а при ректифікації залишку одержують акрилову та оцтову кислоту. Вихід складає 80-85 % за пропіленом. Л ітература 1. Лебедев Н.Н. Химия и технология основного органического и нефтехимического синтеза. – М.: Химия, 1988. С. 338-367. 2. Тимофеев В.С., Серафимов Л.А. Принципы технологии основного органического и нефтехимического синтеза. – М.: Высшая школа, 2003. С. 16-22, 335-348.
Процес и окис н е нн я вуглеводнів Зміст Вступ
|
|||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-03-02; просмотров: 236; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.15.147.215 (0.063 с.) |

 НООС-(СН2)4-СООН + 2N2O3 + 3H2O
НООС-(СН2)4-СООН + 2N2O3 + 3H2O
 R2
R2  OOH ® R2C=O + HO·
OOH ® R2C=O + HO· НСНО +
НСНО + СН3-СНО + СН3ОН
СН3-СНО + СН3ОН + Co(OAc)2 «
+ Co(OAc)2 « ArCH2OOH
ArCH2OOH  ArCHO
ArCHO  ArCOOH
ArCOOH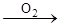 RCH-COR¢
RCH-COR¢  RCH-COR¢ OO·OOH
RCH-COR¢ OO·OOH RCOOH + R¢COOH OOH
RCOOH + R¢COOH OOH =O + O2 ® RCOOO·
=O + O2 ® RCOOO· =O
=O
 C6H5-C-(CH3)2
C6H5-C-(CH3)2  C6H5OH + CH3-CO-CH3
C6H5OH + CH3-CO-CH3
 ROH + CH3-CH-CH2O
ROH + CH3-CH-CH2O


