
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Особенности и классификация коллоидных ПАВ
Коллоидными называют такие ПАВ, молекулы которых способны образовывать мицеллы. Мицеллы — это агрегаты из десятков молекул ПАВ (рис. 21.1). Коллоидные ПАВ находятся в трех различных состояниях: на поверхности раздела фаз в виде адсорбционного слоя, в качестве истинного раствора и в составе мицелл, которые образуют коллоидный раствор. Схематически различное состояние молекул ПАВ можно представить следующей схемой:
Поверхность раздела, -> Истинный Условие (21.1) означает, что истинный раствор переходит в коллоидный, состоящий из мицелл. Поэтому коллоидные ПАВ называют еще мицеллярными*. Число молекул ПАВ в мицеллах обычно составляет 50—100, а мицеллярная масса равна 103—105. Мицеллы коллоидных ПАВ, размеры которых соответствуют высокодисперсным системам, формируют дисперсную фазу; образуется граница раздела между мицеллой и растворителем — дисперсионной средой. Растворы этого класса ПАВ обладают и дисперсностью, и гетерогенностью, т.е. основными признаками коллоидных растворов. Не все растворы ПАВ являются коллоидными. Низкомолекулярные спирты, кислоты, другие органические соединения, которые имеют незначительную длину углеводородного радикала, не образуют мицелл. Для коллоидных ПАВ характерно оптимальное соотношение между углеводородным гидрофобным радикалом и полярной гидрофильной частью молекулы. Подобное соотношение определяется гидрофильно-липофильным балансом (см. рис. 15.3). Коллоидные ПАВ широко распространены. К ним относятся синтетические моющие и чистящие средства, мыла, красители, танниды и многие другие вещества. Производство коллоид-
ных ПАВ постоянно растает. В той или иной мере они применяются в различных отраслях промышленности; не является исключением и пищевая промышленность (см, подробнее параграф 21.4). Коллоидные ПАВ, молекулы которых имеют дифильное строение (см. рис. 5.2), можно классифицировать в зависимости от их способности к диссоциации на ионогенные и неионогенные. В свою очередь ионогенные ПАВ могут быть анионные (анионо-активные), катионные (катионоактивные), амфолитные (амфо-терные).
Ионогенные ПАВ диссоциируют в растворе с образованием поверхностно-активных ионов. Неионогенные ПАВ не диссоциируют, а поверхностная активность их обусловлена молекулами вещества. После диссоциации полярных групп [СООН(М), OSO2OH(M), SO3H(M), где М — металл] анионных ПАВ образуется анион, который является носителем поверхностно-активных свойств, и катион, не обладающий этими свойствами. Примером анионного ПАВ является натриевая соль стеариновой кислоты, которая входит в состав обычного жирового мыла; поверхностно-активный анион образуется следующим образом: C17H35COONa -* С,7Н35СОО +Na + (212) Поверхностная активность определяется анионом, который в данном случае представляет собой остаток стеариновой кислоты. К синтетическим анионным ПАВ относится додецилсульфат натрия, который в водном растворе диссоциирует по следующей схеме: CH3(CH2)10CH2OSO3Na —> CH3(CH2)10CH2OSO3 +Na+. (21.3) Поверхностно-активный анион, подобно молекулам ПАВ (см. рис. 5.2), имеет гидрофильную часть и длинный гидрофобный радикал. Для моющих средств, например, длина этого радикала колеблется в пределах С12—С20. Катионные ПАВ диссоциируют в водном растворе с образованием поверхностно-активного катиона. Из катионных коллоидных ПАВ наибольшее распространение получили четвертичные аммониевые соли, представителем которых является октадециламмонийхлорид; он диссоциирует следующим образом: [c17h35nh3] ci-> c17h35nh; +сг (21.4) Катион C,7H35NH3+ > определяет поверхностно-активные свойства этой группы ПАВ. Амфолитные коллоидные ПАВ в зависимости от рН проявляют свойства анионных и катионных веществ, т.е. поверхностно-активными свойствами обладают анион и катион подобных ПАВ. К числу амфолитных ПАВ относятся белки (см. параграф 20.2). Однако амфолитные коллоидные ПАВ из-за относительно высокой стоимости и сложности получения не нашли еще широкого практического применения в качестве синтетических препаратов. Неионогенные коллоидные ПАВ не диссоциируют в растворе и не образуют ионы. Поверхностной активностью обладают растворенные молекулы ПАВ. К числу распространенных неионогенных ПАВ относятся препараты ОП-7 и ОП-10. Их получают в результате взаимодействия оксида этилена со спиртами, фенолами, жирными кислотами или другими органическими соединениями, в
состав которых входят полярные группы. Общую формулу этих препаратов можно представить в виде -СН2О)„Н Сложные эфиры сахарозы, которые применяют при производстве маргарина, мороженого, шоколада и других продуктов, относятся к неионо-генным ПАВ. Они образуются в результате следующей реакции:
CH3O+(C12H22On)OCR. сложный эфир
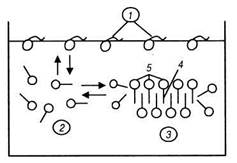
метиловый эфир В настоящее время ассортимент коллоидных ПАВ включает десятки тысяч различных наименований. Молекулы могут состоять из нескольких полярных групп и углеводородных радикалов. Приведенные в уравнениях (21.2)—(21.4) формулы ионо-генных и неионогенных ПАВ являются простейшими. 21.2. Критическая концентрация мицеллообразования Рассмотрим более подробно распределение молекул ПАВ в растворе (см. рис. 21.1). Часть молекул ПАВ адсорбируется на границе раздела жидкость — газ (вода — воздух). Все закономерности, которые были ранее рассмотрены для адсорбции ПАВ на границе раздела жидкости с газовой средой (См. гл. 4 и 5), справедливы и для коллоидных ПАВ. Между молекулами ПАВ в адсорбционном слое 1 и молекулами в растворе 2 существует динамическое равновесие. Часть молекул ПАВ в растворе способна образовывать мицеллы J; между молекулами ПАВ в растворе и молекулами, входящими в состав мицелл, также существует равновесие. Это равновесие на рис. 21.1 показано стрелками. Процесс образования мицелл из молекул растворенных ПАВ можно представить следующим образом: ^ (21.5) где М — молекулярная масса молекулы ПАВ: т — число молекул ПАВ в мицелле. Рис. 21.1. Положение коллоидных ПАВ: 7 — на поверхности; 2 и 3 — в виде истинного и колоидного раствора; 4 — углеводородное ядро; 5 — полярные ионогенные группы Состояние ПАВ в растворе зависит от их концентрации. При небольших концентрациях (10~4— 10~2Л/) образуются истинные растворы, а ионогенные ПАВ проявляют свойства электролитов. При достижении критической концентрации мицеллообразования (ККМ) образуются мицеллы, которые находятся в термодинамическом равновесии с молекулами ПАВ в растворе. При концентрации ПАВ выше ККМ избыток ПАВ переходит в мицеллы. При значительном содержании ПАВ могут образовываться жидкие кристаллы (см. параграф 21.4) и гели. В области, близкой к ККМ, образуются сферические мицеллы (рис. 21.3). При увеличении концентрации ПАВ возникают пластинчатые (рис. 21.1) и цилиндрические мицеллы. Мицеллы состоят из жидкого углеводородного ядра 4 (рис. 21.1), покрытого слоем полярных ионогенных групп 5. Жидкое состояние углеводородных цепей структурно упорядоченно и тем отличается от объемной жидкой (водной) фазы. Слой полярных групп молекул ПАВ выступает над поверхностью ядра на 0,2—0,5 нм, формируя потенциалобразующий слой (см. параграф 7.2). Возникает двойной электрический слой, который обусловливает электрофоретическую подвижность мицелл. Гидрофильная полярная оболочка мицелл резко снижает межфазовое поверхностное натяжение а на границе мицелла — жидкость (вода). При этом соблюдается условие (10.25), что означает самопроизвольное образование мицелл, лиофильность ми-целлярного (коллоидного) раствора и его термодинамическую устойчивость.
Важнейшим поверхностным свойством в растворах ПАВ является поверхностное натяжение а (см. рис. 2.3), а к числу объемных свойств следует отнести осмотическое давление п (см. рис. 9.4) и молярную электропроводностьЯ*, которая характеризует способность раствора, содержащего ионы, проводить электрический ток. На рис. 21.2 показаны изменения поверхностного натяжения ош (кривая 2), осмотического давления п (кривая 3) и молярной электропроводности X (кривая 4) в зависимости от концентрации раствора додецилсульфата натрия, который диссоциирует согласно уравнению (21.3). Область, в которой прекращается снижение поверхностного натяжения растворов коллоидных ПАВ и называют критической концентрацией мицеллообразования. (ККМ). Осмотическое давление п (кривая 3) сначала в соответствии с формулой (9.11) по мере увеличения концентрации ПАВ растет. В области ККМ этот рост прекращается, что связано с обра-
Математически ККМ можно определить как точку перегиба на кривых «свойство растворов коллоидных ПАВ — концентрация» (см. рис. 21.2), когда вторая производная этого свойства становится равной нулю, т.е. cPN/dc2 = 0. Мицеллообразование следует рассматривать как процесс, аналогичный фазовому переходу от истинного раствора ПАВ к ассоциированному состоянию в мицеллах; при этом мицеллообразование происходит самопроизвольно. Концентрация ПАВ в мицеллярной форме значительно, на несколько порядков, превышает концентрацию ПАВ в растворе. Мицеллы дают возможность получать растворы коллоидных ПАВ с большим содержанием растворенного вещества по сравнению с истинными растворами. Кроме того, мицеллы являются своеобразным хранилищем ПАВ. Равновесие между различным состоянием ПАВ в растворе (см. рис. 21.1) подвижное, и по мере израсходования ПАВ, например при увеличении поверхности раздела фаз, часть молекул ПАВ в растворе пополняется за счет мицелл.
ККМ — это важнейшее и отличительное свойство коллоидных ПАВ. ККМ соответствует концентрации ПАВ, при которой в растворе возникают мицеллы, находящиеся в термодинамическом равновесии с молекулами (ионами) ПАВ. В области ККМ резко изменяются поверхностные и объемные свойства растворов. ККМ выражают в молях на литр или в процентах растворенного вещества. Для стеарата кальция при 323 К ККМ равна 510"4 моль/л, а для эфиров сахарозы (0,51,0)10~5 моль/л. Значения ККМ невысокие, достаточно небольшого количества ПАВ, чтобы проявились объемные свойства их растворов, Еще раз подчеркнем, что не все ПАВ в состоянии образовывать мицеллы. Необходимым условием мицеллообразования являются наличие полярной группы в молекуле ПАВ (см. рис. 5.2) и достаточно большая длина углеводородного радикала. Мицеллы образуются и в неводных растворах ПАВ. Ориентация молекул ПАВ в неполярных растворителях противоположна их ориентации в воде, т.е. гидрофобный радикал обращен к углеводородной жидкости. Рис. 21.2. Изменение свойств раствора (N по оси ординат) Додеци л сульфата натрия в зависимости от концентрации: 1 — моющее действие; 2 — поверхностное натяжение; 3 — осмотическое давление для растворенных ПАВ; 4 — молярная электропроводность ККМ проявляется в некотором интервале концентрации ПАВ (см. рис. 21.2). С ростом концентрации ПАВ могут исходить два процесса: увеличение числа сферических мицелл и изменение их формы. Сферические мицеллы теряют правильную форму и могут превращаться в пластинчатые. Таким образом, в области ККМ происходит наиболее значительное изменение объемных и поверхностных свойств растворов коллоидных ПАВ, а на кривых, характеризующих эти свойства, появляются перегибы (см. рис. 21.2). Объемные свойства коллоидных ПАВ проявляются в таких процессах, как солюбилизация, образование пен, эмульсий и суспензий. Наиболее интересным и специфическим из этих свойств является солюбилизация. Солюбылизацией называют растворение в растворах коллоидных ПАВ тех веществ, которые в данной жидкости обычно нерастворимы. Например, в результате солюбилизации в водных растворах ПАВ растворяются углеводородные жидкости, в частности бензин и керосин, а также жиры, которые в воде не растворяются. Солюбилизация связана с проникновением в мицеллы веществ, которые называют солюбилизатами. Механизм солюбилизации для различной природы солюбилизатов можно пояснить при помощи рис. 21.3. При солюбилизации происходит внедрение неполярных веществ (бензола, гексана, бензина и др.) в мицеллу. Если солюбилизат содержит полярную и неполярную группы, то он располагается в мицелле углеводородным концом внутрь, а полярная группа обращена наружу. В отношении солюбилизатов, содержащих несколько полярных групп, наиболее вероятна адсорбция на наружном слое поверхности мицелл.
Солюбилизация начинается тогда, когда концентрация ПАВ достигает ККМ.При концентрации ПАВ выше ККМ число мицелл увеличивается, и солюбилизация идет более интенсивно. Солюбилизирующая способность коллоидных ПАВ растет в пределах данного гомологического ряда по мере увеличения числа
углеводородных радикалов. Ионогенные ПАВ обладают большей солюбилизирующей способностью по сравнению с неино-генными. Особенно значительна солюбилизирующая способность биологически активных коллоидных ПАВ — хелата и дезоксихе-лата натрия. Солюбилизация и эмульгирование (см. параграф 15.4) являются первичными процессами усвоения жиров; в результате солюбилизации жиры растворяются в воде, а затем усваиваются организмом. Таким образом, объемные свойства растворов коллоидных ПАВ обязаны образованию мицелл.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 721; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.184.214 (0.027 с.) |
 * Применявшийся ранее термин «поликоллоиды» не в полной мере отражает существо процессов, происходящих в растворах этой группы ПАВ.
* Применявшийся ранее термин «поликоллоиды» не в полной мере отражает существо процессов, происходящих в растворах этой группы ПАВ.


 * Электропроводность раствора, содержащего один моль вещества и заключенного между электродами площадью в 1 м2, которые расноложены на расстоянии 1 м друг от друга.
* Электропроводность раствора, содержащего один моль вещества и заключенного между электродами площадью в 1 м2, которые расноложены на расстоянии 1 м друг от друга.



 зованием мицелл, размер которых значительно превышает размер молекул растворенных ПАВ. Прекращение роста осмотического давления в связи с увеличением размеров частиц непосредственно следует из формулы (9.13), согласно которой осмотическое давление обратно пропорционально кубу радиуса частиц г3. Связывание молекул ПАВ в мицеллы снижает их концентрацию в растворе как электролитов. Этим обстоятельствоми объясняется снижение молярной электропроводности в области ККМ (кривая 4).
зованием мицелл, размер которых значительно превышает размер молекул растворенных ПАВ. Прекращение роста осмотического давления в связи с увеличением размеров частиц непосредственно следует из формулы (9.13), согласно которой осмотическое давление обратно пропорционально кубу радиуса частиц г3. Связывание молекул ПАВ в мицеллы снижает их концентрацию в растворе как электролитов. Этим обстоятельствоми объясняется снижение молярной электропроводности в области ККМ (кривая 4).






