
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение теоретически необходимого количества воздуха
Горение – это реакция соединения горючих элементов топлива (H, C, S) с окислителем. Горение называют химически полным, если в результате процесса горения образуются продукты полного окисления.
При отсутствии избыточного кислорода состав продуктов сгорания при полном горении выражается уравнением:
Если в процессе горения образуются газообразные продукты неполного окисления (CO, H Теоретически необходимым количеством воздуха (V0) называется объем воздуха при нормальных условиях, который требуется для полного сгорания единицы топлива Для определения данной величины V0 запишем стехиометрические химические реакции горения. Для твердого и жидкого топлива, состав которых выражается в процентах веса, эти реакции (стехиометрические соотношения) имеют вид:
12кг+32кг=44кг 4кг+32кг=36кг 32кг+32кг=64кг или 1кг+ Согласно закону сохранения масс (где 12, 32, 44 и т.д. – атомарные и молекулярные веса реагирующих веществ и продуктов реакций. На основании вышеприведенных реакций и учитывая, что воздух содержит 21% кислорода по объёму, получим:
Для газообразного топлива состав выражается в процентах объема. Запишем стехиометрические соотношения процесса окисления горючих компонентов газообразного топлива, учитывая, что 1 кмоль любого газа при нормальных условиях занимает один и тот же объем (22,41 нм3/кмоль). Закона сохранения объёма не существует.
2H 2м 1м3 0.5м3 1м3 1м3 2м3 1м3
2H 2м3 3м3 2м3 2м3 1м3 1.5м3 1м3 1м3 Таким образом, теоретически необходимый объем воздуха для сжигания газ. топлива
где H Коэффициент избытка воздуха Поскольку процесс перемешивания топлива с воздухом неидеален, то для обеспечения полного сгорания топлива, необходимо подавать воздуха в топку больше Коэффициентом избытка воздуха (α) называется отношение действительного количества воздуха (
- для твердого топлива;
Определение объёмов продуктов сгорания
При полном сгорании топлива и α=1 объем газа
Для определения объема указанных составляющих, снова используем вышеприведенные реакции горения. При сжигании твердого и жидкого топлива (состав в % веса) Объем трехатомных газов
Объем азота состоит из азота воздуха (
Объем водяных паров. Водяные пары в продуктах сгорания появляются за счет: окисления водорода (
При сжигании топлива с α>1 объем газов (
При химически неполном горении и α>1 объем газов равен:
При этом объем сухих газов:
При сжигании газообразного топлива ( состав топлива в % объема ), из вышеприведенных реакций окисления горючих газов, имеем
При изменении балласта топлива ( Объемы сухих газов
Для твердого и жидкого топлива:
Для газового топлива:
Из данных выражений можно получить, что
где
Контроль избытка и присосов воздуха Эффективность процесса горения и экономичность работы парового котла в значительной степени определяется величиной коэффициента избытка воздуха в топке (αт) и присосов воздуха по газовому тракту (∆α). Снижение коэффициента избытка воздуха в топке и присосов воздуха ведет к снижению расхода электроэнергии на тягу и дутье. Снижается потеря тепла с уходящими газами, но чрезмерное снижение коэффициента избытка воздуха в топке (αт) может привести к потерям, связанным с недожогом топлива. Поэтому контроль коэффициента избытка воздуха в топке (αт) и присосов в газоходы (∆α) имеет важное значение при эксплуатации котла
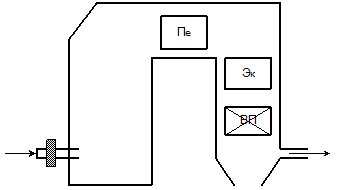
Рассмотрим газовый тракт парового котла.
где
|
|||||||||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 351; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.119.148 (0.02 с.) |
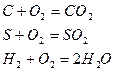
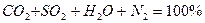
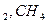 и др.), то горение называется химически неполным.
и др.), то горение называется химически неполным.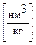 или
или 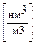 .
.
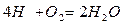
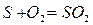
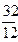 кг=
кг= 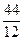 кг 1кг+8кг=9кг 1кг+1кг=2кг
кг 1кг+8кг=9кг 1кг+1кг=2кг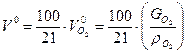 , где
, где 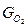
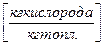 - вес О2 для окисления 1кг топлива
- вес О2 для окисления 1кг топлива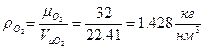 - плотность кислорода при нормальных условиях (
- плотность кислорода при нормальных условиях (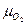 - молекулярный вес О2,
- молекулярный вес О2, 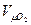 - объём 1 кмоля идеального газа при н.у.)
- объём 1 кмоля идеального газа при н.у.)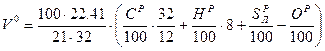
 .
.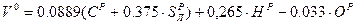

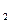 +O
+O 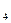 +2O
+2O  1м3 2м3 2м3 1м3 2м3 1м3 2м3 1м3 2м3
1м3 2м3 2м3 1м3 2м3 1м3 2м3 1м3 2м3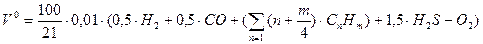
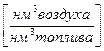 ,
,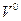 .
.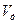 ) к теоретически необходимому (
) к теоретически необходимому ( 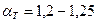
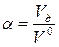
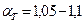 - для газа и мазута (топка под разрежением);
- для газа и мазута (топка под разрежением);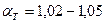 - для газа и мазута (топка “под наддувом”).
- для газа и мазута (топка “под наддувом”).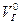 состоит из объема трехатомных газов, объема азота и объема водяных паров.
состоит из объема трехатомных газов, объема азота и объема водяных паров.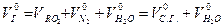 , где
, где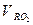 =
= 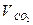 +
+ 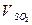 - объем трехатомных газов
- объем трехатомных газов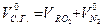 - объем сухих газов
- объем сухих газов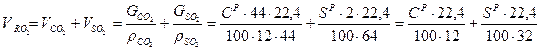
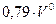 ) и азота топлива (
) и азота топлива (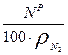 ), где
), где 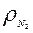 = 28/22,41 - плотность азота.
= 28/22,41 - плотность азота.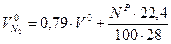
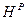 ), влаги топлива (
), влаги топлива (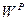 ), влагосодержания воздуха (
), влагосодержания воздуха (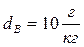 или 13
или 13 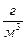 ) и пара при распыле мазута в паровых мазутных форсунках(
) и пара при распыле мазута в паровых мазутных форсунках(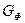 , кг/кг).
, кг/кг).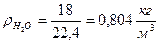 - плотность водяных паров.
- плотность водяных паров.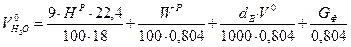
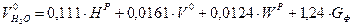
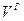 ) будет равен:
) будет равен: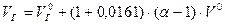
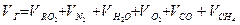 и т.д.
и т.д.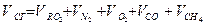 и т.д.
и т.д.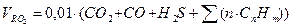
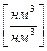
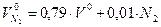
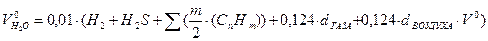
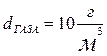
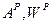 ) объемы теоретически необходимого количества воздуха
) объемы теоретически необходимого количества воздуха 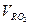 ,
, 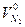 ,
,  пересчитываются по тем же коэффициентам пересчета, что и состав топлива.
пересчитываются по тем же коэффициентам пересчета, что и состав топлива.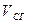 можно определить, зная состав топлива и объемы составляющих продукты сгорания, из соотношения:
можно определить, зная состав топлива и объемы составляющих продукты сгорания, из соотношения: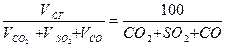 (1)
(1)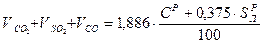 (2)
(2)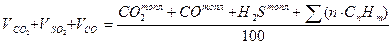 (3)
(3)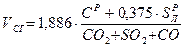 (4)
(4)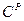 и
и 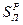 - содержание компонентов в топливе.
- содержание компонентов в топливе.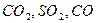 - процентное содержание этих газов в продуктах сгорания.
- процентное содержание этих газов в продуктах сгорания.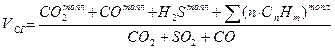 (5)
(5)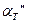
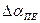
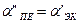


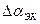
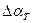


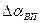

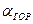
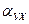
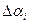 - присос воздуха в i-ый газоход.
- присос воздуха в i-ый газоход.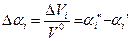 ,
, ,
, 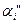 -коэффициенты избытка воздуха до и за i-ым газоходом
-коэффициенты избытка воздуха до и за i-ым газоходом ;
;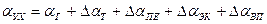 .
.


