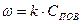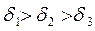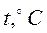Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Классификация котлоагрегатовСтр 1 из 15Следующая ⇒
Энергетические ресурсы
Энергетические ресурсы – это материальные объекты, часть энергии которых может использоваться человеком для получения нужных энергетических эффектов. 1) возобновляемые (непрерывно восстанавливаются природой – солнце, ветер, реки, моря, геотермальные источники) 2) невозобновляемые (ранее накопленные в природе – уголь, сланец, торф, продукты переработки нефти, природный и попутный газ, урановая руда) Основной источник энергии – органическое (Q=8 – 45 МДж/кг) и ядерное (U235, Pu239) топливо.
Виды и классификация ТЭС
ТЭС делятся на конденсационные (КЭС) и теплоэлектроцентрали (ТЭЦ). КЭС (ГРЭС) предназначены для выработки электроэнергии. Располагаются, в основном, в местах добычи или удобной транспортировки топлива, вблизи крупных потребителей электроэнергии, которая поступает в электрические сети. ТЭЦ служат для покрытия тепловых нагрузок в виде горячей воды и пара. Теплоэлектроцентрали размещаются вблизи крупных потребителей тепла. Электроэнергия подается в электросети, тепло – в теплосети. Основными тепловыми агрегатами паротурбинной ТЭС являются паровой котел и паровая турбина. Процесс в паротурбинной установке (ПТУ) - цикл Ренкина
a – b сжатие в питательном насосе; b – c подогрев в экономайзере котла; c – d испарение в парообразующих поверхностях котла; d – e перегрев в пароперегревателе котла; e – f расширение пара в турбине; f – a конденсация пара в конденсаторе. Для повышения экономичности цикла используют: а) регенеративный подогрев конденсата отборным паром турбины; б) вторичный перегрев пара, отработавшего в ЦВД турбины – газовый перегрев в ПК.
Рис. 2. Принципиальная схема КЭС.
1. Паровой котел с промежуточным пароперегревателем. 2. Цилиндр высокого давления. 3. Цилиндр среднего и низкого давления. 4. Электрический генератор. 5. Конденсатор. 6. Конденсатный насос. 7. Подогреватель низкого давления. 8. Деаэратор. 9. Питательный насос. 10. Подогреватель высокого давления. 11. Цех химводоочистки. Пароводяной цикл КЭС замкнут.
Рис. 3. Вид на машинный зал Пермской ГРЭС Бл. (800 Мвт).
Рис. 4. Принципиальная схема ТЭЦ 1. Паровой котел. 2. Паровая турбина. 4. Электрический генератор. 5. Конденсатор. 6. Конденсатный насос. 7. Подогреватель низкого давления. 8. Деаэратор. 9. Питательный насос. 10. Подогреватели высокого давления. 11. Цех химводоочистки. 12. Тепловой потребитель.
Виды и классификация АЭС
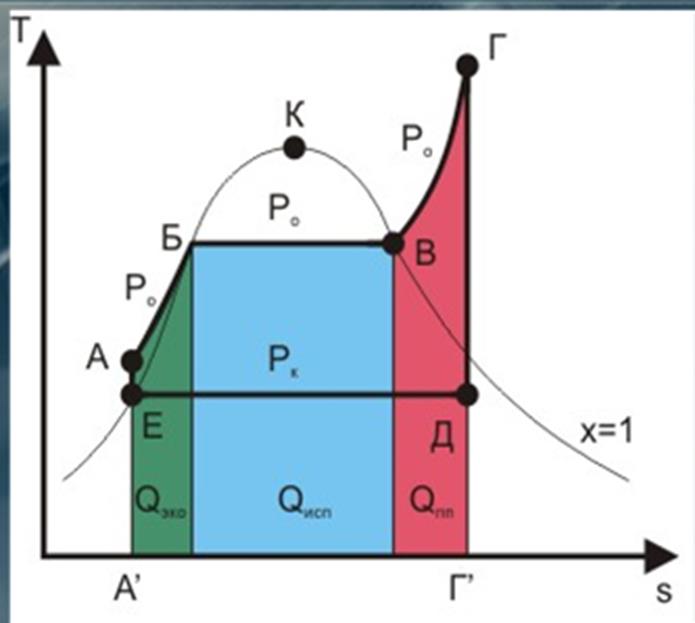
Рис.5 Одноконтурная АЭС
В двухконтурной схеме (Рис.6) контуры рабочего тела и теплоносителя разделены.
7. Циркуляционный насос P1>P2 P1=16,5 МПа P2=6 МПа t1=345 оС t2=275 оС ∆t= t2- t1 Для обеспечения надежного отвода тепла желательно предотвратить закипание воды в реакторе, поэтому P1>P2.
(Рис.6. Двухконтурная схема
Рис. 6.а Трёхконтурная схема
лекция№2
Преимущества тракта под наддувом: · отсутствие присосов холодного воздуха в газоходах котла и, как следствие, сокращение объема продуктов сгорания; · температура газов в топке выше, более полное сгорание топлива и меньше потеря тепла с уходящими газами; · упрощение схемы, снижение капитальных затрат и затрат на собственные нужды. В воздухоподогревателях котлов обоих типов наблюдается переток воздуха с воздушной стороны на газовую, поскольку давление воздуха выше, чем давление газовой смеси.
Принципиальные схемы котлов
Рис. 12 Барабанный котёл высокого, сверхвысокого давления
Рис. 13 Принципиальная схема прямоточного котла СКД
Топливо
Органическое топливо – это вещество, способное активно вступать в реакцию с кислородом воздуха, обладающее значительным удельным тепловыделением, происходящим при высокой температуре продуктов горения.
В энергетике используются твердое, жидкое и газообразное топлива. Твердое топливо имеет растительное происхождение (за исключением веществ животного происхождения). Превращение исходного органического вещества в топливо происходит в течение долгого времени под воздействием большого количества факторов (температура, давление, влияние микроорганизмов и т.д.). Так как условия превращения различны, то различна и степень превращения вещества в топливо, степень углефикации. (у глефикация – процесс насыщения вещества углеродом за счет освобождения кислорода и азота). Зрелость топлива не всегда соответствует его геологическому возрасту. Важнейшими характеристиками твердого топлива являются: влажность W, величина которой может изменяться (5÷60%), зольность (содержание негорючей минеральной части А=5÷50%), выход летучих на горючую массу V Естественным жидким топливом является сырая нефть – это смесь органических соединений (главным образом углеводороды). В состав нефти входят соединения O В энергетике используется мазут М40, М100, М200, где 40, 100, 200 показатель величины условной вязкости при температуре 500С. Преимущества мазута перед твердым топливом: 1. высокая теплота сгорания; 2. легко транспортируется по трубопроводу; 3. легко воспламеняется и имеет устойчивое горение; 4. не требует устройств для удаления золы и шлака. Недостатки: 1. коррозия и загрязнение поверхностей нагрева, особенно при сжигании мазута с высоким содержанием серы; 2. наличие вредных выбросов в атмосферу в виде: SO Газообразное топливо представляет собой смесь горючих и негорючих газов, содержащих небольшое количество примесей в виде водяных паров и пыли. Естественные природные газы имеют биологическое происхождение и являются продуктами разложения. Основной составляющей (80÷95%) природного газа является метан CH Газовое топливо обладает теми же преимуществами что и мазут, но выраженными в большей степени. Его применение дает минимальную коррозию поверхностей нагрева и минимальное загрязнение окружающей среды. Состав топлива Твердое и жидкое органическое топливо состоит из сложных химических соединений, содержащих углерод, водород, серу, кислород, азот, влагу и минеральную часть. · C, H, Sл – горючая часть; · O, N – внутренний балласт; · W, A – внешний балласт. Газообразное топливо представляет собой смесь горючих и негорючих газов с небольшой примесью пыли. Его состав: · CH · Один килограмм водорода выделяет при сгорании тепла в несколько раз больше, чем углерод. Один килограмм серы выделяет при сгорании тепла в 3,5 раза меньше, чем углерод. Сера, содержащаяся в твердом топливе делится на: · S · Sк –колчеданная (входит в состав колчедана или пирита FeS2);
· Sл = S По содержанию серы различают следующие виды мазута: · S ≤0,5 мазут малосернистый; · S ≥1,7 мазут высокосернистый; · 0,5<S<1,7 мазут сернистый. Жидкое и твердое топливо имеет сложный молекулярный состав, поэтому их состав выражается в процентах веса элементов. Топливо, на складе станции, называется рабочим. Состав топлива на рабочую массу записывается в следующем виде: C
Wа =Wр - Wвн Рис. 14 Схема элементарного состава топлива
Органическая масса
C Горючая масса W=A=0
C
C
C
Пересчет состояния топлива с одной массы на другую ведется с помощью коэффициента пересчета Таблица 1. Коэффициенты пересчета на различные массы топлива
При хранении и транспортировке топлива его зольность и влагосодержание могут изменяться.
Теплота сгорания Теплотой сгорания называется количество теплоты, выделившейся при полном сгорании единицы массы или объема топлива
r = 600 Количество водяных паров получающихся при сжигании 1кг топлива
Wp/100-влага топлива (делим на 100, чтобы перейти от % к кг); (запишем стехиометрическую реакцию окисления атомарного водорода)
с учётом молекулярных весов (закон сохранения масс) 4кг+32кг=36кг 1кг+ 8кг = 9кг 9Нр./100-вес водяных паров, образующиеся при окислении 1 кг водорода топлива.
При изменении внешнего балласта топлива пересчет у низшей теплоты сгорания проводится следующим образом:
При изменении балласта топлива Пересчет низшей теплоты сгорания ( 1. при изменении зольности (
2. при изменении влажности топлива пересчет низшей теплоты ведется через высшую теплоту сгорания, которая пересчитывается аналогично составу топлива:
Для твердого и жидкого топлив теплота сгорания может быть примерно рассчитана по полуэмпирической формуле Менделеева.
Теплота сгорания природного газа может быть рассчитана следующим образом:
Теплота сгорания топлива определяется на калориметре.
лекция№4 Зольность Ископаемое твердое топливо содержит негорючие вещества, состоящие главным образом из: глины ( Важнейшей эксплуатационной характеристикой золы является ее плавкость. Плавкость определяется путем помещения образца в виде трехгранной пирамиды в печь.
Рис. 15 Температурные характеристики золы
t t t При организации жидкого шлакоудаления температура газов в нижней части топки должна быть на 100° выше, чем t Влажность. Различают четыре вида влажности: 1. механически удерживаемая влага; 2. капиллярная влага, находящаяся в капиллярах или порах; 3. коллоидная влага; входит в состав коллоидов, находящихся в топливе; 4. кристаллогидратная влага. Выход летучих При нагревании твердого топлива без доступа воздуха, топливо разделяется на газообразную и парообразную части, а также твердый остаток (кокс). Под летучими понимается выход газов без водяных паров, выраженных в процентах массы топлива. Состав летучих: · СО, СnHm, H2 – горючая часть; · O2, N2 – негорючая часть. Наибольшая часть летучих выделяется при нагреве топлива до 850°С. Полное выделение при 1100-1200°С. Степень углефикации топлива и выход летучих взаимосвязаны. Топливо с малой степенью углефикации имеет большой выход летучих, но в их состав входит много кислорода, поэтому удельная теплота сгорания небольшая. Древесина Антрацит Влияние выхода горючих летучих особенно велико в начальной стадии горения, т.е. при воспламени топлива. Топливо с большим выходом летучих называется высокореакционным и наоборот с малым выходом летучих – низкореакционным. Таким образом, под реакционной способностью топлива, понимается способность топлива воспламеняться.
Данная величина положена в основу классификации твердых топлив: · Д – длиннопламенный · Г – газовый · ГЖ – газовый жирный · КЖ – коксовый жирный · ОС – отощенный спекающийся · СС – слабоспекающийся · Т – тощий · А – антрацит Классификация по крупности (размеру кусков δ). · П – плиты ( · К – крупный (δ=100-50 мм) · О – орех (δ=50-25 мм) · М – мелкий (δ=25-13 мм) · С – семечка (δ=13-6 мм) · Ш – штыб (δ=6-0 мм) · Р – рядовой (без ограничения размера). Таким образом, имеем следующие марки каменных углей: АШ, ТСШ, ДР, ГМС и т.д.
К бурым относятся угли с высоким выходом летучих Классификация бурых углей проводится по общей рабочей влаге ( · Б1 - · Б2 - · Б3 - Сланцы занимают среди твердого топлива особое место. Это минерал, пропитанный органическими соединениями сходными по составу с нефтью. Его характеристики:
Характеристики жидкого топлива (мазута) Свойства мазута разделяют на управляемые и неуправляемые: 1. управляемые – те, которые могут изменятся в процессе подготовки топлива: вязкость, содержание влаги, плотность, содержание серы. 2. неуправляемые – те, которые практически не изменяются в процессе подготовки: зольность, температура застывания, температура вспышки, температура воспламенения. Классификация ведется по условной вязкости и содержанию серы. В энергетике вязкость мазута принято измерять в градусах условной вязкости.
Относительная плотность мазута – это отношение плотности мазута при данной температуре к плотности воды при температуре 4°С. Сернистость, зольность, температура вспышки, температура воспламенения, температура застывания.
Приведенные характеристики под приведенными характеристиками понимают отношение характеристики топлива в процентах к 1000 ккал (в системе МКГСС) или к 4190 кДж (в системе СИ) его низшей теплоты сгорания.
. В качестве условного принимают топливо с теплотой сгорания В соответствии с этим каждое топливо имеет тепловой эквивалент ЛЕКЦИЯ №5 Элементы теории горения Под горением понимают процесс химического взаимодействия топлива и окислителя, при интенсивном выделении тепла, скачкообразном росте температур, концентрации продуктов горения и снижении концентрации окислителя. При горении происходит преобразование химической энергии топлива в тепловую энергию, идущую на нагрев продуктов сгорания. Химические реакции, идущие с выделением тепла, называются экзотермическими.
Химические реакции, идущие с поглощением тепла, называются эндотермическими.
Существуют и другие виды реакций: гомогенные, гетерогенные. Интенсивность горения характеризуется скоростью химической реакции. Под скоростью гомогенной химической реакции понимают массовое количество вещества, которое реагирует в единицу объема, в единицу времени.
Считают, что скорость гомогенной реакции подчиняется закону действующих масс, т.е. пропорциональна произведению реагирующих веществ или масс.
m и n – число молей реагирующего вещества, k – постоянная скорости горения. Например:
При данной температуре концентрация пропорциональна парциальному давлению соответствующего газа.
При сжигании твердого топлива парциальное давление паров продуктов газификации, а следовательно и их концентрации есть величины постоянные при данной температуре.
Константа скорости горения определяется по закону Аррениуса: E –энергия активации; R –газовая постоянная; T–температура процесса в градусах °К. Это выражение показывает, что в реакции участвуют не все молекулы топлива, а только молекулы, обладающие энергией активации, т.е. энергией, достаточной для разрушения внутренних связей.
Для того, чтобы сообщить топливу достаточное количество энергии его необходимо подогреть. . Рис. 16 Влияние температуры на величину константу скорости горения
Таким образом, k показывает долю молекул, участвующих в процессе горения. k Горение твердого топлива Различают два периода: 1. сушка при температуре около 100°С. Время сушки зависит от влажности, от размеров кусков, от условий теплообмена. 2. горение состоящее из следующих стадий: а) выход летучих и образование нелетучего остатка; б) горение летучих; в) горение нелетучего коксового остатка. Примерно 90% времени занимает горение коксового остатка (С). Учитывают также, что при этом выделяется основное количество тепла. Горение твердого топлива в основном определяется механизмом и кинетикой горения углерода.
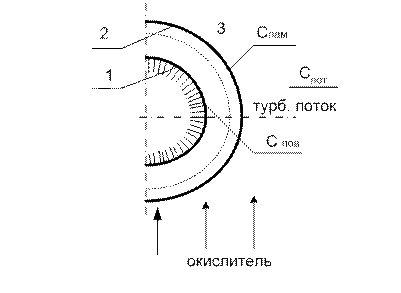
Рис. 17 Схема горения коксовой частицы
1. поверхность коксовой частицы 2. граница ламинарного слоя 3. турбулентный поток. Данное горение протекает на поверхности и относится к гетерогенным реакциям: в этом процессе подводится кислород, который реагирует с частицами твердого топлива.
Скорость химической реакции зависит от скорости подвода кислорода к поверхности реагирования и от кинетики химической реакции. Количество O a) Поверхность ламинарного слоя
b) Поверхность частиц:
D – коэффициент молекулярной диффузии. Совместное решение уравнений (4) и (5):
Таким образом, количество кислорода, подводимого к поверхности, является функцией: При установившемся процессе горения скорость процесса равна скорости подвода кислорода:
С другой стороны, ранее получено, что скорость гетерогенного горения равна:
Совместное решение уравнений (8) и (9) дает выражение для скорости горения:
где
В зависимости от соотношения этих сопротивлений, на которые влияют от температура процесса, диаметр частиц, скорость обтекания и т.д., различают кинетическую и диффузионную области горения. Рассмотрим зависимость скорости процесса горения от температуры процесса и диаметра частиц (δ).
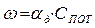
Рис. 18 Области горения При низких температурах (t<1000°С), скорость процесса горения ограничивается кинетическим или химическим сопротивлением процесса горения. Определяющим фактором скорости процесса является температура. Область горения называется кинетической – (II). В области (t>1400°C) скорость реакции горения ограничивается скоростью подвода кислорода. Данная область называется диффузионной (I) В диапазоне температур 1000-14000С - область III на скорость влияют оба фактора (температура процесса горения и скорость подвода кислорода). Данная область называется промежуточной –(III).
Горение жидкого топлива При горении жидкого топлива температура воспламенения и горения выше температуры кипения отдельных его фракций, поэтому жидкое топливо вначале испаряется, а затем сгорание паров смеси с воздухом происходит при одном агрегатном состоянии. Скорость горения определяется скоростью испарения капель мазута, которая зависит от качества распыла и от скорости подвода кислорода. Снижение диаметра капель ведет к увеличению поверхности испарения, повышению температуры процесса, усилению теплообмена. Горение паров жидкого топлива происходит в диффузионной области. При недостатке кислорода наблюдается термический крекинг, т.е. образование тяжелых углеводородов в виде мельчайших частиц углерода (сажи), что снижает полноту сгорания топлива. Условия повышения интенсивности сжигания жидкого топлива: 1. предварительный подогрев; 2. тонкое распыливание; 3. подвод воздуха в ядро факела; 4. хорошие условия перемешивания; 5. поддерживание температуры в ядре факела выше 550°С. Горение газового топлива Установлено, что скорость протекания горения газового топлива значительно выше, чем по закону действующих масс и закону Аррениуса. В действительности реакции протекают не непосредственно между исходными веществами, а через ряд промежуточных стадий, в которых участвуют и исходные молекулы и активные осколки в виде O, H, OH, при этом энергия активации промежуточных стадий значительно ниже, а скорость протекания реакций выше. Началу реакции предшествует период индукции или период зарождения активных частиц за счет разрушения части исходных молекул. Горение газового топлива происходит по законам цепных разветвленных реакций (ЦРР), открытых академиком Семёновым. Согласно данной теории, превращение исходных веществ в конечные происходит через систему промежуточных звеньев, включающих: 1. зарождение цепи;
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-10; просмотров: 349; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.129.211.87 (0.302 с.) |





 6. Парогенератор
6. Парогенератор







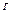 (4÷80%).
(4÷80%). , N
, N 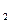 , SO
, SO 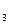 , и окислов азота.
, и окислов азота. . Искусственные и попутные газы в большей степени засорены негорючими примесями и обладают меньшей теплотой сгорания по сравнению с естественными.
. Искусственные и попутные газы в большей степени засорены негорючими примесями и обладают меньшей теплотой сгорания по сравнению с естественными.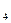 = 80÷95%,
= 80÷95%, 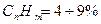 , H
, H 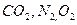 - негорючая часть.
- негорючая часть.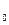 -органическую (входит в состав органических соединений);
-органическую (входит в состав органических соединений);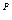 +H
+H  +N
+N  Аналитическая масса – топливо, доведенное до воздушно-сухого состояния.
Аналитическая масса – топливо, доведенное до воздушно-сухого состояния.

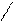 W Wa O N H C S
W Wa O N H C S  C
C  +H
+H 
 +H
+H 
 +H
+H 

 .
.


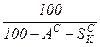



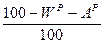
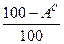





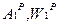 →
→ 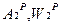 коэффициент пересчета при этом:
коэффициент пересчета при этом: 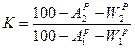 .
.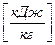 ,
, 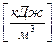 . Различают высшую и низшую теплоту сгорания. Высшей теплотой сгорания называется количество тепла, выделяемое при полном сгорании единицы топлива с учетом теплоты конденсации, образующейся при горении водяных паров. Низшая теплота сгорания – это количество тепла без учета теплоты конденсации.
. Различают высшую и низшую теплоту сгорания. Высшей теплотой сгорания называется количество тепла, выделяемое при полном сгорании единицы топлива с учетом теплоты конденсации, образующейся при горении водяных паров. Низшая теплота сгорания – это количество тепла без учета теплоты конденсации.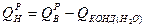
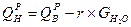 , где
, где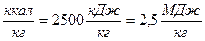 - скрытая теплота парообразования.
- скрытая теплота парообразования.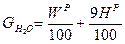
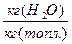 , где:
, где: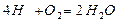
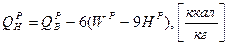
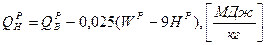
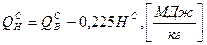
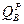 ) пересчитывается, как и состав топлива -
) пересчитывается, как и состав топлива - 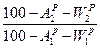
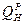 ) при изменении внешнего балласта топлива
) при изменении внешнего балласта топлива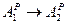 ) пересчет ведется аналогично составу топлива:
) пересчет ведется аналогично составу топлива:
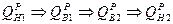
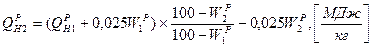
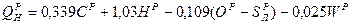 , Мдж/кг.
, Мдж/кг.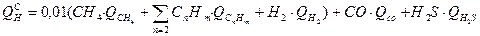
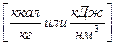
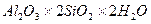 ), силикатов (SiO
), силикатов (SiO 

 13мм
13мм
 6мм t
6мм t 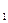 t
t 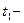 температура начала деформации (1000÷1200°C)-оплавляется вершина пирамиды;
температура начала деформации (1000÷1200°C)-оплавляется вершина пирамиды;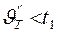 (
(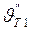 - температура газов за топкой);
- температура газов за топкой);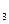 - температура жидко-плавкого состояния (1200÷1500°C);
- температура жидко-плавкого состояния (1200÷1500°C);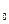 - температура истинно жидкого состояния (при которой шлак подчиняется законам движения жидкости).
- температура истинно жидкого состояния (при которой шлак подчиняется законам движения жидкости).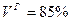
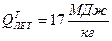
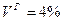
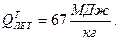
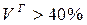
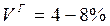 .
.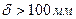 )
)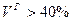 с теплотой сгорания влажной беззольной массы Qн <5700
с теплотой сгорания влажной беззольной массы Qн <5700 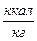 . Эти угли отличаются большой пористостью, высокой гигроскопической влажностью и большой общей влажностью с пониженным содержанием С и повышенным содержанием О. Удельная теплота сгорания
. Эти угли отличаются большой пористостью, высокой гигроскопической влажностью и большой общей влажностью с пониженным содержанием С и повышенным содержанием О. Удельная теплота сгорания 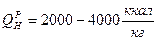 . Они обладают малой механической прочностью, плохо выдерживают длительное хранение, превращаются в мелочь и самовозгораются из-за самоокисления.
. Они обладают малой механической прочностью, плохо выдерживают длительное хранение, превращаются в мелочь и самовозгораются из-за самоокисления.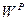 )
)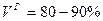
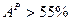
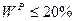
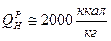
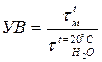
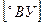 , где
, где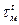 -время истечения мазута при температуре t через калиброванное отверстие вязкозиметра
-время истечения мазута при температуре t через калиброванное отверстие вязкозиметра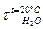 - время истечения дистиллированной воды при t=20оС через то же отверстие (постоянная вязкозиметра).
- время истечения дистиллированной воды при t=20оС через то же отверстие (постоянная вязкозиметра).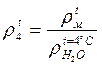 .1<или>1
.1<или>1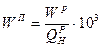
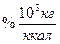 ;
;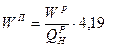
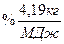 ;
;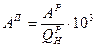 (МКГСС);
(МКГСС);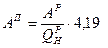 (СИ). Условное топливо
(СИ). Условное топливо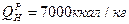 или 29,33 МДж/кг.
или 29,33 МДж/кг.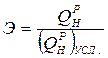 >или<1.
>или<1.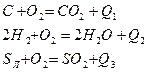
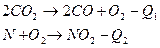
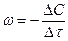
 , где (1)
, где (1)
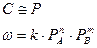 (2)
(2)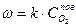 (3)
(3)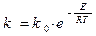
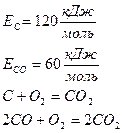

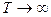
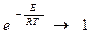
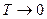
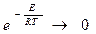
 , А – коэф. турбулентной диффузии. (4)
, А – коэф. турбулентной диффузии. (4) ,
, 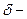 толщина ламинарного слоя. (5)
толщина ламинарного слоя. (5)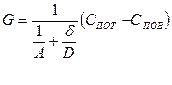 (6)
(6)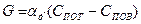
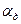 - константа скорости диффузии.
- константа скорости диффузии.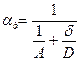
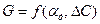 . В свою очередь
. В свою очередь 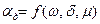 .
.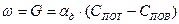 (8)
(8)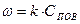 (9)
(9)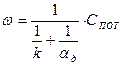 (10)
(10)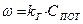 (11)
(11)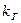 - приведенная константа скорости горения, представляющая из себя единицу, деленную на сопротивление процессу горения.
- приведенная константа скорости горения, представляющая из себя единицу, деленную на сопротивление процессу горения.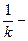 химическое (кинетическое) сопротивление;
химическое (кинетическое) сопротивление;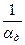 - диффузионное сопротивление;
- диффузионное сопротивление;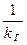 - общее сопротивление.
- общее сопротивление.