
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема 7. «Свойства растворов электролитов»
7.1 Содержание программы Теория электролитической диссоциации Аррениуса. Сильные электролиты. Коэффициент активности. Ионная сила раствора.Слабые электролиты. Степень и константа диссоциации. Закон разбавления Оствальда.Теория кислот и оснований. Уровень теоретической и практической подготовки Студент должен усвоить понятия:электролиты, сольватация, гидратация, диссоциация, константа и степень диссоциации; должен знать диссоциацию важнейших классов неорганических соединений. Студент должен уметь предсказывать силу основания и кислоты, пользоваться таблицами констант диссоциации электролитов, вычислять степень диссоциации, концентрацию электролита с учетом степени диссоциации. 7.2 Методические рекомендации к теме Вещества, распадающиеся в растворах или расплавах на ионы, называются электролитами. К ним относятся вода, соли, кислоты, основания. Растворы этих веществ сильно отклоняются от законов Рауля и Вант-Гоффа. Причиной этого является диссоциация электролитов на ионы. Процесс электролитической диссоциации обусловлен взаимодействием растворенных веществ с водой (или другим растворителем); образующиеся ионы - катионы и анионы - являются гидратированными, т.е. химически связанными с водой. Необходимо разобраться, как диссоциируют важнейшие электролиты. При диссоциации кислот всегда образуются ионы водорода H+ (точнее ионы гидроксония H3O+), которые обусловливают важнейшие свойства кислот: кислый вкус, изменение окраски индикаторов, взаимодействие с основаниями HNO3 ↔ H+ + NO3- Двух и многоосновные кислоты диссоциируют ступенчато, постепенно отщепляя ионы водорода. Например, в случае серной кислоты первая ступень H2SO4 ↔ H+ + НSO4−, вторая ступень HSО4- ↔ Н+ + SO42- При составлении уравнений диссоциации необходимо помнить, что сумма зарядов катионов равна общей сумме зарядов анионов! При диссоциации оснований всегда образуются гидроксид-ионы OH–, например NaOH ↔ Na+ + OH–. Двух и трехкислотные основания в водных растворах диссоциируют ступенчато, т.е. постепенно отщепляют гидроксид-ионы. Например, в случае гидроксида кальция Ca(OH)2 диссоциация протекает в две ступени: первая ступень Ca(OH)2 ↔ Ca(OH)+ + OH–, вторая ступень Ca(OH)+ ↔ Ca2+ + OH–. Существуют электролиты, которые могут диссоциировать, как по механизму кислот (с отцеплением ионов H+), так и по механизму оснований (отщепление ионов OH–). Они называются амфотерными электролитами или амфолитами. К амфотерным электролитам относится, например, вода H2O ↔ H+ + OH–, гидроксид цинка 2Н+ + ZnO22 - ↔ Zn(OH)2 ↔ Zn2+ + 2OH - как кислота как основание. При диссоциации средних солей образуются катионы металлов и анионы кислотных остатков, например Na2SO4 ↔ 2Na+ + SO42- Диссоциация кислых солей протекает ступенчато, как, например, в случае гидрокарбоната натрия: первая ступень NaHCO3 ↔ Na+ + HCO3- , вторая ступень НСО3- ↔ Н+ + СО32-. В результате образуется два типа катионов: катионы металла и ионы водорода. Также ступенчато диссоциируют основные соли, например, хлорид гидроксомагния: первая cтупень МgOHCI ↔ MgOH+ + CI- вторая ступень MgOH+ ↔ Mg2+ + OH- Таким образом, при диссоциации основных солей образуются два типа анионов: анионы кислотных остатков и гидроксид-ионы. По способности к диссоциации электролиты условно делятся: 1. Сильные электролиты - вещества, диссоциирующие при растворении полностью на ионы. В водных растворах сильными электролитами являются кислоты: азотная, серная, соляная, хлорная, бромоводородная, иодоводородная; щелочи: KOH, NaOH, LiOH, CsOH, RbOH, Ca(OH)2, Ba(OH)2, Sr(OH)2; хорошо растворимые соли. Концентрация ионов в растворе сильного электролита достаточно высока и между ними возникают силы взаимодействия. Для описания состояния ионов в растворе введено понятие активности а. Активность – это эффективная концентрация, в соответствии с которой ионы проявляют себя в физико-химических процессах. Связь между молярной концентрацией См и активностью а, выражается уравнением: а = См·f, где f – коэффициент активности иона. Для определения коэффициента активности ионов необходимо рассчитывать ионную силу растворов I. Ионная сила I – это полусумма произведений каждого вида ионов Сi на квадрат заряда иона данного вида z: I = 0,5(С1∙ z12 + С2∙ z22 +… + Cnzn2) = 0,5 ∑ Ci ∙ zi2 (40) В приложении 4 приводятся коэффициенты активности f ионов в зависимости от их заряда и ионной силы раствора. Приближенно f иона можно вычислить также по формуле:
7.4 Тесты для самоконтроля Тест 1 1. Какие из указанных веществ являются слабыми электролитами: сернистая кислота, карбонат калия, гидроксид натрия, гидроксид аммония, фосфат кальция, нитрат калия: 1) К2СО3; NaOH; NH4OH 2) КNO3; H2SO3; K2CO3 3) NaOH; Са3(РО4)2; К2СО3 4) Н2SO3; NH4OH; Ca3(PO4)2 2. Какова суммарная концентрация ионов в 0,1М растворе ортофосфата натрия? 1) 0,3 моль/л 2) 0,1 моль/л 3) 0,4 моль/л 4) 0,2 моль/л 3. В растворах каких веществ концентрация ионов водорода наибольшая: 1) СН3СООН 2) Н2SO4 3) Н3РО4 4) НСIO 4. Сколько молекул электролита продиссоциирует из каждых 150 внесенных в раствор, если степень диссоциации равна 20%?
8.1 Содержание программы Диссоциация воды. Ионное произведение воды. Водородный показатель. Буферные системы. Роль буферных систем в биологических процессах. Понятие гидролиза и его значение. Типы гидролизующихся солей. Применение законов равновесия к гидролизу. Степень и константа гидролиза. Ступенчатый гидролиз.
Уровень теоретической и практической подготовки Студент должен усвоить понятия:ионное произведение воды, водородный и гидроксильный показатели, степень и константа гидролиза; должен знать состав буферных растворов, их свойства и значение, принцип смещения равновесия в применении к гидролизу. Студент должен уметь рассчитывать рН и рОН растворов по известной концентрации водородных (гидроксильных) ионов и наоборот, концентрацию ионов водорода и рН сильных и слабых кислот и оснований, буферных растворов, предсказывать реакцию среды при растворении соли. Студент должен владеть техникой определения рН с помощью индикаторов и иономера. 8.2 Методические рекомендации к теме Соотношение концентраций водородных и гидроксильных ионов играет важную роль в самых различных явлениях и процессах: и в природе, и в технике. Нормальное развитие разных сельскохозяйственных культур возможно лишь в определенных интервалах значений рН почвенного раствора. Для снижения кислотности почв применяют известкование (вносят в почву карбонат кальция и карбонат магния), а для снижения щелочности – гипсование (вносят в почву молотый гипс). Водородный показатель рН – это показатель молярной концентрации водородных ионов в растворе, равный отрицательному десятичному логарифму этой концентрации: рН = - lg[H+] (43) Отсюда [H+]=10-рН (44) По значению рН судят о характере среды (рис.1). Гидроксильный показатель рОН – это показатель молярной концентрации гирдроксильных ионов в растворе, равный отрицательному десятичному логарифму этой концентрации: рОН = - lg[ОH-] (45) Отсюда [ОH]=10-рОН (46)
Водородный и гидроксильный показатели в растворе взаимосвязаны: рН + рОН = 14 (47) Ионное произведение воды (Кw) – это неизменная при постоянной температуре величина Кw = [H+]·[ОH-]=10-14 (при 220С) (48) Существуют растворы, способные поддерживать рН на определенном уровне – буферные растворы. Они играют очень важную роль в жизни растений и животных. Буферные растворы состоят из слабой кислоты и ее соли образованной сильным основанием, например, ацетатный СН3СООН + СН3СООNа; слабого основания и его соли, образованной сильной кислотой, например аммиачный NН4ОН + NН4Сl; солей слабых многоосновных кислот, например карбонатный NaHCO3+Na2CO3. Формулы для вычисления концентрации водородных ионов [H+] в растворах: сильная одноосновная сильное однокислотное кислота: основание (щелочь): [H+] = CМ к-ты (49) [OH-] = CМ щел. (50) слабая одноосновная кислота: слабое однокислотное основание: [H+] =
Таблица – 8. Формулы для вычисления константы гидролиза, степени гидролиза и рН солей
pK – силовой показатель кислоты или основания. Он равен отрицательному десятичному логарифму константы диссоциации кислоты или основания соответственно: рК = -lgK. 8.3 Примеры решения задач Задача 1. Вычистите рН раствора, концентрация гидроксильных ионов в котором 2,65·10-8 моль/л. Решение: 1 cпособ 1) Рассчитываем рОН по формуле 45: рОН = - lg[ОH-]= -lg2,65·10-8 = 8 – lg2,65=8 – 0,42=7,58 2) Так как сумма рН и рОН в растворе равна 14, вычисляем рН: рН=14–7,58=6,42 2 способ 1) Выразим концентрацию ионов водорода из формулы 48: Задача 2. Какова концентрация водородных ионов в растворе с рОН = 3,45? Решение: 1 cпособ1) Рассчитываем рН по формуле 47: рН = 14 – рОН = 14 – 3,45= 10,55 2) По формуле 44 вычисляем [Н+]: [H+]=10-рН = 10-10,55 = 10-11·100,45=2,82·10-11 2 cпособ 1) По формуле 46 вычисляем концентрацию гидроксильных ионов: [ОH]=10-рОН=10-3,45=10-4·100,55=3,55·10-4моль/л 2) Концентрацию водородных ионов рассчитываем через ионное произведение воды: Задача 3. Определите рН 0,008М раствора серной кислоты. Решение: 1) Серная кислота является сильной кислотой, поэтому расчет будем вести по формуле 49 только нужно учесть, что она двухосновная: [H+] = 2·CM(Н2SO4)=2·0,008= 0,016 моль/л 2) Рассчитываем рН: рН = -lg[H+] = -lg0,016 = 1,8 Задача 4. Определите рН 0,03М раствора гидроксида аммония. Решение: 1) Гидроксид аммония является слабым основанием, поэтому используем формулу 52: Задача 5. Рассчитайте рН раствора, если в 2 л его содержится 6 г уксусной кислоты и 8,2 г ацетата натрия. Решение: 1) Раствор данного состава является буферным кислотного типа, поэтому расчет рН будем производить по формуле 53. Для этого сначала рассчитаем молярные концентрации кислоты и соли: М(СН3СООН)=60г/моль, М(СН3СООNa)=82 г/моль
Задача 6. Рассчитайте константу и степень гидролиза (%) и рН 0,02М раствора цианида калия при комнатной температуре. Решение: 1) Сначала необходимо установить тип соли. Так как циановодородная кислота слабая, а гидроксид калия щелочь, соль относится к первому типу, и при решении будем использовать соответствующие формулы из таблицы 8: 8.4 Лабораторная работа №4 « Экспериментальное определение водородного показателя» Цель работы: изучить способы качественной и количественной оценки реакции среды. Приборы и оборудование: иономер И-500, предметное стекло, капельные пипетки, универсальная индикаторная бумага, штатив с пробирками, химические стаканы емкостью 50 см3. Реактивы: растворы индикаторов лакмуса, фенолфталеина, метилового оранжевого, 0,1 н. растворы гидроксида натрия NaOH, соляной кислоты НСI, уксусной кислоты СН3СООН, водопроводная и дистиллированная вода. Выполнение работы. Опыт 1. Окраска индикаторов в различных средах В три пробирки налейте по 1,5 - 2 см3 дистиллированной воды и добавьте по 2 капле фенолфталеина. В одну пробирку добавьте несколько капель 0,1 н. НС1, в другую - 0,1 н. NaOH. Наблюдайте окраску фенолфталеина в нейтральной, кислой и щелочной средах. После выполнения опыта растворы вылейте, посуду тщательно вымойте. Повторите опыт с использованием индикаторов метилоранжа и лакмуса. Окраску индикаторов запишите в табл.9. Таблица 9 – Окраска индикаторов в различных средах
Опыт 2. Определение рН в растворах посредством универсальной индикаторной бумаги На предметное стекло поместите 4 кусочка универсальной индикаторной бумаги, нанесите на каждый по капле исследуемого раствора, сравните изменение окраски с цветной шкалой и определите значение рН. Результаты наблюдений занесите в таблицу 10.
Таблица 10 – Окраска универсальной индикаторной бумаги в различных средах
Опыт 3.Определение рН растворов с помощью иономера Ознакомьтесь с правилами работы на иономере. Проведите определение рН растворов на приборе по прилагаемому к нему описанию. Рассчитайте значения концентраций [H+] и [OH-] в исследуемых растворах по результатам значений рН, полученным на иономере. Результаты запишите в сводную таблицу 11. Таблица 11 – Результаты измерения рН растворов с помощью иономера
Опыт 4.Определение рН раствора уксусной кислоты Измерьте рН 0,1 н. раствора уксусной кислоты с помощью иономера. Для этого налейте в стакан емкостью 50 см3 анализируемый раствор и поместите его на предметный столик. Опустите электроды в раствор и измерьте рН. Так как уксусная кислота является слабым электролитом, рассчитайте концентрацию гидроксильных ионов в анализируемом растворе по формуле 51: [H+] = 3. Каковы значения рН в кислой, щелочной и нейтральной средах? 4. Что называется ионным произведением воды? Чему оно равно при 200С? Как изменяется с ростом температуры? 5. Назовите методы определения рН. 6. Приведите примеры влияния рН на биологические и сельскохозяйственные объекты. 7. Что такое буферные растворы? Приведите примеры.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 738; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.39.93 (0.03 с.) |
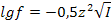 (41)2. Слабые электролиты в растворах диссоциируют частично. К ним относятся вода, кислоты, например: HNO2, HCIO, HCIO2, H2SO3, H2CO3, H2S, CH3COOH; нерастворимые в воде основания, гидроксид аммония NH4OH. В их растворах устанавливается динамическое равновесие между недиссоциированными молекулами и ионами. Так, например, в водном растворе азотистой кислоты устанавливается равновесие: HNO2 ↔ H+ + NO2- Процесс диссоциации слабого электролита характеризуется степень и константой диссоциации. Константа диссоциации (Кд) является частным случаем константы равновесия применительно к процессу диссоциации. В данном примере она выглядит так:
(41)2. Слабые электролиты в растворах диссоциируют частично. К ним относятся вода, кислоты, например: HNO2, HCIO, HCIO2, H2SO3, H2CO3, H2S, CH3COOH; нерастворимые в воде основания, гидроксид аммония NH4OH. В их растворах устанавливается динамическое равновесие между недиссоциированными молекулами и ионами. Так, например, в водном растворе азотистой кислоты устанавливается равновесие: HNO2 ↔ H+ + NO2- Процесс диссоциации слабого электролита характеризуется степень и константой диссоциации. Константа диссоциации (Кд) является частным случаем константы равновесия применительно к процессу диссоциации. В данном примере она выглядит так: Константы диссоциации слабых кислот и оснований приведены в приложении 5. Чем больше Кд тем сильнее электролит. Степень диссоциации (α) – это число, показывающее какая часть от общего количества электролита распалась на ионы:
Константы диссоциации слабых кислот и оснований приведены в приложении 5. Чем больше Кд тем сильнее электролит. Степень диссоциации (α) – это число, показывающее какая часть от общего количества электролита распалась на ионы: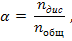 где nдис – количество электролита, распавшегося на ионы, nобщ - общее количество электролита. Степень и константа диссоциации связаны законом разбавления Оствальда:
где nдис – количество электролита, распавшегося на ионы, nобщ - общее количество электролита. Степень и константа диссоциации связаны законом разбавления Оствальда:  , где См - молярная концентрация электролита. Так как для слабого электролита α «1, то 1–α ≈ 1 и закон приобретает вид: Кд = α2См (42) 7.3 Примеры решения задач Задача 1. Рассчитайте ионную силу и активность ионов в 0,05М растворе сульфата калия. Решение: 1) При диссоциации 1 молекулы сульфата калия образуется 2 иона К+ и 1 ион SO42-: К2SO4 →2К+ + SO42-. Поэтому концентрации ионов ответственно равны: СК+= 0,1моль/л, СSO₄²⁻ = 0,05 моль/л. 2) Рассчитаем ионную силу раствора по формуле (40):
, где См - молярная концентрация электролита. Так как для слабого электролита α «1, то 1–α ≈ 1 и закон приобретает вид: Кд = α2См (42) 7.3 Примеры решения задач Задача 1. Рассчитайте ионную силу и активность ионов в 0,05М растворе сульфата калия. Решение: 1) При диссоциации 1 молекулы сульфата калия образуется 2 иона К+ и 1 ион SO42-: К2SO4 →2К+ + SO42-. Поэтому концентрации ионов ответственно равны: СК+= 0,1моль/л, СSO₄²⁻ = 0,05 моль/л. 2) Рассчитаем ионную силу раствора по формуле (40):  3) Коэффициенты активности ионов рассчитаем по формуле 41: lgf(K+) = – 0,5z2√Ī= – 0,5·12√0,15= –0,19; f(K+)= 0,65 lgf(SO4 2-) = – 0,5z2√Ī= – 0,5·22√0,15= – 0,774; f (SO42-) = 0,17 4) Находим активность ионов: а (К+)=0,65·0,1=0,065 моль/л; а(SO42-)=0,17·0,05=0,0085моль/л Задача 2. Вычислить суммарную концентрацию ионов в 0,02М растворе муравьиной кислоты, если степень диссоциации равна 3%. Решение: 1) Согласно уравнению диссоциации НСООН ↔ Н+ + НСОО- концентрации катионов и анионов равны и совпадают с количеством продиссоциировавшей кислоты: [H+]=[HCOO-]=nдис= α· nобщ=0,02·0,03=0,0006 моль/л 2) Находим суммарную концентрацию ионов [H+]+[HCOO-]= 0,0012 моль/л. Задача 3. При какой концентрации раствора степень диссоциации гидроксида аммония будет равна 0,01? Решение: 1) Рассчитываем концентрацию гидроксида аммония по закону разбавления (формула 42):
3) Коэффициенты активности ионов рассчитаем по формуле 41: lgf(K+) = – 0,5z2√Ī= – 0,5·12√0,15= –0,19; f(K+)= 0,65 lgf(SO4 2-) = – 0,5z2√Ī= – 0,5·22√0,15= – 0,774; f (SO42-) = 0,17 4) Находим активность ионов: а (К+)=0,65·0,1=0,065 моль/л; а(SO42-)=0,17·0,05=0,0085моль/л Задача 2. Вычислить суммарную концентрацию ионов в 0,02М растворе муравьиной кислоты, если степень диссоциации равна 3%. Решение: 1) Согласно уравнению диссоциации НСООН ↔ Н+ + НСОО- концентрации катионов и анионов равны и совпадают с количеством продиссоциировавшей кислоты: [H+]=[HCOO-]=nдис= α· nобщ=0,02·0,03=0,0006 моль/л 2) Находим суммарную концентрацию ионов [H+]+[HCOO-]= 0,0012 моль/л. Задача 3. При какой концентрации раствора степень диссоциации гидроксида аммония будет равна 0,01? Решение: 1) Рассчитываем концентрацию гидроксида аммония по закону разбавления (формула 42): 

 (51) [OH-] =
(51) [OH-] =  (52)
(52)
 буферный раствор кислотного типа: буферный раствор основного типа: [H+] = Кк-ты
буферный раствор кислотного типа: буферный раствор основного типа: [H+] = Кк-ты  (53) [OH-] = Косн
(53) [OH-] = Косн  (54) Важным понятием этой темы является гидролиз солей, так как этот процесс имеет большое значение в жизни животных и растений. Ведь усвоение питательных веществ осуществляется в виде ионов – продуктов гидролиза многих солей. Гидролизом солей называется взаимодействие ионов соли с водой, ведущее к образованию слабого электролита. Необходимо отработать навыки составления уравнений гидролиза. Для успешного усвоения достаточно сложного материала целесообразно придерживаться следующего плана: 1) определить, каким основанием и какой кислотой образована соль, используя таблицу растворимости и таблицу констант диссоциации; 2) составить уравнение диссоциации соли; 3) гидролиз пойдет по иону, входящему в состав слабого электролита; 4) составить уравнение реакции взаимодействия этого иона с водой. Это уравнение и будет сокращенным ионным уравнением гидролиза; 5) записать уравнение гидролиза в полной ионной форме. При этом к каждому иону приписать ионы противоположного заряда; 6) заключительным этапом является составление молекулярного уравнения. Пример 1. Составить уравнение гидролиза нитрата меди (II):
(54) Важным понятием этой темы является гидролиз солей, так как этот процесс имеет большое значение в жизни животных и растений. Ведь усвоение питательных веществ осуществляется в виде ионов – продуктов гидролиза многих солей. Гидролизом солей называется взаимодействие ионов соли с водой, ведущее к образованию слабого электролита. Необходимо отработать навыки составления уравнений гидролиза. Для успешного усвоения достаточно сложного материала целесообразно придерживаться следующего плана: 1) определить, каким основанием и какой кислотой образована соль, используя таблицу растворимости и таблицу констант диссоциации; 2) составить уравнение диссоциации соли; 3) гидролиз пойдет по иону, входящему в состав слабого электролита; 4) составить уравнение реакции взаимодействия этого иона с водой. Это уравнение и будет сокращенным ионным уравнением гидролиза; 5) записать уравнение гидролиза в полной ионной форме. При этом к каждому иону приписать ионы противоположного заряда; 6) заключительным этапом является составление молекулярного уравнения. Пример 1. Составить уравнение гидролиза нитрата меди (II):  Cu(NO3)2 Cu (OH)2 слабый электролит 2) Cu(NO3)2 ↔ Cu 2+ + NO3- (I) 3) ион Сu2+ входит в состав слабого электролита, следовательно, гидролиз пойдет по катиону 4) записываем уравнение реакции его с водой: Cu2+ + HOН ↔ (CuOH)+ + H+ Естественно, что ион Сu2+ будет связывать отрицательный ион ОН- из состава воды. Заряд образовавшегося иона CuOH+ равен сумме зарядов Cu2+ и OH-. Связывание ионов ОН- ведет к избытку в растворе ионов Н+, что создает кислую реакцию в растворе 5) к каждому иону приписываем ионы противоположного знака, содержащиеся в растворе (это ионы NO3 -): Cu2+ + 2NO3- + H2O ↔ (CuOH)+ + NO3- + H+ + NO3- 6) объединяя противоположные ионы в молекулы, составляем молекулярное уравнение гидролиза: Cu(NO3)2 + H2O ↔ (CuOH)NO3 + HNO3 Так как ион Cu2+ двухзарядный, то возможна и вторая ступень гидролиза соли. Суть ее состоит во взаимодействии катиона, образовавшегося на первой ступени еще с одной молекулой воды. Все остальные действия повторяются: (CuOH)+ + H2O ↔ Cu(OH)2 +H+ (CuOH)+ + NO3- + H2O ↔ Cu(OH)2 + H+ + NO3- CuOHNO3 + H2O ↔ Cu(OH)2 + HNO3 Пример 2. Гидролиз карбоната калия
Cu(NO3)2 Cu (OH)2 слабый электролит 2) Cu(NO3)2 ↔ Cu 2+ + NO3- (I) 3) ион Сu2+ входит в состав слабого электролита, следовательно, гидролиз пойдет по катиону 4) записываем уравнение реакции его с водой: Cu2+ + HOН ↔ (CuOH)+ + H+ Естественно, что ион Сu2+ будет связывать отрицательный ион ОН- из состава воды. Заряд образовавшегося иона CuOH+ равен сумме зарядов Cu2+ и OH-. Связывание ионов ОН- ведет к избытку в растворе ионов Н+, что создает кислую реакцию в растворе 5) к каждому иону приписываем ионы противоположного знака, содержащиеся в растворе (это ионы NO3 -): Cu2+ + 2NO3- + H2O ↔ (CuOH)+ + NO3- + H+ + NO3- 6) объединяя противоположные ионы в молекулы, составляем молекулярное уравнение гидролиза: Cu(NO3)2 + H2O ↔ (CuOH)NO3 + HNO3 Так как ион Cu2+ двухзарядный, то возможна и вторая ступень гидролиза соли. Суть ее состоит во взаимодействии катиона, образовавшегося на первой ступени еще с одной молекулой воды. Все остальные действия повторяются: (CuOH)+ + H2O ↔ Cu(OH)2 +H+ (CuOH)+ + NO3- + H2O ↔ Cu(OH)2 + H+ + NO3- CuOHNO3 + H2O ↔ Cu(OH)2 + HNO3 Пример 2. Гидролиз карбоната калия  H2 CO 3 cлабый электролит
H2 CO 3 cлабый электролит  1) K2CO3 KОН сильный электролит 2) K2CO3 ↔ 2K+ + CO 32- 3) так как в состав слабого электролита входит ион СО32-, то гидролиз пойдет по аниону 4) записываем уравнение реакции его с водой СО32- + НОН = НСО3- + ОН-Естественно, что отрицательный ион CO32- будет связывать положительный ион Н+. Заряд образовавшегося иона НСО3- равен сумме зарядов СО32- и Н+. Связывание ионов Н+ ведет к избытку ионов ОН- , что определяет щелочную реакцию раствора. 5) СО32- + 2К+ + Н2О ↔ НСО3- + К+ + ОН- + К+ 6) К2СО3 + Н2О ↔ КНСО3 + КОН Так как ион СО32- двухзарядный, то он будет взаимодействовать поочередно с двумя молекулами воды, т.е. возможна II ступень гидролиза: НСО3- + Н2О ↔ Н2СО3 + ОН- НСО3- + К+ + Н2О ↔ Н2СО3 + ОН- + К+ КНСО3 + Н2О ↔ Н2СО3 + КОН Пример 3. Гидролиз нитрита аммония:
1) K2CO3 KОН сильный электролит 2) K2CO3 ↔ 2K+ + CO 32- 3) так как в состав слабого электролита входит ион СО32-, то гидролиз пойдет по аниону 4) записываем уравнение реакции его с водой СО32- + НОН = НСО3- + ОН-Естественно, что отрицательный ион CO32- будет связывать положительный ион Н+. Заряд образовавшегося иона НСО3- равен сумме зарядов СО32- и Н+. Связывание ионов Н+ ведет к избытку ионов ОН- , что определяет щелочную реакцию раствора. 5) СО32- + 2К+ + Н2О ↔ НСО3- + К+ + ОН- + К+ 6) К2СО3 + Н2О ↔ КНСО3 + КОН Так как ион СО32- двухзарядный, то он будет взаимодействовать поочередно с двумя молекулами воды, т.е. возможна II ступень гидролиза: НСО3- + Н2О ↔ Н2СО3 + ОН- НСО3- + К+ + Н2О ↔ Н2СО3 + ОН- + К+ КНСО3 + Н2О ↔ Н2СО3 + КОН Пример 3. Гидролиз нитрита аммония:  1) NH4NO2 H NO 2 слабый электролит 2) NH4NO2 ↔ NH 4+ + NO 2- 3) так как оба иона входят в состав слабых электролитов, то оба будут взаимодействовать с водой 4) NH4+ + NO2- + Н2О ↔ NH4OН + НNO2 5) NH4NO2 + Н2О ↔ NH4OН + НNO2
1) NH4NO2 H NO 2 слабый электролит 2) NH4NO2 ↔ NH 4+ + NO 2- 3) так как оба иона входят в состав слабых электролитов, то оба будут взаимодействовать с водой 4) NH4+ + NO2- + Н2О ↔ NH4OН + НNO2 5) NH4NO2 + Н2О ↔ NH4OН + НNO2 
 Среда будет зависеть от того, какой электролит сильнее – гидроксид аммония или азотистая кислота. Так как Кд (НNO2) = 4·10 – 4, Кд (NH4OН) = 2·10 – 5 и 4·10 – 4 > 2·10 – 5 среда будет кислая. Необходимо знать, что соли, образованные очень слабым основанием и очень слабой кислотой, могут подвергаться необратимому гидролизу. Например, карбонат железа (III): 3CO2 Fe2(CO3)3 + 6H2O = 2Fe (OH)3↓ + 3H2CO3 3H2O Количественными характеристиками процесса гидролиза являются степень и константа гидролиза. Константа гидролиза (Кг) – это частный случай константы равновесия применительно к реакции гидролиза. Например, для реакции гидролиза нитрата аммония: NH4+ + NO2- + Н2О ↔ NH4OН + НNO2 выражение константы гидролиза имеет вид:
Среда будет зависеть от того, какой электролит сильнее – гидроксид аммония или азотистая кислота. Так как Кд (НNO2) = 4·10 – 4, Кд (NH4OН) = 2·10 – 5 и 4·10 – 4 > 2·10 – 5 среда будет кислая. Необходимо знать, что соли, образованные очень слабым основанием и очень слабой кислотой, могут подвергаться необратимому гидролизу. Например, карбонат железа (III): 3CO2 Fe2(CO3)3 + 6H2O = 2Fe (OH)3↓ + 3H2CO3 3H2O Количественными характеристиками процесса гидролиза являются степень и константа гидролиза. Константа гидролиза (Кг) – это частный случай константы равновесия применительно к реакции гидролиза. Например, для реакции гидролиза нитрата аммония: NH4+ + NO2- + Н2О ↔ NH4OН + НNO2 выражение константы гидролиза имеет вид: 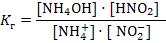 Степень гидролиза (h) показывает какая часть молекул соли подверглась гидролизу:
Степень гидролиза (h) показывает какая часть молекул соли подверглась гидролизу:  Для расчета степени гидролиза, константы гидролиза и рН растворов солей можно пользоваться формулами таблицы 8.
Для расчета степени гидролиза, константы гидролиза и рН растворов солей можно пользоваться формулами таблицы 8.
 Тип соли
Тип соли
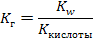





 2) По формуле 43 рассчитываем рН: рН = - lg[H+]= - lg3,77·10-7=7-lg3,77=7-0,576=6,42
2) По формуле 43 рассчитываем рН: рН = - lg[H+]= - lg3,77·10-7=7-lg3,77=7-0,576=6,42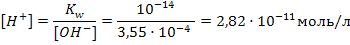
 Константу диссоциации гидроксида аммония берем из приложения 5. 2) Рассчитываем рН раствора: рН=14-рОН=14+lg7,25·10-4=14-4+lg7,25=10,86
Константу диссоциации гидроксида аммония берем из приложения 5. 2) Рассчитываем рН раствора: рН=14-рОН=14+lg7,25·10-4=14-4+lg7,25=10,86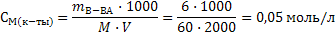
 2) Рассчитываем концентрацию водородных ионов и рН:
2) Рассчитываем концентрацию водородных ионов и рН:  рН=-lg[H+]=-lg1,75·10-5=5-lg1,75=5-0,24=4,76
рН=-lg[H+]=-lg1,75·10-5=5-lg1,75=5-0,24=4,76
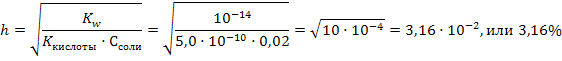 рН=7+½рКкис+½lgCсоли=7-½lg5,0·10-10+½lg0,02=7-½(-10+lg5,0)+½lg0,02=7-+4,65-0,85=10,8
рН=7+½рКкис+½lgCсоли=7-½lg5,0·10-10+½lg0,02=7-½(-10+lg5,0)+½lg0,02=7-+4,65-0,85=10,8


