
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Водный обмен и его нарушенияСтр 1 из 19Следующая ⇒
ВОДНЫЙ ОБМЕН, Выделение
Водный обмен и его нарушения Вода является растворителем органических и неорганических веществ. Она представляет собой основную среду развертывания метаболических процессов, осуществляет транспорт многих веществ, как между клетками, так и органами. В различных органах и тканях взрослого человека относительное содержание воды от 68% (печень) до 83% (кровь). Исключение составляет скелет (22%) и жировая ткань (10%). Среднее содержание воды в организме взрослого мужчины около 73% массы тела. В организме женщин, как правило, жира больше и поэтому в их теле воды примерно на 6-10% меньше. У новорожденных процентное содержание воды примерно на 10% выше. Это различие ликвидируется постепенно к окончанию полового созревания. Количество воды, входящей в различные структуры клетки, межклеточное вещество, полости, определяет водный режим организма (рис. 73). В организме вода находится в пяти основных формах: внутриклеточная, интестициальная (межклеточная), внутрисосудистая (в системе крово- и лимфообращения), жидкость закрытых полостей (внутри суставов, в сердечной сумке, плевральной полости и др.) и "открытых" органах (желудочно-кишечном тракте, мочевых путях, потовых железах). Между всеми этими водными средами идет активный обмен жидкости. Особенно он интенсивен между первыми тремя. Так, в опытах с применением меченой воды показано, что за 1 минуту более 70% всей жидкости плазмы крови обменивается с интерстициальным пространством.
Рис. 73. Основные жидкие среды организма
У здорового человека поддерживается равенство объема поступающей и выделяемой воды, что носит название водного баланса организма. Обычно в организм здорового человека с пищей и питьем поступает около 2100 мл воды, 200-300 мл образуется в клетках в процессе окисления. Диффузия через кожу обеспечивает выделение около 300-400 мл, потеря через органы дыхания составляет так же 300-400 мл, с потом выделяется минимум 100 мл. С фекалиями выделяется до 100 мл воды. Остальное количество воды выделяется через почки. При различных условиях (изменение внешней температуры, характера питания и питья, физической активности) отдельные показатели водного баланса меняются, но у здорового человека сам баланс сохраняется. Так, выделение воды с потом весьма вариабельно: от 100 мл/сутки до 2000 мл/час. Почки у здорового человека также обладают довольно широким диапазоном колебаний количества выделяемой жидкости: от 0,5 до 20 л/сутки. Интерстициальная жидкость Среди всех жидкостных сред организма наиболее мобильным звеном является жидкость межклеточного пространства. Она практически не имеет собственных механизмов образования и регуляции. Образуется она в результате фильтрации: с одной стороны из плазмы крови, с другой - из клеток тканей. Здесь жидкость находится главным образом в связанном с белками состоянии в виде геля. Небольшое количество свободной жидкости размещется в виде мельчайших пузырьков среди структур межклеточного вещества. В связи с тем, что основная вода находится в связанном состоянии, ток ее через гель очень медленный. Ведущей движущей силой здесь является диффузия. Диффундируют не только молекулы воды, но и продукты клеточного обмена, газы (О2 и СО2), электролиты. В межклеточном веществе возникает и гидростатическое давление. Оно образуется в связи с тем, что объем межуточного пространства ограничивают соединительнотканные волокна, а наличие белковых молекул и ионов, создавая некоторую величину осмотического и онкотического давления, притягивают воду. В большинстве органов онкотическое давление около 6 мм рт.ст. В различных органах и тканях коллоидно-осмотическое и гидростатическое давления в межклеточном веществе отличаются.
В плотноупакованных органах и тканях гидростатическое давление на несколько мм рт.ст. выше атмосферного. Так, в мозге оно в пределах +4 - +6 мм рт.ст., в почке - около +6 мм рт.ст. В отличие от этого в интерстиции подкожной клетчатки его величина несколько ниже атмосферного: -2 - -6 мм рт.ст. Столь низкое гидростатическое давление подкожной клетчатки создает возможность для развития здесь отека. Этому способствует застой крови в венах, что приводит к росту гидростатического давления в капиллярах. Снижение концентрации белков крови, уменьшая силу онкотического давления, удерживающую воду в русле крови, увеличивает содержание свободной воды в подкожной клетчатке. Кровь и водный обмен Осмотическое давление крови. Различные соединения, растворенные в плазме и в форменных элементах крови, создают в них осмотическое давление. В норме осмотическое давление плазмы крови около 7,6 атм. (5700 мм рт.ст., 762 кПа, около 282 мОсм/н.). Величина осмотического давления определяется количеством растворенных молекул, а не их размерами. Львиная доля (примерно 199/200) ионов плазмы - неорганические ионы. Их количество и определяет величину осмотического давления. Белки плазмы создают онкотическое давление, равное лишь 0,03 - 0,04 атм. (25-30 мм рт.ст.). Но в то же время онкотическое давление играет важнейшую роль в регуляции распределения воды между плазмой и тканями. Из общего онкотического давления на альбумины (4,5 г%) приходится 21,8 мм рт.ст., глобулины (2,5 г%) - 6,0 мм рт.ст. и фибриноген (0,3 г%) - 0,2 мм рт.ст. Участие онкотического давления в регуляции обмена воды обусловлено тем, что стенка обменных сосудов (капилляров) в большинстве органов непроницаема для белков. В тканевой жидкости свободных белков мало, поэтому имеется градиент их концентрации с кровью. В отличие от этого в крови и межклеточной жидкости содержание неорганических или небольших органических молекул, как правило, одинаково. Большее онкотическое давление крови служит основой механизма удержания воды в ней.
Рис. 74. Эритроцит (сканирующая микроскопия): А - интактный эритроцит; Б - эритроцит в гипертоническом растворе.
Механизмы гипогидратации При чрезмерном снижении поступления жидкости в организм или при усиленном и несбалансированном ее выведении развивается гипогидратация. Сравнительно редко, например, сразу после кровопотери, когда за счет поступления межклеточной жидкости начинается восстановление утерянного объема крови, наблюдается изоосмомолярная ги-погидратация. Но чаще всего гипогидратация бывает гипо- либо гиперосмомолярной. Гипоосмомолярная гипогидратация возникает при чрезмерной потери жидкости содержащей электролиты. Это происходит при диарее, при снижении продукции АДГ и альдостерона. Недостаток указанных гормонов приводит к выведению через почки большого количества гипоосмомолярной мочи. Но это приведет к развитию лишь внеклеточной гипоосмомолярной гипогидратации, так как отсюда вода и ионы начнут поступать в русло крови. При крайней степени гипогидратации может развиваться даже внутриклеточный отек, так как мембрана у большинства клеток слабо проницаема для ионов и вода из межуточного вещества начнет поступать в клетки. Гиперосмомолярная гипогидратация развивается при потере жидкости обедненной электролитами. Чаще всего она развивается вследствие уменьшения воды, поступающей в организм через желудочно-кишечный тракт (диарея, рвота). При выведении воды из желудочно-кишечного тракта она начинает поступать сюда из крови (см. механизм всасывания воды в кишечнике). Данная форма нарушения водного обмена наблюдается и при чрезмерном выделении мочи (например, при сахарном диабете и другого типа полиурии), при профузном потоотделении. Возрастание осмотического давления плазмы крови приведет к движению жидкости из межклеточной среды в кровь, а из клеток в межклеточное пространство. В результате постепенно разовьется и общая гипогидратация организма. Гипогидратация может быть причиной развития цепи изменений. Так, обезвоживание межклеточного сектора приведет к развитию гиповолемии и артериальной гипотензии. Следствием этого возникнет гипоксия, обусловленная недостаточным кровоснабжением органов. Эти явления резко усиливаются внутрисосудистыми (результат сгущения крови) и внесосудистыми нарушениями микроциркуляторной гемодинамики. Все это приведет к нарастанию дезорганизации метаболизма в тканях вплоть до распада белков и появления гидроперекисей липидов. А это еще более осложнит гемодинамику и может привести к недостаточности функции почек.
Механизмы гипергидратации Избыточное поступление воды при недостаточном выведении ее из организма является причиной гипергидратации. Типичным примером развития такой ситуации является острая почечная недостаточность. При нарушении функции почек гипергидратация может быть следствием даже таких врачебных манипуляций как промывание желудка большим количеством воды. При этом возникает гипоосмомолярная гипергидратация чаще всего внеклеточного и клеточного секторов (отек). Чрезвычайно выраженная гипергидратация проявляется в виде водной интоксикации. Когда осмотическое давление в интерстиции снижается больше, чем в клетках, тогда клетки начинают поглощать воду. В результате снижения осмотического давления в них нарушаются функции. Особенно наглядно такое нарушение проявляется на самых чувствительных клетках - нервных, что сопровождается возникновением возбуждения многих нервных центров. ВЫДЕЛЕНИЕ В водном и ионном обмене огромную роль играют почки, при этом они, образуя водный раствор – мочу, участвуют в выполнении выделительной функции. В процессе метаболизма образуются соединения, от которых организм должен освобождаться, так как они, накапливаясь в большом количестве, не только нарушают функции отдельных органов и всего организма, но могут послужить и причиной его гибели. Выделению подлежат также некоторые вещества, поступающие с пищей, или вводимые при проведении лечебных процедур. Среди указанных метаболитов имеются газообразные, жидкие и твердые вещества. В выделении их кроме почек принимают участие и другие органы: легкие, потовые железы кожи, желудочно-кишечный тракт. Тем самым все эти органы участвуют в поддержании гомеостаза. Особенно значительная роль в системе выделения принадлежит почкам. При этом они выполняют следующие функции: · экскретируют конечные метаболиты азотистого обмена; · экскретируют чужеродные вещества; · экскретируют избыток органических и неорганических веществ, попавших с пищей или образовавшихся в ходе метаболизма; · поддерживают постоянство осмотического давления крови; · поддерживают ионный баланс организма; · поддерживают кислотно-основное состояние; · участвуют в метаболизме белков, жиров, углеводов; · участвуют в регуляции кровообращения; · участвуют в регуляции объема циркулирующей крови, · секретируют биологически активные вещества и ферменты; · регулируют эритропоэз. Поэтому патология почек приводит к развитию разнообразных нарушений функций организма. Но при этом особенно проявляется недостаточность именно выделительной их функции, которая лишь частично может быть компенсирована другими органами. И при полной анурии через две-три недели наступает неминуемая гибель организма от уремии. Уремия. Одним из наиболее грозных осложнений почечной недостаточности является уремия. Хотя под уремией чаще всего понимают задержку выведения из организма мочевины. Но кроме мочевины в крови повышается содержание и других продуктов, содержащих небелковый азот, таких как мочевая кислота и креатинин. Эти соединения (как и мочевина) представляют из себя конечные продукты обмена, которые обеспечивают обновление клеточных структур организма. При хронической почечной недостаточности концентрация в плазме крови указанных метаболитов примерно соответствует степени уменьшения числа нефронов. При острой же ее недостаточности концентрация мочевины в течение первых 2-х недель может превышать норму в 10 раз. Определение содержания в крови этих соединений играет важную роль в оценке степени почечной недостаточности и развития уремии.
Но при недостаточности почек, как правило, не удаляются в должном объеме и другие соединения (вода, гуанидиновые основания, фенолы, сульфаты, фосфаты, калий и т.д.). Все это приводит к целому букету патологических проявлений. Немаловажно еще и то, что уремия приводит к задержке воды в организме и развитию генерализованных отеков. В этом (максимальная концентрация мочи – 1200 мосм/л) заключается и механизм обезвоживания при попытке пить морскую воду. Осмомолярность океанической воды также около 1000-1200 мосм/л. Значит, с 1 литром воды в организм дополнительно поступит еще и 1200 мосм NaCl. Но почкам необходимо выделять еще и «свои» как минимум 600 мосм растворенных веществ в сутки. Таким образом, выпив 1 л морской воды человек должен выделить около 2 л мочи в сутки, что и приводит к обезвоживанию. 6.2.2. Нефроны Мочеобразование происходит при взаимодействии всех структур нефpона и сосудистой сети. Можно выделить три основные физиологические процессы, протекающие сопряженно и обеспечивающие образование из крови мочи: · клубочковая фильтрация, · канальцевая реабсорбция, · секреция. Структурнофункциональной единицей почек является нефрон. В каждой почке их насчитывается порядка 1,2 - 1,3 млн. В зависимости от места расположения в почке, глубины залегания в корковом слое, различают три типа нефронов: суперфициальные, интракортикальные и юкстамедулярные. Соотношение их таково: суперфициальных нефронов 20-30%, интракортикальных - 40-50%, юкстамедуллярных - 20-30%. Несмотря на некоторые отличия принципиальная схема строения и функционирования нефронов одинакова.
Рис. 6.5. Особенности кровоснабжения различного типа нефронов (а) и строение эпителия различных отделов канальцев (б).
Фильтрация Фильтрация плазмы крови происходит в клубочке 20-40 капилляров, представляющих собой разветвление приносящего сосуда (vasa afferens), собирающихся в выносящий сосуд (vasa efferens). К капиллярам примыкает внутренняя стенка двухслойной капсулы Боумена-Шумлянского. Пространство, находящееся между двумя слоями капсулы (мочевое прстранство), образует как бы воронку, сообщающуюся с просветом канальца. Кроме эндотелия капилляров и подоцитов, в гломерулах есть третий тип клеток - мезангиальные, находящиеся в центральной части внутри капилляных петель. Это соединительная ткань клубочка - мезангий как брыжейка подвешивает капилляры клубочка к гломерулярному полюсу. Из трех типов мезангиоцитов наибольший интерес представляют клетки гладкомышечного типа. Они осуществляют синтез всех компонентов мезангиального матрикса. Эту их функцию контролируют мезангиоциты костномозгового происхождения. Основными компонентами мезангиального матрикса являются коллагеновые волокна и фибронектин. Почечная мембрана. Кровь, протекающая по капиллярам клубочка, от фильтрата, находящегося в полости между двумя листками капсулы, отделяет почечная мембрана. Фильтрующая мембрана состоит из 3-х слоев: эндотелия кровеносных капилляров, базальной мембраны (БМ) и эпителиальных клеток капсулы. Все они имеют “окна”, через которые может легко проходить вода и большинство растворенных в плазме веществ (рис. 662-Б). Эндотелиальные клетки капилляров имеют поры 100-150 нм, закрытые лишь тонкой диафрагмой. Круглые или овальные отверстия эндотелиоцитов, занимающие до 30% площади клетки, за счет имеющегося на их мембране гликокаликса, мешают проникновению форменных элементов крови и крупных молекул. Капсула клубочка представлена базальной мембраной (БМ) и эпителиальными клетками - подоцитами. Последние фиксированы на БМ с помощью филаментов, содержащих актомиозин. Сокращение их обеспечивает один из механизмов регуляции фильтрационной функции почки.
Рис. 75. Структурные элементы, входящие в почечную мембрану (А) и детализация расположения пор (Б). Базальная мембрана имеет толщину 250-400 нм. Она состоит из трех слоев. Ее основной средний слой толщиной 1,2-2,5 нм представлен сетчатыми структурами белков. Состав белков не постоянен и, к примеру, с возрастом количество коллагена в БМ значительно увеличивается, а гликопротеинов - снижается. Вещества базальной мембраны продуцируются подоцитами, эндотелием капилляров и мезангиальными клетками. Из них особая роль принадлежит подоксилину - основному сиалопротеину клубочка. Сиалопротеины подоцитов и эндотелия совместно с протеин-гликанами БМ обеспечивают отрицательный заряд ее, что является одним из основных барьеров для анионных и нейтральных макромолекул. Из всех трех структур почечной мембраны наименее проницаемой является базальная мембрана. Средний радиус пор БМ определяется расстоянием между филаментами коллагеноподобных белков. Промежутки между коллагеновыми нитями примерно 3-7,5 нм. Проницаемость почечной мембраны. Кроме отрицательного заряда структур базальной мембраны, большое значение при фильтрации плазмы крови имеют указанные выше размеры пор. Суммарное “сито” мембраны капсулы легко проходимо для веществ, имеющих молекулярную массу менее 5500. В норме молекулярная масса 80000 является абсолютным пределом прохождения частиц через поры. В указанном промежутке (5500 - 80000) фильтруемость молекул тем меньше, чем больше размер молекулы. Так, фильтруемость гемоглобина (мол. масса 64500) составляет лишь около 3%, а альбумина плазмы (мол. масса 69000) - менее 1%. Естественно, что при поражениях гломерулярных отделов почки, проницаемость их фильтра изменяется, и в мочу могут попадать в большом количестве не только крупные белки, но даже и форменные элементы крови. Скорость клубочковой фильтрации (СКФ). Основой фильтрата (первичной мочи) является вода, в которой можно обнаружить почти все вещества, содержащиеся в плазме крови, за исключением крупных белков. Эффективное фильтрационное давление (ЭФД) является результирующей взаимодействия сил, часть которых выталкивает содержимое крови из капилляров, а другая этому препятствует. Выталкивающей силой является тpансмуpальное давление (Рt), обусловленное pазницей между гидpодинамическим давлением крови клубочка (Рк) и гидpостатическим давлением жидкости, находящейся в пpосвете капсулы (Ргк), а препятствующей - онкотическое давление крови (Ро): ЭФД = Рt - Рo (мм рт.ст.) (6.1) В обычных условиях ЭФД в начальной части капилляра около: (65 - 15) - 25 = 25 мм рт.ст. (33 кПа). Коэффициент фильтрации (Кф) зависит от проницаемости мембраны. В норме, при ненарушенной почечной мембране, фильтрация мало зависит от указанного коэффициента. Существенную поправку в скорость клубочковой фильтрации (СКФ) этот коэффициент вносит при патологии, когда увеличиваются поры почечного “сита”: СКФ = ЭФД·Кф (мл/мин) (6.2) У мужчин СКФ около 125 мл/мин, а у женщин - 110 мл/мин из расчета равной площади поверхности тела в 1,73 м3. В фильтрат поступает примерно 1/5 часть проходящей через почки плазмы. В результате, за сутки образуется 150-180 л фильтpата (первичной мочи). Легко подсчитать, что вся плазма крови очищается почками не менее 60 раз в сутки. Определенный интерес представляет и то, что по мере прохождения крови по капилляру клубочка, в связи с потерей 20% воды происходит существенное возрастание в ней онкотического давления: с 24-28 мм рт.ст. в приносящем конце капилляра до 33-35 мм рт.ст. в выносящем. В результата и данного процесса во второй половине капилляра ЭФД существенно снижается. Это приведет к уменьшению клубочковой фильтрации. Такая ситуация возникает тогда, когда почечный плазмоток невелик (частицы крови продвигается медленнее). В противоположность этому высокая скорость кровотока приведет к увеличению образования первичного фильтрата. Снижение концентрации белка в плазме крови, как это бывает при патологии печени, понижая онкотическое давление, приведет к увеличению скорости клубочковой фильтрации. В то же время увеличение онкотического давления плазмы артериальной крови приведет к снижению скорости клубочковой фильтрации. В физиологических условиях изменение величины давления в капсуле имеет очень небольшое значение. Но в патологии, когда, к примеру, происходит закупорка мочеточника камнем и затрудняется отток по всему мочеатводящему каналу, фильтрация снижается и из-за роста этого показателя. В отличие от плазмы крови ультрафильтрат содержит очень мало белков. Кроме того, в нем в несколько меньшей концентрации находятся многие неорганические катионы, так как часть их в плазме находится не в свободном, а в связанном с белками состоянии. Соотношение свободных и связанных ионов находится в равновесном состоянии и именуется равновесием Доннана. Различие между первичной мочой и плазмой крови по содержанию одновалентных ионов невелико, в то время как по двухвалентным - более существенно. Так, в плазме 40% Са2+ связано с белками. Поэтому содержание кальция в плазме 2,5 ммоль/л, а в фильтрате - 1,3 ммоль/л в виде свободных ионов и 0,2 ммоль/л низкомолекулярных комплексов его. Сиалопротеины подоцитов и эндотелия совместно с протеингликанами БМ обеспечивают отрицательный заряд ее, что является основным барьером для анионных и нейтральных макромолекул. Поэтому содержание такого типа веществ в ультафильтрате также меньше, чем в плазме крови. При некоторых видах патологических процессов, когда исчезает отрицательный заряд пор, почечное тельце становится более проницаемо к белкам. Заряд пор не играет никакой роли для неорганических веществ или низкомелекулярных органических соединений. 6.2.4. Почечная мембрана и регуляция процесса фильтрации. Учитывая значение давления крови в капиллярах клубочка для фильтрации, становится понятным, что для сохранения стабильного процесса мочеобразования оно должно поддерживаться на постоянном уровне. Однако в pеальной жизни даже у здорового человека процесс фильтрации не всегда постоянен, он регулируем и меняется в зависимости от интенсивности кровотока и состояния организма. В зависимости от этого происходит: · изменение скорости фильтрации, · включение или выключение того или иного количества нефронов из процесса мочеобразования как среди однотипных, так и расположенных на разных уровнях почки. Регулируется также и состояние почечного фильтра. Имеющаяся в почке система обратной связи регулирует скорость клубочковой фильтрации в зависимости от объема притекающей крови и во многом - скорости реабсорбции NaCl в данном нефроне. Эта функция выполняется клетками юкстагломерулярного аппарата (ЮГА), которые реагируют на: · степень растяжения афферентной артериолы, · уровень реабсорбции NaCl. При отклонении их параметров от нормы ЮГА, секретируя ренин, запускает гормональную регуляцию процессов реабсорбции и кровотока (подробнее см. ниже). При падении гидростатического давления в капиллярах клубочка “упаковка” коллагеноподобных филаментов в БМ изменяется, что ведет к увеличению размера пор и росту фильтрации. Среди мезангиальных клеток имеются сократимые элементы, фибриллы которых обладают актиновой и миозиновой активностью. Такие же структуры имеются в отростках подоцитов. Это обеспечивает их способность к сокращению и изменению размера пор БМ, от которых во многом зависит фильтрационная функция клубочка. Однако фильтрация осуществляется не только через щелевую диафрагму. В подоцитах имеется система микротрубочек, через которые фильтруется первичная моча. Сокращение миофиламентов цитоплазмы подоцитов путем субмикроскопических насосов своим путем участвует в перекачивании ультрафильтрата плазмы в полость капсулы. Клубочек является так же местом действия ряда гормонов и другого типа регуляторов. Так, фильтрация снижается под влиянием вазопрессина, ангиотензина II, простагландинов Е1, Е2, ацетилхолина, брадикинина, которые воздействуя на мезангиальные клетки, влияют на проницаемость пор клубочковой мембраны. Многие из них действуют опосредованно через увеличение образования или затрудняя разрушение в клетках цАМФ. Накапливаясь, он усиливает секрецию ренина и образование ангиотензина II, что активирует сокращение клеток мезаглии. Мезангиоциты, подоциты и эндотелиоциты почечной мембраны выполняют еще одну весьма важную функцию - они секретируют метаболиты арахидоновой кислоты (простагландины, лейкотриены, тромбоксан), которые регулируют состояние самих этих клеток, почечный кровоток, а так же иммунные реакции в клубочках. Кроме того, костномозговое происхождение мезангиоцитов обеспечивает активное участие их в местных иммунных реакциях. Они реагируют на повреждение гломерулярного фильтрата, продуцируя вещества БМ. Гипертрофия и гиперклазия мезангиальных клеток приводит к утолщению или склерозу капилляров - гломефулосклерозу при многих гломерулопатиях (гломерулонефрит, диабетический и печеночный гломерулосклероз). Мезангиоциты, выполняя фагоцитарную функцию, очищают клубочки. Для оценки клинических процессов весьма важно то, что при патологии почек для снижения процессов фильтрации имеет значение не столько изменение различных условий в пределах одного нефрона, сколько уменьшение числа функционирующих нефронов. Кровоснабжение почек По своей интенсивности кровоснабжение почки близко к кровоснабжению эндокринных желез, так как кровь в них выполняет не только трофическую функцию, а и обеспечивает специфические функции этих органов. В норме у взрослого человека через почки проходит до 25% сердечного выброса (1000- 1200 мл/мин), и при весе обеих почек в 300 г удельный кровоток через них составляет 4 мл/мин/г. Столь обильное кровоснабжение обеспечивается анатомическими особенностями почечных артерий, отходящих непосредственно от брюшного отдела аорты в виде короткого толстого ствола. Небольшая длина каждого из последующих ветвлений почечных артерий обеспечивает высокое давление в капиллярах клубочка (около 65-70 мм рт.ст.). Поддержанию высокого давления способствует и меньший диаметр выносящего сосуда, создающий повышенное сопpотивление кpовотоку. Так как капилляры клубочков не выполняют трофическую функцию, а обеспечивает процесс фильтрации, то кровь, выходящая из капсулы, остается артериальной, то есть содержит практически столько же газов, сколько и входящая. Уже в коре выносящая артериола вновь распадается на капилляры и вокруг извитых отделов канальцев, расположенных в корковом отделе, образуется густая сеть капилляров. В отличие от этого капилляры, сопровождающие канальцы мозгового слоя, образуют прямые, редко ветвящиеся сосуды. Все эти повторно образующиеся капилляры выполняют как мочеобразовательную, так уже и трофическую функции. Низкое давление (около 13 мм рт. ст.) в перитубулярных капиллярах обеспечивает их активное участие в процессах реабсорбции. Антидиуретический гормон Одним из основных гормонов, обеспечивающих контроль интенсивности факультативной реабсорбции воды в дисталнх отделах нефронов, является АДГ (вазопрессин) гипофиза. Основным стимулом образования АДГ является рефлекторный - через осморецепторы, находящиеся в ткани мозга около третьего желудочка и супраоптического ядра. Возбуждаются они при увеличении (достаточно и 1%) осмомолярности внеклеточной жидкости (тем самым контролируется и осмотическое давление крови). Это возбуждение передается нейронам супраоптического ядра гипоталамуса, регулируя здесь выделение АДГ. В этой области мозга нетипично высока проницаемость гемаэнцефалического барьера, что позволяет растворенным веществам перемещаться из плазмы в цереброспинальную жидкость, окружающую осморецепторы. Объемный механизм (через ОЦК), а также барорецепторный механизм также присутствуют, но для их реализации требуется более значимые изменения ОЦК – не менее 10 % снижения ОЦК или артериального давления. АДГ в крови быстро разрушается (Т1/2 около 25 с), так что для сохранения высокого уровня реабсорбции воды требуется постоянное поступление из гипофиза все новых порций его. Недостаточное образование АДГ может быть следствием нарушения гипоталамо-гипофизарных механизмов, что приводит к несахарному диабету - выделению большого количества мочи.
Рис. 80. Схема регуляции функций почки при восстановлении осмотического давления к. ПНУГ - предсердный натрийуретический гормон.
АДГ - сберегающий воду гормон. Под его влиянием в дистальных отделах неровифрона создаются условия для удержания воды в организме. Взаимодействие гормона с V2-рецепторами приводит к активации аденилатциклазы и увеличению в клетках образования цАМФ. Последняя диффундирует на противоположный конец клетки к апикальной мембране, где совместно с кальцием активирует проницаемость мембраны для воды. Такой механизм реализуется в собирательных трубочках. В дистальных канальцах под влиянием АДГ происходит выход из клетки гиалуронидазы, расщепляющей гиалуроновую кислоту межклеточного пространства. В результате прoницаемость эпителия канальцев и собирательных трубочек для воды возрастает и она получает возможность легко поступать из фильтрата в паренхиму почки. В отличие от этого взаимодействие гормона с V1 рецептором приводит к образованию внутри клеток других вторичных мессенджеров: инозитолтрифосфата и диацилглицерола. Эти посредники являются регуляторами уровня внутриклеточного цАМФ - они понижают его. Наиболее выражено это влияние на кровеносных сосудах, которые суживаются. Данным путем вазопрессин косвенно так же оказывает свое влияние и на процессы мочеобразования. Таким образом, двумя путями вазопрессин с помощью двух типов рецепторов не просто повышает проницаемость мембраны для воды, но оказывает регулирующее влияние на эти процессы. Но при действии АДГ лишь создаются условия для реабсорбции воды. Само же движение ее определяется соотношением ионов в моче и межклеточной жидкости. Обычно когда в паренхиме почек, окружающей дистальные канальца и особенно собирательные трубочки, осмотическое давление высокое, то вода выходит из фильтрата и задерживается в организме. Однако, если по какой-либо причине на предыдущих этапах не произойдет достаточной реабсорбции ионов и концентрация их в поступившей сюда моче останется высокой, то, несмотря на присутствие АДГ, диурез будет повышенным. Гиперосмия «не выпустит» воду из канальца. Таким путем, например, возникает полиурия при сахарном диабете, когда в моче остается нереабсорбированная глюкоза. Гормональная регуляция реабсорбции ионов. На пpоцесс реабсорбции воды в дистальных отделах нефрона оказывает влияние также и реабсорбция Nа+ и Сl-. Если Nа+ будет задерживаться в моче, то одновременно будет затруднена и реабсорбция воды. Реабсорбцию Nа+ в свою очередь регулиpуют альдостерон - гормон коркового вещества надпочечников и натрийуретические гормоны предсердий.
Рис. 81. Механизм действия альдостерона в клетке эпителия канальцев.
Натрийуретические петиды
|
|||||||||
|
Последнее изменение этой страницы: 2017-01-27; просмотров: 498; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.150.80 (0.067 с.) |
 Одновременно происходит постепенное обновление всей воды организма. Для обновления используется как "внешняя" вода, поступающая через желудочно-кишечный тракт, так и "эндогенная", образующаяся в процессе метаболизма. При окислении 100 г жира образуется более 100 мл воды, 100 г белка - около 40 мл, 100 г углеводов - 55 мл воды. Естественно, что с повышением уровня метаболических процессов параллельно возрастает и образование "воды окисления". Однако, у человека эндогенной воды недостаточно для обеспечения метаболизма водной среды, поэтому требуется ее постоянное поступление и обновление. Вся вода организма обновляется примерно за месяц, а наиболее мобильная внеклеточная - примерно за неделю.
Одновременно происходит постепенное обновление всей воды организма. Для обновления используется как "внешняя" вода, поступающая через желудочно-кишечный тракт, так и "эндогенная", образующаяся в процессе метаболизма. При окислении 100 г жира образуется более 100 мл воды, 100 г белка - около 40 мл, 100 г углеводов - 55 мл воды. Естественно, что с повышением уровня метаболических процессов параллельно возрастает и образование "воды окисления". Однако, у человека эндогенной воды недостаточно для обеспечения метаболизма водной среды, поэтому требуется ее постоянное поступление и обновление. Вся вода организма обновляется примерно за месяц, а наиболее мобильная внеклеточная - примерно за неделю. Осмотическое и онкотическое давления обеспечивают, с одной стороны, обмен воды между плазмой крови и тканями, а с другой - с форменными элементами самой крови. При нарушении осмотического или онкотического давления в плазме или клетках может изменяться функция клеток крови и продолжительность их жизни. Так, при понижении осмотического давления плазмы вода будет поступать в клетки крови, что при достижении предела растяжимости приведет к разрыву их оболочки - осмотическому гемолизу. Особенно это опасно для эритроцитов. Разрушение даже части их понизит возможность функциональной системы транспорта О2. Но не менее важно и то, что при поступлении в плазму большого количества гемоглобина может сказаться токсическое влияние, как самого гемоглобина, так и продуктов его метаболизма на многие жизненно важные органы (и в первую очередь на почки). Напротив, повышение осмотического давления плазмы приведет к выходу жидкости из клеток, потере упругости, сморщиванию их (рис. 74). Это также отpицательно отpазится на жизнедеятельности клеток и может привести к их разрушению макрофагами тканей.
Осмотическое и онкотическое давления обеспечивают, с одной стороны, обмен воды между плазмой крови и тканями, а с другой - с форменными элементами самой крови. При нарушении осмотического или онкотического давления в плазме или клетках может изменяться функция клеток крови и продолжительность их жизни. Так, при понижении осмотического давления плазмы вода будет поступать в клетки крови, что при достижении предела растяжимости приведет к разрыву их оболочки - осмотическому гемолизу. Особенно это опасно для эритроцитов. Разрушение даже части их понизит возможность функциональной системы транспорта О2. Но не менее важно и то, что при поступлении в плазму большого количества гемоглобина может сказаться токсическое влияние, как самого гемоглобина, так и продуктов его метаболизма на многие жизненно важные органы (и в первую очередь на почки). Напротив, повышение осмотического давления плазмы приведет к выходу жидкости из клеток, потере упругости, сморщиванию их (рис. 74). Это также отpицательно отpазится на жизнедеятельности клеток и может привести к их разрушению макрофагами тканей. В норме существует определенная периодичность функционирования нефронов: не все нефроны функционируют одновременно, одни из них “работают” - другие нет. С одной стороны, в этом проявляется функциональная избыточность, дублирование структур, общая для всех органов. Однако, с другой стороны, местоположение клубочкового аппарата капсулы Боумена-Шумлянского существенно отражается на функции канальцевого аппарата, который осуществляет реабсорбцию из первичного фильтрата не только веществ, поступивших туда «по ошибке», которые необходимо удержать в организме, но и воды. Чем глубже залегает нефрон, тем дальше в мозговое вещество заходит петля Генле, а это обеспечивает более интенсивный процесс реабсорбции в ней воды и NaCl, так как проявляется зависимость от онкотического давления в паренхиме: чем глубже в мозговой слой, тем оно выше). Тем самым в системе почечного кровотока создается возможность регулировать состав выводимой мочи, включая один тип нефронов или другой.
В норме существует определенная периодичность функционирования нефронов: не все нефроны функционируют одновременно, одни из них “работают” - другие нет. С одной стороны, в этом проявляется функциональная избыточность, дублирование структур, общая для всех органов. Однако, с другой стороны, местоположение клубочкового аппарата капсулы Боумена-Шумлянского существенно отражается на функции канальцевого аппарата, который осуществляет реабсорбцию из первичного фильтрата не только веществ, поступивших туда «по ошибке», которые необходимо удержать в организме, но и воды. Чем глубже залегает нефрон, тем дальше в мозговое вещество заходит петля Генле, а это обеспечивает более интенсивный процесс реабсорбции в ней воды и NaCl, так как проявляется зависимость от онкотического давления в паренхиме: чем глубже в мозговой слой, тем оно выше). Тем самым в системе почечного кровотока создается возможность регулировать состав выводимой мочи, включая один тип нефронов или другой. Подоциты, отходящими из перинуклеарной зоны большими отростками, напоминают “подушки”, охватывающие значительную поверхность капилляра (рис. 75-А). Малые их отростки отходят от больших и, переплетаясь, закрывают все свободное от больших отростков пространство капилляра. Межпедикулярное пространство составляет 25-30 нм. Оно занято фибриллярными структурами, образующими щелевую диафрагму, своеобразную решетку - систему пор величиной 5-12 нм. Снаружи щелевая диафрагма покрыта гликокаликсом. Внутри указанная диафрагма граничит с базальной мембраной (БМ).
Подоциты, отходящими из перинуклеарной зоны большими отростками, напоминают “подушки”, охватывающие значительную поверхность капилляра (рис. 75-А). Малые их отростки отходят от больших и, переплетаясь, закрывают все свободное от больших отростков пространство капилляра. Межпедикулярное пространство составляет 25-30 нм. Оно занято фибриллярными структурами, образующими щелевую диафрагму, своеобразную решетку - систему пор величиной 5-12 нм. Снаружи щелевая диафрагма покрыта гликокаликсом. Внутри указанная диафрагма граничит с базальной мембраной (БМ). На базолатеральных мембранах клеток канальцев и собирательных трубочек имеется два типа рецепторов к вазопрессину: V1 и V2. Через V1-рецепторы осуществляется преимущественно вазоконстрикторый и другие эффекты гормон. А V2-рецепторы реализуют гидроосмотическое влияние гормона.
На базолатеральных мембранах клеток канальцев и собирательных трубочек имеется два типа рецепторов к вазопрессину: V1 и V2. Через V1-рецепторы осуществляется преимущественно вазоконстрикторый и другие эффекты гормон. А V2-рецепторы реализуют гидроосмотическое влияние гормона.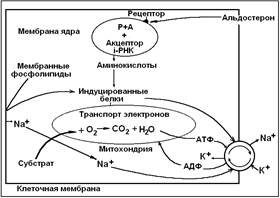 Снижение концентрации Nа+ в кpови стимулирует образование альдостерона, который cоздает условия для активной реабсорбции Nа+ эпителиальными клетками дистальных отделов нефрона. В основе влияния альдостерона лежит регуляция биосинтеза Na,K-АТФазы в указанных клетках. Активное откачивание Na+ из клеток обеспечивает процесс поступления иона в клетки из фильтрата (рис. 81). Интенсивность секреции альдостеpона зависит также от уpовня ангиотензина II в кpови.
Снижение концентрации Nа+ в кpови стимулирует образование альдостерона, который cоздает условия для активной реабсорбции Nа+ эпителиальными клетками дистальных отделов нефрона. В основе влияния альдостерона лежит регуляция биосинтеза Na,K-АТФазы в указанных клетках. Активное откачивание Na+ из клеток обеспечивает процесс поступления иона в клетки из фильтрата (рис. 81). Интенсивность секреции альдостеpона зависит также от уpовня ангиотензина II в кpови.


