Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Штами, дефіцитні по фруктокиназе, сбраживают глюкозу до еталона, при цьому в середовищі накопичується фруктоза, що дозволяє одержати із сахарози этанол і фруктозу.
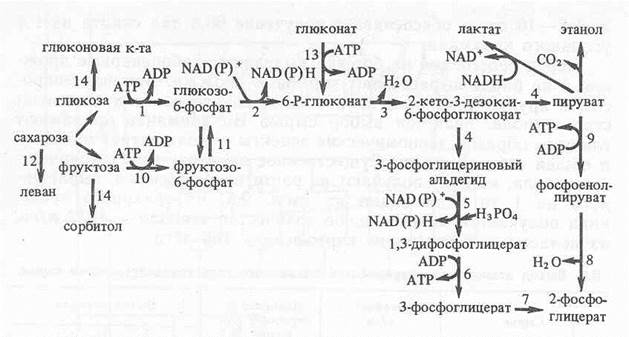
Рис. 2. Схема катаболізму в Zymomonas mobіlіs: Глюкокиназа, 6- фосфатдегидрогеназа, фосфоглюконатдегидро- геназа, 4- 6- фосфоглюконатальдолаза; 5 - дегидрогеназа фосфо- гліцеринового альдегіду; 6 - фосфоглицераткиназа, 7- фосфоглицеромутаза, 5- енолаза, 9 - пируваткиназа, 10 - фруктокиназа, 11- фосфогексоизомераза, 12 - левансахараза, 13 - глюконокиназа, 14 – глюкозофруктозотрансгидрогеназа Тому що швидкість росту біомаси Zymomonas mobіlіs невелика, у середовищі звичайно накопичується 2-3 г/л біомаси, що негативно впливає на продуктивність системи. У зв'язку із цим практикують або штучну іммобілізацію кліток, або використовують флокулирующие штами, наприклад штамом ZM-4, отриманим П. Роджерсом, Л. Аркури із сотр. Використовуючи іммобілізовані клітки Zymomonas mobіlіs у середовищі, що містить 10 % глюкози, досяглися в противоточном режимі продуктивності системи по этанолу 152 г/(л-ч). Максимальна продуктивність при роботі з Saccharomyces cerevіsіae 80 г/ (л x ч). На жаль, на мелассных середовищах продуктивність Z. mobіlіs нижче. Великі успіхи по одержанню этанола при культивуванні Z. mobіlіs досягнуті в Канаді (Н. Lawford et. al., 1989). У результаті цілеспрямованої селекції флокулирующего штаму й оптимізації процесу ферментації продуктивність системи по этанолу становить до 200 г/(л-ч), що майже на 2 порядку перевищує продуктивність ферментаційного процесу на більшості спиртових заводів. При одержанні этанола хімічним шляхом з этилена продуктивність становить 80 г/(л-ч). Зараз у біотехнології этанола широко застосовують флокулирующие штами, які дозволяють підвищити концентрацію біомаси до 40-60 г/л. Однак виникають проблеми, пов'язані з інтенсивним виділенням диоксида вуглецю, який коалестирует і порушує гомогенность процесу. Щоб запобігти цим небажаним явищам створена багатоступінчаста вертикальна колона. Усередині неї встановлений ряд усічених конусів, звернених більшою підставою до верху. Через нижній отвір конуса нагору піднімається рідка фаза із продуцентом, а газ накопичується в просторі між верхньою зовнішньою частиною конуса й циліндром. Звідти через патрубок виводиться З2 з биореактора в загальний вертикальний колектор. При переробці мелассы тростинного цукру з концентрацією цукру 160 г/л за допомогою флокулирующей культури Saccharomyces uvapum биореактор працює 460 год при D = 0,18 год -1. Зміст этанола 7-8 % об. Зміст кліток в 1 мол сброженного субстрату не більш 10. За допомогою колонного ферментатора в досвідах Кастро досягнута продуктивність по этанолу на глюкозному середовищу 22,5 г/(л-л- ч), на мелассной середовищу - 9,6 г/(л-ч), на крохмальній - 2,2 г/(л-ч). Необхідно відзначити, що при ферментації крохмалю були сполучені процеси оцукрювання за допомогою іммобілізованої амилоглюкозидазы й спиртового шумування за допомогою дріжджів.
Цікаві результати при сбраживании висококонцентрованих крохмальних субстратів отримані в умовах сполученого процесу оцукрювання й спиртового шумування за допомогою культур Rhіzopus sp. і Saccharomyces у біореакторі із циркуляцією газу. При концентрації субстрату 265 г/л через 3 сут этанола втримувалося 11 % про. Такий вихід досягається за рахунок того, що при циркуляції этанольные й водяні пари переходять у газ. Этанол з газу можна конденсувати при концентрації субстрату в системі 400 г/л, зміст этанола в конденсаті досягає 35,2 %. У зв'язку з обмеженням ресурсів традиційної сировини для виробництва этанола зараз розробляються процеси на основі нових замінників цукру. До них можна віднести синтетичний газ, одержуваний з вугілля. Як відомо, цей газ складається із CO, Н2 і CO2. Виділені бактерії, здатні конвертувати CO і Н2 до этанола згідно з рівняннями: 6CO + ЗН2О - C2Н5OH + 4CO2; 6Н2 + 2CO2 - C2Н5OН + ЗН2O. При одержанні этанола із синтетичного газу велике значення має оптимізація массообмена між газової, рідкої й твердої фазами. У колонному апарату можна одержати концентрацію этанола 2-3 %. Важливим досягненням в області раціонального використання рослинної сировини є розкриття біохімічних і генетичних основ биоконверсии ксилозы в этанол. Мікроорганізми, здатні трасформировать D- Ксилозу в этанол, повинні мати два ферменти. Перший фермент - Nadh-Зави- Симая ксилозоредуктаза - катализирует перетворення D- Ксилози в ксиліт, другий -- Nad- Залежна ксилитдегидрогеназа - окиснить ксиліт в D- Ксилулозу. Остання через пентозный шунт і по гликолизному шляхи може конвертуватися в этанол.
Однак цей біохімічний механізм важко піддається регуляції, тому методами генетичної інженерії необхідно було ввести в клітки ген, що кодує синтез ксилозоизомеразы - ферменту, що забезпечує пряму конверсію D-Кси- лози в D- Ксилулозу. Такий ген був трансплантований у дріжджі Schіzosaccharomyces pombe за допомогою ксилозоизомеразной плазмиды Е. coll. Ген інтегрувався із хромосомальной ДНК дріжджів і забезпечив експресію ксилозоизомеразы, що дозволило сбраживать ксилозу до этанола. У результаті продуктивність штаму по этанолу збільшилася з 0,063 до 0,177 г/(л-л- ч). У такий спосіб стало можливим за допомогою Schіzosaccharomyces pombe сбраживать в этанол не тільки D- Глюкозу, одержувану після гідролізу целюлози, але й D- Ксилозу, одержувану після гідролізу гемицеллюлозы.
|
||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 106; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.147.89.24 (0.006 с.) |