
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Внутренняя энергия и теплоемкость
Получим выражение для внутренней энергии и теплосодержания единицы массы жидкости. Внутренняя энергия единицы массы U зависит от параметров состояния. Так как p, V, T связаны уравнением состояния, то независимыми переменными являются только какие-нибудь два из них, и можно считать: U = U (V, T), где Отсюда полный дифференциал внутренней энергии равен
Чтобы иметь возможность проинтегрировать уравнение (3.18) и получить расчетную формулу для внутренней энергии, нужно определиться с частными производными Согласно первому закону термодинамики
где
Введем понятие удельной теплоемкости с как физической величины, численно равной количеству тепла, которое необходимо сообщить (отнять) единице массы жидкости, чтобы изменить ее температуру на 1 К:
Если тепло подводить к единице массы жидкости, сохраняя постоянным объем, то удельную теплоемкость называют теплоемкостью при постоянном объеме –
Таким образом, определился первый коэффициент уравнения (3.18). Для определения
Процессы, протекающие без теплообмена и при отсутствии потерь механической энергии, т. е. при S = const называются изоэнтропическими. С учетом уравнения (3.19) имеем следующее:
Так как dS – полный дифференциал, то накрест взятые частные производные от коэффициентов при dT и dV должны быть равны между собой. То есть
После дифференцирования
Теперь можно получить выражения для внутренней энергии (для идеального и реального газа):
где Установим связь между теплоемкостями
Из выражения (3.19) можно записать следующее:
Тогда при p = const
Для идеальных газов Для реальных газов С учетом полученных зависимостей выражение для теплосодержания единицы массы неподвижного идеального газа (энтальпии) следующие:
Считая, что
Получим выражение для энтропии идеального газа. Так как
После интегрирования получаем следующее:
Если рассматривается изоэнтропический или адиабатический процесс, для которого характерно постоянство энтропии (S = const), то и второе слагаемое в выражении (3.21) должно быть неизменным, т. е.
Выражение (3.22) носит название адиабаты Пуассона, и в соответствии с этим показатель степени в этом выражении k называют показателем адиабаты. Соотношение (3.22) имеет место в частице, и Предположение о постоянстве
Интегралы дифференциальных уравнений Эйлера
В общем виде дифференциальные уравнения движения Эйлера не интегрируются. Их интегралы можно найти только для некоторых частных случаев. Рассмотрим порядок нахождения интегралов: 1) для потенциального неустановившегося движения; 2) для установившегося непотенциального движения сжимаемого газа.
|
||||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 157; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.221.15.15 (0.014 с.) |
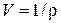 .
.
 . (3.18)
. (3.18)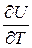 и
и  .
.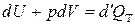 , (3.18а)
, (3.18а)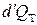 – количество тепла, получаемое единицей массы жидкости за время
– количество тепла, получаемое единицей массы жидкости за время  (
( , имеем следующее:
, имеем следующее: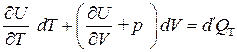 . (3.19)
. (3.19) .
. если тепло подводить при p = const – то теплоемкостью при постоянном давлении –
если тепло подводить при p = const – то теплоемкостью при постоянном давлении –  В условиях, далеких от сжижения газов, теплоемкость зависит от температуры газа и почти не зависит от давления. Тогда выражение для
В условиях, далеких от сжижения газов, теплоемкость зависит от температуры газа и почти не зависит от давления. Тогда выражение для 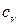 имеет вид
имеет вид .
. воспользуемся выражением для дифференциала энтропии. Энтропия – это функция, которая определяется следующим дифференциальным уравнением:
воспользуемся выражением для дифференциала энтропии. Энтропия – это функция, которая определяется следующим дифференциальным уравнением: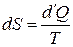 .
. .
. .
. и сокращения получаем
и сокращения получаем  . Для дальнейшего преобразования воспользуемся уравнением состояния. Для идеальных газов
. Для дальнейшего преобразования воспользуемся уравнением состояния. Для идеальных газов 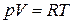 . Отсюда
. Отсюда  , т. е.
, т. е.  и
и 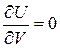 . Для реальных газов, подчиняющихся уравнению состояния Ван-дер-Ваальса
. Для реальных газов, подчиняющихся уравнению состояния Ван-дер-Ваальса .
. (3.20)
(3.20) – внутренняя энергия жидкости при температуре Т = 0 К; для идеального газа
– внутренняя энергия жидкости при температуре Т = 0 К; для идеального газа 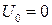 .
. и
и  и
и  .
. .
.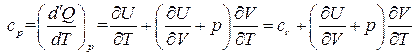 .
. и
и  . Отсюда
. Отсюда 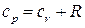 . Отношение удельных теплоемкостей обозначим
. Отношение удельных теплоемкостей обозначим 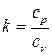 , тогда
, тогда 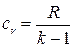 , а
, а  .
. ,
, 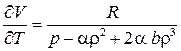 и
и 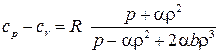 .
. .
.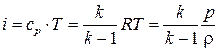 .
. ,
, 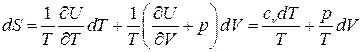 ,
,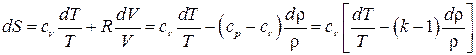 ,
, .
. . (3.21)
. (3.21) . (3.22)
. (3.22) может изменяться от частицы к частице. При установившемся движении
может изменяться от частицы к частице. При установившемся движении  на линии тока.
на линии тока. и
и 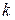 зависит от структуры молекул газа: для одноатомных газов
зависит от структуры молекул газа: для одноатомных газов 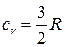 и
и 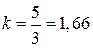 ; для двухатомных, к которым можно отнести и воздух,
; для двухатомных, к которым можно отнести и воздух,  и
и  ; для трехатомных
; для трехатомных 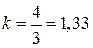 .
.


