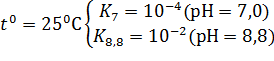Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт 13. Изучение участия пиридиннуклеотидов в биохимических реакциях окисления-восстановления.Содержание книги
Поиск на нашем сайте
Теоретическое введение. Пиридиннуклеотиды, входящие в качестве коферментов в состав более чем 150 так называемых «пиридинзависимых» дегидрогеназ, играют существенную роль в реакциях окисления-восстановления (главным образом, в процессе дыхания, т. е. в процессе переноса электронов от органических субстратов к молекулярному кислороду). Спектрофотометрическое определение восстановленных пиридиннуклеотидов служит в связи с этим одним из важных методов современной энзимологии. В основе метода лежит существенное отличие спектров окисленной и восстановленной форм кофермента. Спектр поглощения окисленной формы — NAD+ имеет максимум при 260 нм. Для восстановленной формы — NADH характерен более длинноволновый максимум поглощения — при 340 нм. Измеряя в ходе окислительно-восстановительной реакции оптическую плотность объекта при 340 им, можно установить (зная коэффициент поглощения и длину кюветы) количество нуклеотида в пробе. С другой стороны, учитывая, что окисление-восстановление 1 мкмоля кофермента сопровождается восстановлением-окислением 1 мкмоля субстрата, этим же методом можно определить количество прореагировавшего субстрата. Исследуемая реакция протекает по следующей схеме: фермент субстрат + NAD+ ---------------→ продукт реакции + NADH Как правило, все компоненты, кроме определяемого, присутствуют в избытке. В расчетах исходят из величины коэффициента молярной экстинкции NADH: при окислении 1 мкмоль кофермента в 1 мл смеси оптическая плотность при 340 нм в кювете толщиной 1 см меняется на 6,22 ед. Количество определяемого вещества в пробе (в мкмолях) М рассчитывается по формуле:
где ∆D340 — изменение оптической плотности смеси при 340 нм; V — объем пробы (мл). Энзиматический метод количественного определения
Принцип метода. NAD восстанавливается в присутствии этанола и алкогольдегидрогеназы. Количество образовавшегося NADH равно исходном количеств NAD+ и определяется спектрофотометрически: При рН = 8,8 и концентрации спирта 0,5 М можно получить практически полное восстановление NAD+. Реактивы. 1 Этанол 0,5 М, приготовленный на 0,1 М трис-буфере с рН= 10,1 (молекулярная масса этанола 46,07). 2. Алкогольдегидрогеназа: растворить в 1—2 мл дистиллята 1—2 мг белка непосредственно перед использованием. В случае использования суспензии учесть, что одной ферментной единицы (см. обозначения на упаковке белка) достаточно для полного превращения 1 мкмоля субстрата в 3. Раствор NAD+: 1—2 мл концентрации 1- 4 мМ; рН = 6,5 (молекулярная масса NAD+=633). Процедура определения. В две спектрофотометрические кюветы помещают по 0,39 мл Н2O (дистиллят); 2,5 мл раствора этанола 0,5 М на Измеряют по точкам спектры поглощения растворов в опытной кювете и в контрольной для области 220—380 нм с шагом 5 нм. Учитывая поглощение контроля, оценивают ∆D340 в опытной кювете. Рассчитывают количество NADH в растворе и количество прореагировавшего NAD+. Последнюю величину сравнивают с исходной. Спектры поглощения, снятые по точкам, необходимо представить в виде таблиц и графиков (ордината — D, абсцисса — λ в нм).
Практическое задание 1. Кофермент А принимает участие в качестве кофактора во многих ферментативных реакциях протекающих в организме человека и животных. Перепишите формулу кофермента А в тетрадь:
Карандашом обведите формулу пантотеновой кислоты в составе кофермента, также укажите в его составе аденин и рибозу. 2. В состав кофермента ФАД входит витамин рибофлавин. Перепишите в тетрадь формулу ФАД:
Карандашом обведите формулу рибофлавина. 3. Витамин никотинамид входит в состав кофермента НАД:
В тетрадь перепишите формулу НАД, карандашом обведите формулу витамина.
Вопросы для проверки полученных знаний
3. БИОЛОГИЧЕСКИ ВАЖНЫЕ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
|
||||
|
Последнее изменение этой страницы: 2016-12-16; просмотров: 574; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.27 (0.009 с.) |