
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Строение атома и периодический закон Д. И. МенделееваСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Строение атомов 1. Какой элемент имеет в атоме три электрона, для каждого из которых главное квантовое число n = 3 и орбитальное квантовое число l = 1? Чему равны для этих электронов значения магнитного ml и спинового mS квантовых чисел? 2. Валентные электроны атома химического элемента характеризуются следующим набором квантовых чисел n, l, ml и mS соответственно: 5, 0, 0, +1/2; 5, 0, 0, -1/2; 5, 1, 1, +1/2; 5, 1, 0, +1/2. О каком элементе идет речь? Составьте электронную формулу его иона, находящегося в высшей степени окисления. 3. Составьте электронную формулу иона таллия Tl3+. Для валентных электронов атома Tl укажите набор всех четырех квантовых чисел. 4. Напишите полное уравнение ядерной реакции 5. Для элемента Х даны энергии ионизации (кДж·моль-1): I1 = 1402; I2 = 2856; I3 = 4578; I4 = 7475; I5 = 9445; I6 = 53266. В какой группе периодической системы находится элемент Х? Ответ обоснуйте. 6. Для элемента Х получены следующие значения энергий ионизации (кДж·моль-1): I1 = 801; I2 = 2427; I3 = 3660; I4 = 25026; I5 = 32827. Определите наиболее вероятную формулу оксида элемента Х. Выбор обоснуйте. 7. Среди указанных наборов квантовых чисел укажите те, которые корректно определяют орбиталь атома: 1) 2, 1, -1, +1/2; 2) 1, 1, 0, +1/2; 3) 3, 1, -1, +1/2. Ответ обоснуйте. 8. Сколько неспаренных электронов содержат невозбужденные атомы а) B; б) S; в) As; г) Cr; д) Hg; е) Eu? Дайте обоснованный ответ. Составьте электронно-графическую формулу и объясните особую устойчивость иона Fe3+ (по сравнению с ионом Fe2+). 9. У элементов каких периодов электроны внешнего слоя характеризуются значением суммы главного и орбитального квантового чисел n+l = 5? Укажите значения всех квантовых чисел для валентных электронов атома иттрия. 10. Какие из следующих изотопов (их два) неустойчивы: 67Zn, 101Rh, 32Mg, 43Ca, 141La? Ответ поясните. Для неустойчивых изотопов укажите тип и количество частиц, испускание которых приведет к образованию устойчивого изотопа. Какие устойчивые изотопы образуются? 11. Сколько электронов и сколько протонов входит в состав следующих частиц: а) 12. Напишите уравнение реакции образования соединения, в состав которого входят только ионы элементов с конфигурацией внешних электронов 3s23p6. Какова масса всех электронов, содержащихся в 100г этого вещества? (Масса электрона равна 1/1832 а.е.м). 13. Химический элемент имеет в атоме 4 электрона, для каждого из которых главное квантовое число n = 2 и орбитальное квантовое число l = 1. Чему равны для этих электронов значения магнитного ml и спинового mS квантовых чисел? О каком элементе идет речь? 14. Валентные электроны атома химического элемента характеризуются следующим набором квантовых чисел n, l, ml и mS соответственно: 3, 2, 2, +1/2; 4, 0, 0, +1/2; 4, 0, 0, -1/2. О каком элементе идет речь? Составьте электронную формулу его иона, находящегося в высшей степени окисления. 15. Составьте электронную формулу иона In3+. Для валентных электронов атома In укажите набор всех четырех квантовых чисел. 16. Среди указанных наборов квантовых чисел укажите те, которые корректно определяют орбиталь атома: 1) 1, 0, 0, +1/2; 2) 2, 2, 1, -1/2; 3) 2, 1, -1, +1/2. Ответ обоснуйте. 17. Сколько неспаренных электронов содержат невозбужденные атомы а) Fe; б) Kr; в) Te; г) W? Дайте обоснованный ответ. Какие общие свойства имеют элементы Mn и Cl? 18. У элементов каких периодов электроны внешнего слоя характеризуются значением суммы главного и орбитального квантового чисел n+l = 4? Укажите значения всех квантовых чисел для валентных электронов атома кремния. 19. Сколько электронов и сколько протонов входит в состав следующих частиц: а) 20. Химический элемент состоит из двух изотопов. Ядро первого изотопа содержит 10 протонов и 10 нейтронов. В ядре второго изотопа нейтронов на 2 больше. На 9 атомов легкого изотопа приходится один атом более тяжелого изотопа. Вычислите среднюю атомную массу элемента.
|
||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 681; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.15 (0.008 с.) |

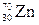 [p, n]? Для валентных электронов атома образовавшегося изотопа укажите набор квантовых чисел.
[p, n]? Для валентных электронов атома образовавшегося изотопа укажите набор квантовых чисел.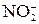 ; б) PH3? Для валентных электронов атома фосфора укажите набор всех четырех квантовых чисел.
; б) PH3? Для валентных электронов атома фосфора укажите набор всех четырех квантовых чисел. ; б) KBr? Для валентных электронов атома серы укажите набор всех четырех квантовых чисел.
; б) KBr? Для валентных электронов атома серы укажите набор всех четырех квантовых чисел.


