Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Хронические осложнения сахарного диабета
Диабетические микроангиопатии Поражения сосудов микроциркуляторного русла при сахарном диабете являются его частыми осложнениями. Развиваются морфологические изменения всех без исключения сосудов микроциркуляторного русла, но чаще всего – сосудов почек, сетчатки глаза и сосудов, питающих нервы. Появление этих осложнений начинается с развития дисфункции эндотелиоцитов кровеносных сосудов, а затем и повреждения этих клеток. Под дисфункцией эндотелия понимают потенциально обратимые нарушения функций этих клеток, характеризующиеся следующими признаками: · нарушением баланса между образованием и/или действием веществ с сосудорасширяющими свойствами (оксида азота NO; веществ, вызывающих гиперполяризацию и расслабление гладкомышечных клеток кровеносных сосудов; простациклина) и сосудосуживающими свойствами (эндотелина-1 и ангиотензина II) в пользу преобладания последних; · утратой атромбогенных свойств эндотелиоцитов и склонностью к увеличению тромбообразования; · усилением адгезии активированных лейкоцитов к эндотелию и развитием воспаления в сосудистой стенке. Появление и прогрессирование этих нарушений во многом объясняет высокую встречаемость заболеваний сердечно-сосудистой системы у пациентов с сахарным диабетом. Нарушения морфологических и функциональных свойств эндотелиоцитов при сахарном диабете обусловлены, в первую очередь, тем, что при внеклеточной гипергликемии эндотелиоциты не способны ограничивать транспорт глюкозы в них. Таким образом, у пациентов, страдающих сахарным диабетом, содержание глюкозы в эндотелиоцитах значительно возрастает. Это сопровождается изменением функционирования внутриклеточных сигнальных путей в эндотелиоцитах и развитием дисфункции эндотелиоцитов. Далее, развивается повреждение эндотелиоцитов, могут стимулироваться процессы их гибели в результате апоптоза, повышается сосудистая проницаемость, развивается воспаление в сосудистой стенке, происходит гибель перицитов, нарушаются эластические свойства сосудов микроциркуляторного русла, развиваются микротромбозы этих сосудов с последующим гиалинозом и склерозом с исходом в капиллярно-трофическую недостаточность. Патогенез диабетических микроангиопатий представлен на рис. 13. Рассмотрим отдельные звенья патогенеза этих осложнений подробнее.
Активация полиолового пути метаболизма глюкозы Этот путь, включающийся в метаболические процессы при сахарном диабете, наиболее изучен в эндотелиоцитах, а также в клетках нервной ткани. Ключевым ферментом этого пути является альдозоредуктаза, которая превращает токсические альдегиды в спирты (рис. 14). Степень сродства альдозоредуктазы к глюкозе обычно низкая, но при гипергликемии альдозоредуктаза использует ее в качестве субстрата, превращая глюкозу в сорбитол. При этом содержание НАДФН и миоинозитола в клетках уменьшается. Дефицит НАДФН способствует нарушению регенерации окисленного глутатиона, что, наряду с повышением продукции активных форм кислорода при сахарном диабете, способствует развитию «окислительного» стресса и повреждению клеток. Кроме того, образовавшийся сорбитол плохо проникает через клеточную мембрану,и поэтому накапливается в клетках. Поскольку сорбитол – осмотически активное вещество, увеличение его концентрации в клетках приводит к развитию внутриклеточного отека и нарушению функциональных свойств эндотелиоцитов. Расстояние между эндотелиоцитами увеличивается, и возрастает сосудистая проницаемость. Формированию внутриклеточного отека способствует и то, что в условиях гипергликемии развивается активация протеинкиназы С, которая способствует повышению активности фосфолипазы А2. Под действием этого фермента могут образовываться эндогенные ингибиторы Na+/K+-АТФазы. В результате действия этого механизма в клетках возрастает содержание ионов Na+, и внутриклеточный отек прогрессирует.
Рис. 13. Важнейшие механизмы развития диабетических микроангиопатий
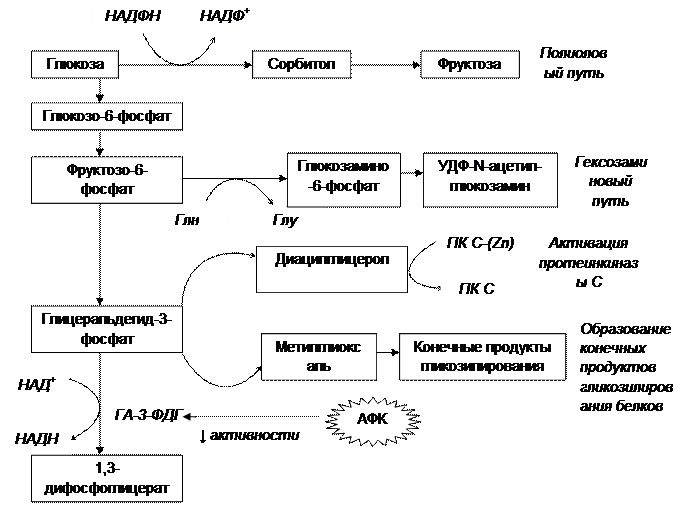
Рис. 14. Активация альтернативных путей метаболизма глюкозы при увеличении ее содержания в эндотелиоцитах кровеносных сосудов, клетках почечных клубочков и клетках нервной ткани при сахарном диабете (в соответствии с Brownlee M., Aiello L.P., Cooper M.E., et al., 2008)
Условные сокращения: глн – глицин, глу – глутамин, ПК С - протеинкиназа С, АФК – активные формы кислорода, ГА-3-ФДГ - глицеральдегид-3-фосфат-дегидрогеназа
2.2.1.2. Увеличение образования конечных продуктов Гликозилирования В условиях гипергликемии глюкоза без участия ферментов, т.е. неферментативным путем способна взаимодействовать с аминогруппами белков с образованием нестабильных промежуточных продуктов (оснований Шиффа). При дальнейшей модификации их структуры основания Шиффа превращаются в более стабильные конечные продукты гликозилирования белков – продукты Амадори. В настоящее время принято считать, что в механизмах развития диабетических ангиопатий, а также других осложнений сахарного диабета, лежит образование конечных продуктов гликозилирования белков не столько внеклеточно, сколько внутриклеточно, т.к. скорость образования последних значительно выше. Внутри клеток могут протекать следующие реакции, способствующие образованию конечных продуктов гликозилирования белков: · глюкоза способна аутоокисляться с образованием глиоксаля; · стабильные продукты Амадори могут распадаться под действием фермента амадориазы до 3-дезоксиглюкозона; · глицеральдегид-3-фосфат может превращаться в метилглиоксаль (рис. 21). Образовавшиеся дикарбонилы способны взаимодействовать с аминогруппами не только внутриклеточных, но и внеклеточных белков с образованием конечных продуктов гликозилирования белков. Эти продукты разрушаются различными редуктазами. При преобладании скорости образования конечных продуктов гликозилирования белков над скоростью их разрушения они накапливаются и оказывают патогенное действие. Примером гликозилирования белков у пациентов с сахарным диабетом может быть образование гликозилированного гемоглобина (HbA1c). Регулярный контроль содержания в крови пациентов гликозилированного гемоглобина позволяет ретроспективно судить об адекватности соблюдения пациентом диеты и о достаточности либо недостаточности вводимой доза инсулина. При повышении содержания в крови HbA1c у пациента можно сделать заключение о недостаточно эффективных лечебных мероприятиях в течение последних нескольких месяцев, т.к. продолжительность жизни эритроцита составляет около 120 дней. Вместе с тем, при адекватной терапии и снижении концентрации HbA1c хотя бы на 1% от исходной, вероятность развития микроангиопатий уменьшается на 25-35%. Накопление конечных продуктов гликозилирования белков и липидов способствует повреждению сосудов микроциркуляторного русла, так как при этом: 1. Изменяется функциональная активность факторов транскрипции и нарушается характер экспрессии генов в эндотелиоцитах. В результате баланс между образованием проангиогенных, например, эндотелиоцитарного фактора роста, и антиангиогенных факторов (в частности, ангиопоэтина-2) смещается в пользу преобладания последних. Это способствует нарушению процессов неоангиогенеза. 2. Изменяются свойства гликозилированных белков соединительнотканного матрикса. При взаимодействии конечных продуктов гликозилирования белков с молекулами коллагена I типа они становятся «упакованы» более компактно, что приводит не только к снижению эластичности кровеносных сосудов, но и к нарушению транскапиллярного обмена. Продукты гликозилирования белков также связываются и с другими белками, входящими в состав сосудистой стенки – коллагеном IV типа, ламинином и витронектином. Итогом таких взаимодействий являются нарушения прочности сосудистой стенки, утрата атромбогенных свойств эндотелия, а также нарушение механизмов регуляции сосудистого тонуса с появлением тенденции к его повышению и нарушением агонистиндуцированнного расслабления кровеносных сосудов.
3. Конечные продукты гликозилирования в настоящее время рассматривают в качестве одних из многочисленных «сигналов опасности для иммунной системы», которые способны взаимодействовать с особыми рецепторами на поверхности клеток. К настоящему времени известны несколько типов рецепторов для конечных продуктов гликозилирования, обнаруженных на поверхности макрофагов, эндотелиоцитов, мезангиальных клеток, нейронов, кардиомиоцитов и других клеток. При взаимодействии конечных продуктов гликозилирования с этими рецепторами происходит активация внутриклеточных сигнальных путей, повышается активность факторов транскрипции, в частности, ядерного фактора транскрипции NF-kb, который, перемещаясь в ядро и связываясь со специфическими участками ДНК, изменяет характер экспрессии многих генов, продукты которых участвуют в процессе воспаления. Активация протеинкиназы С Основным стимулом для повышения активности протеинкиназы С является внутриклеточное увеличение содержания глюкозы, в частности, в эндотелиоцитах. Повышение содержания глюкозы в этих клетках сопровождается стимуляцией гликолиза. Из промежуточного продукта глицеральдегид-3-фосфата, образующегося в результате гликолиза, синтезируется диацилглицерол (ДАГ), и в качестве «побочных продуктов» - активные формы кислорода (АФК). ДАГ и АФК, взаимодействуя с регуляторным доменом протеинкиназы С, способствуют высвобождению ионов цинка из «цинкового пальца» этого домена, богатого цистеиновыми остатками. В итоге повышается активность нескольких изоформ протеинкиназы С. Существует еще один путь активации этого фермента – посредством фосфорилирования тирозиновых остатков в составе протеинкиназы С, однако этот механизм еще недостаточно изучен. Следствия активации протеинкиназы С в эндотелиоцитах при сахарном диабете представлены на рис. 15.
|
|||||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 255; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.44.23 (0.011 с.) |