
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Властивості розчинів сильних електролітів
Розчини сильних електролітів не підпорядковуються закону розведення, що свідчить про необоротність процесу дисоціації сильних електролітів. На-справді речовини, кристали яких побудовані з іонів, у розчинах дисоціюють повністю − їх дійсний ступінь дисоціації дорівнює одиниці. Твердження, що сильні електроліти повністю дисоціюють на іони, є основним положенням теорії розчинів сильних електролітів, для яких a повинно дорівнювати одиниці. Однак для концентрованих розчинів сильних електролітів a < 1. Тому експериментальне значення a сильних електролітів називають уявним ступенем дисоціації. Відхилення α сильних електролітів від одинці в бік менших значень пояснюється тим, що в теорії електролітичної дисоціації Арреніуса не була врахована електростатична міжіонна взаємодія в розчині, а пояснювалося все дією сил Ван-дер-Ваальса. Якщо в розчинах слабких електролітів електростатичні сили між іонами можна не брати до уваги, оскільки α<< 1, то в розчинах сильних електролітів не враховувати їх не можна,і тому вводиться коефіцієнт активності. Коефіцієнт активності речовин та іонів характеризує ступінь відхилення властивостей реального розчину від властивостей ідеального, де немає жодної взаємодії. Він є функцією концентрації розчину, природи електроліту, температури та іонної сили розчину. Можна сказати, що активність – це уявна концентрація. Ця величина позначається літерою a та розраховується за формулою a=f∙C, де f - коефіцієнт активності, C – молярна концентрація речовини. Іонна сила розчину (m) − це півсума добутку концентрації всіх іонів
Вважають, що в разі постійного значення іонної сили розчину коефіцієнти активності іонів також залишаються сталими і не залежать від їх концентрації. Оскільки не існує прямих методів визначення коефіцієнтів активності, то їх значення можна знайти шляхом розрахунку. Зокрема, для їх обчислення можна застосовувати формулу Дебая−Хюккеля:
якщо Недоліком теорії сильних електролітів є те, що їй підпорядковуються тільки розбавлені розчини. Крім того, вона не враховує хімічні процеси, які відбуваються в розчині, зокрема явище сольватації і можливі зміни внаслідок цього в активності розчинника, який теж є активним компонентом розчину.
Добуток розчинності Якщо кристали малорозчинної солі побудовані з іонів, то в розчин переходять не молекули, а іони солі. Для малорозчинної сполуки, наприклад BaSO4 або AgCl, яка знаходиться в рівновазі зі своїм насиченим розчином, рівняння динамічної рівноваги має такий вигляд: BaSO4 Û Ba2+ + SO42-, Тверда фаза Насичений розчин тобто за постійної температури за одиницю часу в розчин переходить така кількість солі, яка за цей же час із розчину випадає в осад (тверду фазу). Оскільки числове значення знаменника у виразі константи рівноваги дорівнюватиме 1 (для чистої твердої речовини), для наведеного вище зворотного процесу за постійної температури [Ba2+]∙[SO42-] = K, де К – константа рівноваги між малорозчинною сполукою та її іонами Із рівняння випливає, що в насиченому за певної температури розчині добуток концентрацій іонів малорозчинного електроліту являє собою сталу величину, яка називається добутком розчинності і позначається ДР. Тоді для насиченого розчину BaSO4 (при 250) запишемо так: ДР (BaSO4) = [Ba2+]∙[SO42-]=1∙10-10. У загальному вигляді вираз добутку розчинності насиченого розчину малорозчинної речовини KxAy, яка розпадається на іони за рівнянням KxAy Û xKy+ + yAx-, буде мати такий вигляд: ДР (KxAy) = [Ky+]x∙[Ax-]y. Наприклад, для малорозчинних у воді солей Ag2S та Ba3(PO4)2 маємо:
Виходячи з добутків розчинності (табличних даних) можна розрахувати розчинність різних важкорозчинних сполук і навпаки. Наприклад:
або Оскільки ДР сполуки за певної температури є сталою величиною, то збільшення концентрації в розчині одного з іонів, на які дисоціює дана сполука, обумовлює зменшення концентрації іншого. Так, якщо до насиченого розчину Таким чином, введення однойменних іонів у розчин малорозчинного електроліту зменшує його розчинність (це відбувається до певної межі, оскільки надлишок однойменного іона кількістю, що перебільшує 50%, починає сприяти розчиненню). Цей висновок має велике практичне значення, зокрема в кількісному аналізі, оскільки дає можливість практично повністю осаджувати той чи інший іон у вигляді малорозчинної сполуки.
|
||||||
|
Последнее изменение этой страницы: 2016-07-16; просмотров: 191; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.154.208 (0.006 с.) |
 .
. ,
,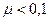 , то
, то  .
. ,
, .
.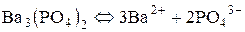 ,
, .
.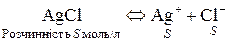 ,
,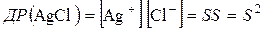

 додати розчин сполуки, яка містить іон
додати розчин сполуки, яка містить іон  , то рівновага порушиться і відповідно до принципу Ле Шателье зміститься вліво, тобто в осад почне випадати
, то рівновага порушиться і відповідно до принципу Ле Шателье зміститься вліво, тобто в осад почне випадати 


