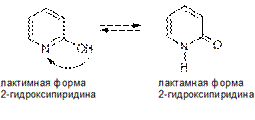Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Салициловая кислота и её производные (ацетилсалициловая кислота, фенилсалицилат). п-амино-бензойная кислота и её производные (новокаин, анестезин). Биологическая роль этих соединений.
n-Аминобензойная кислота (ПАБК) и ее производные. Эфиры ароматических аминокислот способны в той или иной степени вызывать местную анестезию. Особенно заметно это свойство у пара-производных. В медицине используют анестезин (этиловый эфир ПАБК) и новокаин (2-диэтиламиноэтиловый эфир ПАБК). Новокаин при- меняют в виде соли (гидрохлорида), что связано с необходимостью повышения его растворимости в воде.
Анестезин - одно из самых первых синтетических соединений, применяемых в качестве местноанестезирующих средств. Несмотря на более чем 100-летнее существование (синтезирован в 1890 г.; применяется с конца 90-х годов), его до сих пор относительно широко используют самостоятельно и в сочетании с другими лекарственными средствами. Недавно предложен новый аэрозольный препарат "Ампровизоль", содержащий анестезин. Анестезин является активным поверхностным местноанестезирующим средством. В связи с трудной растворимостью в воде препарат не применяют парентерально и для обезболивания при хирургических операциях. Однако его широко используют в виде мазей, присыпок и других лекарственных форм при крапивнице, заболеваниях кожи, сопровождающихся зудом, а также для обезболивания раневой и язвенной поверхности. Применяют 5 - 10 % мази или присыпки и готовые лекарственные препараты ("Меновазин", "Ампровизоль" и др.). Новокаин(прокаина гидрохлорид) - сложный эфир диэтиламиноэтанола и парааминобензойной кислоты. В медицинской практике используют в виде гидрохлорида. Обладает достаточно выраженной анестезирующей активностью, но уступает в этом отношении другим препаратам. Продолжительность инфильтрационной анестезии составляет 30 мин-1 ч. Большим преимуществом новокаина является низкая токсичность. Это относится и к его метаболитам. Через слизистые оболочки новокаин проходит плохо, поэтому для поверхностной анестезии он применяется редко (иногда для этих целей его используют в оториноларингологии в высоких концентрациях - 10% растворы). Новокаин в отличие от кокаина не суживает сосуды. Их тонус не меняется или несколько снижается, поэтому нередко в растворы новокаина добавляют адреномиметики (например, адреналин). Суживая сосуды и замедляя всасывание новокаина, адреномиметики усиливают и пролонгируют его анестезирующее действие, а также снижают его токсичность.При резорбтивном действии новокаин оказывает преимущественно угнетающее влияние на нервную систему. Обладает умеренной анальгетической активностью. В больших дозах может вызвать судороги.Влияние новокаина на сердечно-сосудистую систему проявляется гипотензивным эффектом (результат угнетающего воздействия препарата на ЦНС и симпатические ганглии), а также кратковременным противоаритмическим действием (увеличиваются эффективный рефрактерный период и время проведения по проводящей системе сердца, снижаются возбудимость и автоматизм).В организме новокаин довольно быстро гидролизуется эстеразами плазмы и тканей. Его основными метаболитами являются диэтиламиноэтанол и парааминобензойная кислота. Следует учитывать, что последняя является конкурентным антагонистом антибактериальных средств из группы сульфаниламидов. Продукты превращения новокаина выделяются почками.
Салициловая кислота и ее производные.Салициловая кислота относится к группе фенолокислот. Как соединение с орто- расположением функциональных групп она декарбоксилируется при нагревании с образованием фенола.
Салициловая кислота умеренно растворима в воде, дает интенсивное окрашивание с хлоридом железа(Ш), на чем основано качественное обнаружение фенольной гидроксильной группы. Салициловая кислота проявляет антиревматическое, жаропонижающее и антигрибковое действие, но как сильная кислота (рKа 3,0) вызывает раздражение желудочно-кишечного тракта и поэтому применяется только наружно. Внутрь применяют ее производные - соли или эфиры. Салициловая кислота способна образовывать производные по каждой функциональной группе. Практическое значение имеют салицилат натрия, сложные эфиры по карбоксильной группе - метилсалицилат, фенилсалицилат (салол), а также по гидроксильной группе - ацетилсалициловая кислота (аспирин).
Гетероциклы с одним гетероатомом. Пиррол, индол, пиридин, холин. Понятие о строении тетрапиррольных соединений (порфин, гем). Производные пиридина (никотинамид, пиридоксаль). Производные 8-оксихинолина: антибактериальные средства комплексообразующего действия. Важнейшим представителем пятичленных гетероциклов с одним гетероатомом является пиррол. К пирольным соединениям относят конденсированную систему индола и полностью насыщенный аналог пиррола – пирролидин, которые входят в состав сложных по структуре молекул хлорофиллов, гемма крови и алкалоидов, например никотина и тропана. Так в основе структуры гемма и хлорофиллов лежит тетрапиррольная система порфина. Пиррол. (C4H5N) Пиррол относится к ароматическим соединениям. Атомы углерода и азота в нем находятся в состоянии sp2-гибридизации. На негирибидизованной р-орбитали атома азота находится неподеленная пара электронов. Она участвует в сопряжении с р-электронами четырех атомов углерода с образованием единого шестиэлектроннного облака. Три sp2-гибридные орбитали образуют три σ-связи – две с атомами углерода, одну с атомами водорода. Атом азота в таком состоянии получил название пиррольного.
Индол. (С8Н7N)Индол ацидофобен и практически лишен основных свойств. Индол является структурным фрагментом белковой аминокислоты триптофана и продуктов его метаболических превращений- триптамина(С10Н12N2) и серотонина(N2ОС10Н12), относящихся к биогенным аминам. Немало синтетических производных индола приеняется в медицине, например индопан.
Пиридин. (C5H5N)Представитель ароматических гетероциклов проявляет свойства араматических соединений. Гомологи пиридина легко окисляются в соответствующие пиридинкарбоновые кислоты. Важное значение имеет окисление изомерных метилпиридинов. Основность пиридина выше, чем ароматических аминов, но ниже чем алифатических. Это связано с тем, что неподеленная пара электронов атома азота занимает sp2-гибридную орбиталь. Пиридин может вступать в реакции с нуклеофильными реагентами. Структура полностью насыщенного пиридина – пиперидина лежит в основе анальгетика промедола. Важнейшим производным пиридина являются некоторые витамины группы В, вступающие в роли структурных элементоы коферментов.
Плоский макроцикл порфина представляет собой сопряженную ароматическую систему из 26 π-электронов. Замещенные порфины называют порфиринами, один из которых – протопорфин. Порфирины в природе находятся в виде комплексов с ионами металлов. Производные порфиринов, содержащие ион железа3, называют генами. Примером может быть протогем – простетическая группа гемоглобина.
Целый ряд производных 8-оксихинолина обладает антибактериальной, противопаразитарной и противогpибковой активностью. Препараты этого ряда применяют в качестве химиотерапевтических и антисептических веществ. Солью (сульфатом) незамещенного 8-оксихинолина является давно известный препарат хинозол. жеобразованных тромбов под действием пептизаторов.
31. Гетероциклы с несколькими гетероатомами. Пиразол, имидазол, пиразин, пиримидин, тиазол, пурин. Барбитуровая кислота и её производные. Гидроксипурины (ксантин, мочевая кислота, витамин В1). Пятичленные гетероциклы с двумя гетероатомами, один из которых азот, имеют общее название азолы. Важнейшими представителями являются пиразол, имидазол, пиразин, пиримидин, тиазол, пурин. Пиразол.(C3H4N2O) Производные пиразола в природе не обнаружены. Наиболе известным производным пиразола является пиразолон. На основе пиразолона созданы анальгетические средства – анальгин, бутадион и др.
Имидазол.(С3Н4N2)Этот гетероцикл является структурным фрагментом белковой аминокислоты гистидина и продукта ее дикарбоксилирования – биогенного амина гистамина. Имидазол, конденсированный с бензольным кольцом – бензимидазол – входит в состав ряда природных веществ, в частности витамина В12, а также вазодилатируещего средства дибазола.
Пиразин.(C4H4N2) Шестичленное гетероциклическое органическое соединение с двумя атомами азота. Ароматичен. Хорошо растворим в воде, этаноле, этоксиэтане. Вступает в реакции нуклеофильного и электрофильного замещения. При аминировании амидом натрия в жидком аммиаке превращается в 2-аминопиразин. При окислении смесью уксусный ангидрид — перекись водорода, дает N-оксиды по одному или обоим азотам.
Пирамидин.(C4N2H4) Гетероциклическое соединение, имеющее плоскую молекулу, простейший представитель 1,3-диазинов. Производные пиримидина широко распространены в живой природе, где участвуют во многих важных биологических процессах. В частности, такие производные как цитозин, тимин, урацил входят в состав нуклеотидов, являющихся структурными единицами нуклеиновых кислот, пиримидиновое ядро входит в состав некоторых витаминов группы B, в частности B1, коферментов и антибиотиков. Пиримидиновая структура — как ароматическая, так и гидрированная, входит в состав многих биологически активных веществ и лекарственных препаратов — например, барбитуратов — производных 1,3,5-тригидроксипиридина, обладающих снотворным, противосудорожным и наркотическим действием.
Тиазол. (C3H3SN) В цикле тиазола содержатся два разных гетероатома. Структура тазола встречается в составе важных биологически активных веществ-тиамина и ряде сульфаниламидных препаратов, например, противомикробного средства фталозола. Цикл полностью гидрированного тиазола – тиазолидин – является структурным фрагментом пенициллиновых антибиотиков.
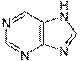
Пурин.(C5N4H4) Простейший представитель имидазо[4,5-d]пиримидинов. Бесцветные кристаллы, хорошо растворимые в воде, горячем этаноле и бензоле, плохо растворимые в диэтиловом эфире, ацетоне и хлороформе. Производные пурина играют важную роль в химии природных соединений (пуриновые основания ДНК и РНК; кофермент NAD; алкалоиды, кофеин, теофиллин итеобромин; токсины, сакситоксин и родственные соединения; мочевая кислота) и, благодаря этому, в фармацевтике.
К производным пирамидина относится барбитуровая кислота, которая может существовать в нескольких таутомерных формах. В кристаллическом состоянии барбитуровая кислота имеет строение триоксопроизводного, которое преобладает и в растворе. Барбтуровая кислота легко образует соли при действии щелочей. Её высокая кислотность, обусловлена эффективной днлокализацией отрицательного заряда в барбитурат-ионе с участием двух атомов кислорода. Гипоксантин, ксантин и мочевая кислота образуются в организме при метаболизме нуклеиновых кислот. У гидроксипуринов возможна как лактим-лактамная таутомерия, так и таутомерия азолов, связанная с миграцией атома водорода от атома N-7 к N-2. Мочевая кислота конечный продукт метаболизма пуриновых соединений к организме. Мочевая кислота двухосновна, плохо растворима в воде, но легко растворяется в щелочах. Соли мочевой кислоты называются уратами. Ксантин по химическому поведению во многом аналогичен мочевой кислоте.
32. Алкалоиды - это азотсодержащие гетероциклические основания, обладающие сильной и специфической биологической активностью. Хорошо растворяются в воде. Содержание алкалоидов в растениях, как правило, невелико - от следов до нескольких процентов (на сухой вес растения). В цветковых растениях чаще всего представлено одновременно несколько групп алкалоидов, различающихся не только по химической структуре, но и по биологическим эффектам. Алкалоиды: метилированные ксантины (кофеин, теофиллин, теобромин содержатся в зернах кофе и чае, шелухе какао-бобов, в орехах кола. Кофеин, теобромин и теофиллин широко применяются в медицине. Кофеин используется преимущественно как психостимулятор, теобромин и теофиллин — как сердечно-сосудистые средства.
В отличие от других алкалоидов у метилированных ксантинов основные свойства выражены очень слабо, их соли с минеральными кислотами гидролизованы. За счет пиррольного атома азота теофиллин и теобромин обладают кислотными свойствами, они способны образовывать нерастворимые соли с ионами некоторых металлов, что используется для их идентификации и количественного определения в фармацевтическом анализе.
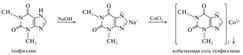
Так, водонерастворимый теофиллин, предварительно превращенный в растворимую натриевую соль, осаждается ионами кобальта(II) в виде соли светло-розового цвета.
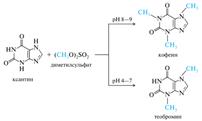
Теобромин при такой же обработке дает соль серовато-голубого цвета; анион этой соли представлен ниже в виде резонансных структур, соответствующих лактамной и лактимной формам теобромина. Кофеин, не обладающий кислотными центрами, подобной соли не образует. На использовании кислотных свойств пуриновых алкалоидов основано получение водорастворимых препаратов. Примером может служить эуфиллин — соль теофиллина с этилендиамином. Следует отметить, что все три метилированных ксантина устойчивы к щелочам только при обычной температуре, а при нагревании подвергаются частичному (теобромин) или полному разрушению с раскрытием пиримидинового кольца. Пуриновые алкалоиды извлекают из отходов переработки чая (содержание кофеина до 5%) или из низкосортного кофе (содержание кофеина до 1,5%). Однако большую часть пуриновых алкалоидов получают синтетически из доступной и дешевой мочевой кислоты (см. 29.3.2). Алкилирование ксантина диметилсульфатом при pH 8—9 приводит преимущественно к образованию кофеина, при рН 4—7 — теобромина.
Атомы азота в молекуле ксантина подвергаются алкилированию в последовательности N-3,N-7,N-1, поэтому теофиллин прямым алкилированием ксантина синтезировать не удается, его получают другими методами.
Алкалоиды: никотин, анабазин В эту группу входят алкалоиды относительно простого строения, довольно давно выделенные в чистом виде.
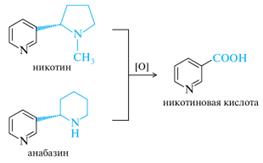
Никотин основной алкалоид табака и махорки, представляет собой жидкость с характерным табачным запахом. Из двух атомов азота в молекуле никотина большей основностью обладает атом азота насыщенного пирролидинового кольца, что объясняется их разной гибридизацией.
Анабазин— алкалоид ежовника безлистного, из которого его выделяют в промышленности. В небольшом количестве содержится в табаке. Анабазин представляет собой бесцветную жидкость. Анабазин по фармакологическому действию похож на никотин. Используется как средство, облегчающее отвыкание от курения табака, применялся еще как инсектицид, но в настоящее время снят с производства из-за высокой токсичности. При окислении никотина и анабазина образуется никотиновая кислота: Хинин— алкалоид, выделенный из коры хинного дерева (Cinchona oficinalis) — представляет собой бесцветные кристаллы очень горького вкуса.
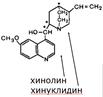
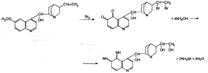
Содержащиеся в его молекуле два атома азота различаются по основности, поэтому хинин образует два ряда солей: первым протонируется более основный атом азота хинуклидиновой системы. Сульфат хинина в водном растворе дает синюю флуоресценцию. Флуоресценция настолько интенсивна, что заметна даже в очень разбавленных растворах хинина, например в прохладительных напитках, в которые небольшие количества хинина добавляются для горечи. Хинин используется в медицине в качестве противомалярийного средства, однако к настоящему времени из-за многих негативных побочных эффектов применение его ограничено. Общей реакцией на хинин является так называемая талейохинная проба. Она заключается в окислении хинина бромной водой до образования бесцветного раствора орто-хинона. Последующее действие раствором аммиака приводит к образованию дииминопроизводных орто-хиноидной структуры, окрашенных в изумрудно-зеленый цвет.
Морфин— важнейший из опиумных алкалоидов. Морфин, кодеин и тебаин относятся к морфинановым алкалоидам. Морфин обладает сильным анальгезирующим действием, благодаря чему долгое время использовался в медицине в качестве обезболивающего средства. Морфин, его производные и синтетические аналоги, относящиеся к классу наркотических анальгетиков, называются опиатами. Крайне негативным побочным действием морфина является возникновение в результате даже непродолжительного применения болезненного привыкания (наркозависимости). Некоторые синтетические производные морфина обладают более сильным наркотическим действием, чем сам морфин. Диацетат морфина — героин — наиболее распространенный наркотик. Вещество Бентли (синтетический аналог морфина) примерно в 10 000 раз активнее морфина.
ЛАКТИМ-ЛАКТАМНАЯ ТАУТОМЕРИЯ Взаимопревращение таутомерных форм связано с переносом протона от гидроксильной группы, напоминающей фенольную ОН-группу, к основному центру — пиридиновому атому азота и наоборот. Обычно лактамная форма в равновесии преобладает.
Нуклеи́новая кислота (от ла. nucleus — ядро) — высокомолекулярное органическое соединение, биополимер (полинуклеотид), образованный остатками нуклеотидов. Нуклеиновые кислоты ДНК и РНК присутствуют в клетках всех живых организмов и выполняют важнейшие функции по хранени, передаче и реализации наследственной информации. Цепи НК содержат большое количество фосфатных остатков, обладающих высокой кислотностью и ионизированных в водной среде. Поэтому молекулы НК несут на себе большой отрицательный заряд, и выделяемые препараты НК представляют собой их натриевые соли. омплементарное соединение оснований - комплементарность последовательностей оснований в противоположных цепях ДНК: основания нуклеиновых кислот всегда взаимодействуют одинаково: - в ДНК адениновое основание всегда взаимодействует с тимином, а цитозиновое основание всегда взаимодействует с гуанином; - в молекуле РНК пару с аденином образует урацил, основание заменяющее тимин. Между пуриновыми и пиримидиновыми основаниями, находящимися лактамной форме (за исключением аденина, у которого нет лактим-лактамной таутомерии) возникают водородные связи. Водородные связи возможны как между водородом и кислородом, так и между водородом и пиридиновым азотом.
|
|||||||||
|
Последнее изменение этой страницы: 2016-08-01; просмотров: 1325; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.218.55.14 (0.043 с.) |

 Перечисленные производные (кроме салола) оказывают анальгетическое, жаропонижающее и противовоспалительное действие. Метилсалицилат из-за раздражающего действия используется наружно в составе мазей. Салол применяется как дезинфицирующее средство при кишечных заболеваниях и примечателен тем, что в кислой среде желудка не гидролизуется, а распадается только в кишечнике. В связи с этим салол используют также в качестве материала для защитных оболочек некоторых лекарственных средств, нестабильных в кислой среде желудка. Салициловая кислота впервые была получена путем окисления салицилового альдегида, содержащегося в растении таволге (род Spireae). Отсюда и ее первоначальное название - спировая кислота, с которым связано название аспирин (начальная буква «а» обозначает ацетил). Ацетилсалициловая кислота в природе не найдена.
Перечисленные производные (кроме салола) оказывают анальгетическое, жаропонижающее и противовоспалительное действие. Метилсалицилат из-за раздражающего действия используется наружно в составе мазей. Салол применяется как дезинфицирующее средство при кишечных заболеваниях и примечателен тем, что в кислой среде желудка не гидролизуется, а распадается только в кишечнике. В связи с этим салол используют также в качестве материала для защитных оболочек некоторых лекарственных средств, нестабильных в кислой среде желудка. Салициловая кислота впервые была получена путем окисления салицилового альдегида, содержащегося в растении таволге (род Spireae). Отсюда и ее первоначальное название - спировая кислота, с которым связано название аспирин (начальная буква «а» обозначает ацетил). Ацетилсалициловая кислота в природе не найдена.