
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Робота з газами в курсі хіміїСтр 1 из 5Следующая ⇒
Заняття 9, 10, 11 ДЕМОНСТРАЦІЙНИЙ ЕКСПЕРИМЕНТ НА УРОКАХ ХІМІЇ Робота з газами в курсі хімії
Питання для підготовки. 1. Прилади для добування та зберігання газів. 2. Будова, принцип дії та підготовка до роботи апарата Кіппа та газометра; правила роботи з ними. Методика їх використання. 3. Застережні заходи при роботі з приладами для добування газів. 4. Саморобні прилади для добування газів. Перевірка приладів на герметичність. 5. Способи збирання та переливання газів. 6. Висушування газів. 7. Газоподібні речовини, що вивчаються в курсі неорганічної хімії: кисень, водень, гідрогенхлорид, амоніак, карбон діоксид: добування, збирання, вивчення властивостей. 8. Робота з газами в курсі органічної хімії. Добування та дослідження властивостей метану, етилену та ацетилену. 9. Знешкодження залишків газів після проведення дослідів з ними. Утилізація газів. 10. Аналіз шкільних програм. Місце запропонованих дослідів у шкільному курсі хімії (клас, тема, на які базові знання спираються, які нові поняття та вміння формуються).
Завдання: повторити теоретичні знання з фізичних та хімічних властивостей газоподібних речовин, способів їх добування, збирання та зберігання; проробити демонстраційні досліди з даного розділу, з’ясувати техніку та методику їх проведення, провести вправи з демонстрування.
ХІД ЗАНЯТТЯ
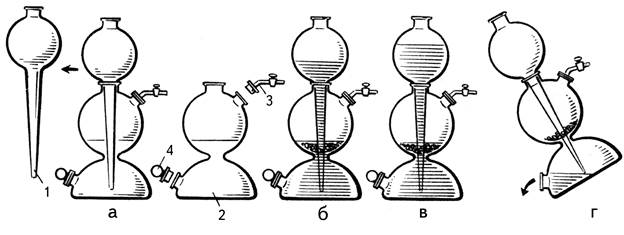
Апарат для добування газів АКТ-500 (апарат Кіппа) В шкільних умовах апарат використовують для добування водню дією розбавленої хлоридної кислоти на метали (цинк), а також для добування вуглекислого газу дією розбавленої хлоридної кислоти на мармур. Апарат складається з основної посудини з сферичною частиною (2) – реактором та напівсферичною опорною частиною. Верхній отвір реактора слугує для установки лійки (1) (масивної, сферичної форми, з довгим – майже до дна основи – стеблом, що тоншає донизу), а боковий – газового крану (3). У більшості апаратів опорна частина містить тубус (4) для зливу рідини при розбиранні. Між реактором та опорною частиною розміщують диск (вініпластовий або гумовий) для розташування твердих реагентів.
Підготовка до роботи. 1. Вміщують в реактор (2) диск для твердих реагентів, закривають зливний тубус пробкою (4). 2. На шліф лійки (1) наносять ущільнюючу змазку, з’єднують її з реактором. 3. Через отвір в реакторі для газового крану за допомогою лійки для порошків засипають гранули твердого реагенту (якщо він просипається у нижню частину – замінити диск). 4. Встановлюють газовий кран (3), відкривають його. 5. За допомогою конічної лійки, тимчасово встановленої у верхній отвір сферичної лійки (1), заливають розчин кислоти (приблизно 800 мл хлоридної кислоти 1:1 чи 1:2 або сульфатної – 1:5). Її ллють до тих пір, доки рівень рідини в реакторі підніметься вище твердої речовини на 1-1,5 см (б). 6. Закривають кран. Рідина із реактора газом витісняється у лійку (в).
Після проведення дослідів апарат розбирають та підготовлюють до зберігання. Переносячи прилад не можна тримати його за лійку. Порядок розбирання АКТ-500. 1. Підготовлюють стакан для злива кислоти. Апарат ставлять на підвищення, стакан розташовують трохи нижче. 2. Нахиляють прилад, відкривають зливну пробку. Зливають кислоту (г). Для прискорення процесу відкривають газовий кран на реакторі; після зливу кислоти його знімають. 3. Закривають пробку зливного отвору, заливають у прилад воду для відмивання його від кислоти. Зливають воду в каналізацію, операцію повторюють ще раз. 4. Якщо апаратом тривалий час не будуть користуватись, то розбирання проводять повне: знімають сферичну лійку, висипають твердий реагент, видаляють ущільнюючий засіб (стрічку чи змазку), промивають частини апарата з миючим засобом, висушують у сушильній шафі та складають для зберігання, заложивши у місця з’єднань смужки паперу.
Газометр Г-5 Газометр застосовують для збирання, зберігання та використання газів, малорозчинних у воді, та які не утворюють з повітрям вибухових сумішей (кисню, азоту, нітроген(II) оксиду тощо). Газометр (б) складається із циліндричної посудини (в) з верхнім отвором для сполучення з лійкою та двома тубусами (верхнім – для установки газового крану та нижнім – для установки пробки, через яку заповнюють прилад газами та зливають воду). Лійка (а) являє собою фігурний масивний пристрій з краном та звуженою донизу стеблиною. Пробка для нижнього тубусу містить два отвори, в які вставлені трубки: коротка більшого діаметру – для випуску води при заповненні приладу газом, довгу меншого діаметра – для подачі газу. Зовнішні кінці трубок приблизно однакові, трохи загнуті. Частина трубки для подачі газу, повернута всередину газометра, повинна бути трохи довшою тубуса.
Густина водню
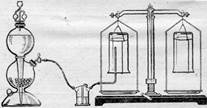
Апарат Кіппа з’єднайте з промивною склянкою, до якої приєднайте зігнуту під прямим кутом скляну трубку. До терезів підвісьте 2 стакани. Для цього скористайтеся дротом. Терези врівноважте. Під один із стаканів обережно підведіть скляну трубку і пустіть слабкий потік водню із апарата Кіппа. Водень поступово витісняє повітря зі стакану, а чашка терезів з ним піднімається. Коли протилежна чашка опуститься до можливої межі припиніть подачу водню. Підпаліть водень в стакані – відбувається невеликий вибух. Стінки стакану запотівають. 2Н2 + О2 = 2Н2О
Переливання водню Реактиви та обладнання: 2 скляні циліндри для збирання газу, апарат Кіппа з цинком і розчином сульфатної кислоти.
Фізичні властивості кисню Реактиви та обладнання: 2 скляні циліндри (банки) для збирання газу, газометр, технохімічні терези, 2 колби на 500 мл, зігнута скляна трубка, пісок, тліюча скалка. Агрегатний стан, відсутність кольору і запаху можна спостерігати, зібравши кисень в банку або газометр. Доказ того, що кисень важче за повітря На терезах врівноважують порожню колбу (з повітрям), яку наповнюють з газометра киснем (краще просушеним). При цьому рівновага порушується, колба з киснем переважує. Переливання кисню Киснем заповнюють банку в 500 мл. Зібраний кисень поволі переливають в іншу банку місткістю менше першої (250-300 мл). Банку, з якої переливали кисень, залишають стояти вверх дном. Випробуванням тліючою скалкою визначають присутність кисню тільки в меншій банці.
Склад повітря Реактиви та обладнання: скляний дзвін місткістю 3-5 л з верхнім тубусом і добре підігнаною пробкою (або бутель з відрізаним дном), кристалізатор, порцелянова чашка діаметром 5-6 см, скляна паличка (по висоті дзвону), штатив з лапкою, пальник, скалка, червоний фосфор.
В кристалізатор наполовину його об'єму налийте воду (3), на її поверхню помістіть порцелянову чашку (2), в яку покладіть 1-1,5 г сухого червоного фосфору. Фосфор повинен бути взятий в кількості, дещо більшій проти необхідного для зв’язування всього кисню повітря, розміщеного під дзвоном. Вийнявши пробку з тубуса, помістіть дзвін в кристалізатор, укріпіть його в лапці штативу. Занурте дзвін у воду (або підливайте її) настільки, щоб рівень води в кристалізаторі співпадав з нижнім розподілом дзвону, але нижній край останнього не доходив до дна кристалізатора (рівень А) Сильно нагрійте кінець довгої скляної палички в полум'ї пальника, введіть її в дзвін через відкритий тубус і, торкаючись до фосфору, підпаліть його. Негайно видаливши паличку, тубус щільно закрийте пробкою. Дзвін наповнюється густим білим димом оксиду фосфору (V). При горінні фосфору об'єм повітря усередині дзвону спочатку від нагрівання дещо збільшується, а рівень води знижується. У міру витрачання кисню полум'я поступово затухає, горіння припиняється, хоча фосфор і не прореагував повністю. Білий дим поступово розчиняється у воді. Охолоджуючись, газ під дзвоном зменшується в об'ємі, а рівень води підвищується. В кристалізатор доливають води стільки, щоб і всередині і зовні дзвону рівні були однаковими і співпадали з другим розподілом дзвону (рівень Б ). Цеозначає, що 1/5 повітря (кисень) витратилась при горінні фосфору, а 4/5, що залишилися, є азотом, в якому палаюча скалка гасне.
Розчинення аміаку у воді Реактиви та обладнання: прилад для добування аміаку, циліндр місткістю 0,5 л з скляною пластинкою, кристалізатор, 2 великі скляні бутлі або великі колби з пробками і трубками, промывна склянка з водою, штатив з двома кільцями, розчин фенолфталеїну. Розчинення аміаку в промивній склянці, наповненою водою з декількома краплями фенолфталеїну. До приладу, в якому одержують аміак, приєднайте промивную склянку. Не дивлячись на те що аміак безперервно поступає в трубку, пробулькування газу через рідину не спостерігається, оскільки він весь розчиняється у воді. При цьому рідина, в яку доданий фенолфталеїн, забарвлюється в червоний колір.
Метан Реактиви та обладнання: металічний штатив з лапкою, пробка з газовідвідною трубкою, 2 сухі великі пробірки, скляна паличка, натрій ацетат безводний, натронне вапно, шпатель, 4 пробірки для розчинів, розчин вапняної води, сірники, пальник. Добування метану.
Пробірку закрити пробкою з газовідвідною трубкою. Закріпити пробірку у лапці штативу нахилити у бік пробки. Суміш нагріти. (Спочатку всю пробірку прогрівають, а потім нагрівають саме реакційну суміш у слабкому полум'ї). У другу пробірку зібрати газ, що виділяється. Відношення метану до окисників, кислот, лугів У 4 пробірки налити розчини КМnО4, бромної води, кислоти, лугу. Газовідвідну трубку, через яку виділяється метан почергово опускати в пробірки з розчинами. Роблять висновок про відношеня метану до окисників. Якісний склад метану Пробірку, заповнену метаном, перевертають догори дном,відхиляють, підпалюють газ. Метан згоряє. На стінках пробірки утворюються крапельки води. Пробірку перевертають догори отвором та вміщують 0,5-1 мл вапняної води, енергійно збовтують, роблять висновки. Етилен Реактиви та обладнання: металічний штатив з лапкою, пробка з газовідвідною трубкою, суха велика пробірка, скляна паличка, етиловий спирт 96 %-ний, концентрована сульфатна кислота, 2 пробірки для розчинів, кип’ятильні камінці, сірники, пальник. Добування етилену. Скласти прилад для добування газу. В суху пробірку налити 2-3 мл суміші: одна частина 96 %-ного етилового спирту та три частини H2SO4 (конц.), покласти трохи піску або кип’ятильних камінців. Пробірку закрити газовідвідною трубкою та закріпити у лапці штативу так, щоб її дно було нижче від отвору. Суміш нагрівають. Спочатку всю пробірку прогрівають, а потім нагрівають саме реакційну суміш у слабкому полум'ї. Доведення ненасиченості етилену. У пробірку налити бромної води 1-2 мл, в іншу пробірку налити розчин КМnО4 1-2 мл, який підкислити розчином H2SO4. B кожну пробірку пропустити етилен. Спостерігати, які зміни відбуваються з розчинами. Горіння етилену. Газовідвідну трубку перевернути догори отвором. Газ, що виділяється підпалити. Етилен горить світним полум’ям.
Ацетилен Реактиви та обладнання: металічний штатив з лапкою, пробка з газовідвідною трубкою, суха велика пробірка, скляна паличка, кальцію карбід, шпатель, розбавлена сульфатна кислота, 2 пробірки для розчинів, сірники. Добування ацетилену та доведення його ненасиченості.
Горіння ацетилену. Газовідвідну трубку повертають догори отвором. Ацетилен запалюють. Він горить кіптявим полум'ям.
7. Провести демонстрування дослідів та надати відповідний коментар до них. 8. Відкоригувати картки дослідів, зазначити тривалість демонстрування.
Заняття 9, 10, 11 ДЕМОНСТРАЦІЙНИЙ ЕКСПЕРИМЕНТ НА УРОКАХ ХІМІЇ Робота з газами в курсі хімії
Питання для підготовки. 1. Прилади для добування та зберігання газів. 2. Будова, принцип дії та підготовка до роботи апарата Кіппа та газометра; правила роботи з ними. Методика їх використання. 3. Застережні заходи при роботі з приладами для добування газів. 4. Саморобні прилади для добування газів. Перевірка приладів на герметичність. 5. Способи збирання та переливання газів. 6. Висушування газів. 7. Газоподібні речовини, що вивчаються в курсі неорганічної хімії: кисень, водень, гідрогенхлорид, амоніак, карбон діоксид: добування, збирання, вивчення властивостей. 8. Робота з газами в курсі органічної хімії. Добування та дослідження властивостей метану, етилену та ацетилену. 9. Знешкодження залишків газів після проведення дослідів з ними. Утилізація газів. 10. Аналіз шкільних програм. Місце запропонованих дослідів у шкільному курсі хімії (клас, тема, на які базові знання спираються, які нові поняття та вміння формуються).
Завдання: повторити теоретичні знання з фізичних та хімічних властивостей газоподібних речовин, способів їх добування, збирання та зберігання; проробити демонстраційні досліди з даного розділу, з’ясувати техніку та методику їх проведення, провести вправи з демонстрування.
ХІД ЗАНЯТТЯ
Апарат для добування газів АКТ-500 (апарат Кіппа) В шкільних умовах апарат використовують для добування водню дією розбавленої хлоридної кислоти на метали (цинк), а також для добування вуглекислого газу дією розбавленої хлоридної кислоти на мармур. Апарат складається з основної посудини з сферичною частиною (2) – реактором та напівсферичною опорною частиною. Верхній отвір реактора слугує для установки лійки (1) (масивної, сферичної форми, з довгим – майже до дна основи – стеблом, що тоншає донизу), а боковий – газового крану (3). У більшості апаратів опорна частина містить тубус (4) для зливу рідини при розбиранні. Між реактором та опорною частиною розміщують диск (вініпластовий або гумовий) для розташування твердих реагентів.
Підготовка до роботи. 1. Вміщують в реактор (2) диск для твердих реагентів, закривають зливний тубус пробкою (4). 2. На шліф лійки (1) наносять ущільнюючу змазку, з’єднують її з реактором. 3. Через отвір в реакторі для газового крану за допомогою лійки для порошків засипають гранули твердого реагенту (якщо він просипається у нижню частину – замінити диск). 4. Встановлюють газовий кран (3), відкривають його. 5. За допомогою конічної лійки, тимчасово встановленої у верхній отвір сферичної лійки (1), заливають розчин кислоти (приблизно 800 мл хлоридної кислоти 1:1 чи 1:2 або сульфатної – 1:5). Її ллють до тих пір, доки рівень рідини в реакторі підніметься вище твердої речовини на 1-1,5 см (б). 6. Закривають кран. Рідина із реактора газом витісняється у лійку (в).
Після проведення дослідів апарат розбирають та підготовлюють до зберігання. Переносячи прилад не можна тримати його за лійку. Порядок розбирання АКТ-500. 1. Підготовлюють стакан для злива кислоти. Апарат ставлять на підвищення, стакан розташовують трохи нижче. 2. Нахиляють прилад, відкривають зливну пробку. Зливають кислоту (г). Для прискорення процесу відкривають газовий кран на реакторі; після зливу кислоти його знімають. 3. Закривають пробку зливного отвору, заливають у прилад воду для відмивання його від кислоти. Зливають воду в каналізацію, операцію повторюють ще раз. 4. Якщо апаратом тривалий час не будуть користуватись, то розбирання проводять повне: знімають сферичну лійку, висипають твердий реагент, видаляють ущільнюючий засіб (стрічку чи змазку), промивають частини апарата з миючим засобом, висушують у сушильній шафі та складають для зберігання, заложивши у місця з’єднань смужки паперу.
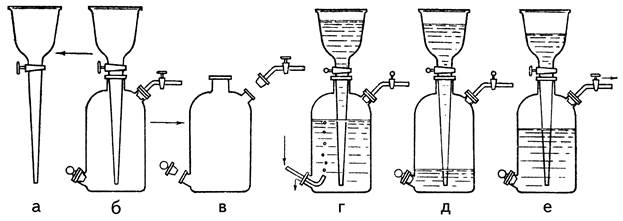
Газометр Г-5 Газометр застосовують для збирання, зберігання та використання газів, малорозчинних у воді, та які не утворюють з повітрям вибухових сумішей (кисню, азоту, нітроген(II) оксиду тощо). Газометр (б) складається із циліндричної посудини (в) з верхнім отвором для сполучення з лійкою та двома тубусами (верхнім – для установки газового крану та нижнім – для установки пробки, через яку заповнюють прилад газами та зливають воду). Лійка (а) являє собою фігурний масивний пристрій з краном та звуженою донизу стеблиною. Пробка для нижнього тубусу містить два отвори, в які вставлені трубки: коротка більшого діаметру – для випуску води при заповненні приладу газом, довгу меншого діаметра – для подачі газу. Зовнішні кінці трубок приблизно однакові, трохи загнуті. Частина трубки для подачі газу, повернута всередину газометра, повинна бути трохи довшою тубуса.
|
|||||||||
|
Последнее изменение этой страницы: 2016-07-11; просмотров: 567; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.150.109 (0.049 с.) |
 Реактиви та обладнання: апарат Кіппа, цинк, розчин кислоти, промивна склянка, технохімічні терези, 2 стакани на 500 мл, зігнута скляна трубка, пісок, м’який дріт.
Реактиви та обладнання: апарат Кіппа, цинк, розчин кислоти, промивна склянка, технохімічні терези, 2 стакани на 500 мл, зігнута скляна трубка, пісок, м’який дріт.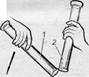 Переверніть циліндр догори дном і введіть в нього трубку від апарату Кіппа. Наповніть циліндр воднем. Не міняючи його положення, наблизьте до нього циліндр з повітрям (2), також перевернений догори дном. Циліндр з воднем (1) поволі повертайте до тих пір, поки він не виявиться отвором вгору якраз під циліндром з повітрям. Якщо тепер нижній циліндр піднести до полум'я пальника, то виявиться, що в ньому водню немає. При тому, що при піднесенні же до полум'я верхнього циліндра відбувається спалах, який супроводжується невеликим (небезпечним) вибухом.
Переверніть циліндр догори дном і введіть в нього трубку від апарату Кіппа. Наповніть циліндр воднем. Не міняючи його положення, наблизьте до нього циліндр з повітрям (2), також перевернений догори дном. Циліндр з воднем (1) поволі повертайте до тих пір, поки він не виявиться отвором вгору якраз під циліндром з повітрям. Якщо тепер нижній циліндр піднести до полум'я пальника, то виявиться, що в ньому водню немає. При тому, що при піднесенні же до полум'я верхнього циліндра відбувається спалах, який супроводжується невеликим (небезпечним) вибухом. Скляний дзвін розділіть на 6 рівних за об'ємом частин. Для цього закрийте тубус пробкою і переверніть дзвін тубусом вниз, наповніть його до країв водою. Змірявши таким чином загальний об'єм, знову налийте в дзвін воду вже частинами — по 1/6 загального об'єму, відзначаючи кожного разу відповідний рівень води. Потім на суху зовнішню поверхню дзвону нанесіть міцні і добре помітні розподіли (ізоляційною стрічкою, масляною фарбою тощо). Як мітки можуть бути використані смужки яскраво забарвленого паперу, які потім покривають шаром розплавленого парафіну або прозорою клейкою стрічкою (1).
Скляний дзвін розділіть на 6 рівних за об'ємом частин. Для цього закрийте тубус пробкою і переверніть дзвін тубусом вниз, наповніть його до країв водою. Змірявши таким чином загальний об'єм, знову налийте в дзвін воду вже частинами — по 1/6 загального об'єму, відзначаючи кожного разу відповідний рівень води. Потім на суху зовнішню поверхню дзвону нанесіть міцні і добре помітні розподіли (ізоляційною стрічкою, масляною фарбою тощо). Як мітки можуть бути використані смужки яскраво забарвленого паперу, які потім покривають шаром розплавленого парафіну або прозорою клейкою стрічкою (1). Скласти прилад для добування газу та перевірити його на герметичність. На аркуш паперу насипати одну частину CH3COONa (прожареного), та дві частини натронного вапна, перемішати скляною паличкою і насипати суміш в суху пробірку на чверть її вмісту.
Скласти прилад для добування газу та перевірити його на герметичність. На аркуш паперу насипати одну частину CH3COONa (прожареного), та дві частини натронного вапна, перемішати скляною паличкою і насипати суміш в суху пробірку на чверть її вмісту. У пробірку вміщують 3-4 шматочки СаС2 (карбіду кальцію) і закріплюють її в лапці штативу вертикально. Наливають воду або розчин H2SO4 (1:3) 2-3 мл. Пробірку закривають пробкою з газовідвідною трубкою, кінець якої опускають в пробірку з бромною водою або з розчином КMnО4, який підкислюють сірчананою кислотою.
У пробірку вміщують 3-4 шматочки СаС2 (карбіду кальцію) і закріплюють її в лапці штативу вертикально. Наливають воду або розчин H2SO4 (1:3) 2-3 мл. Пробірку закривають пробкою з газовідвідною трубкою, кінець якої опускають в пробірку з бромною водою або з розчином КMnО4, який підкислюють сірчананою кислотою.


