
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Дослід 12. Добування нітриту калію
а) Розплавте у пробірці 0,5-1 г нітрату калію. Нагрівання треба продовжувати до припинення реакції. Як встановити кінець реакції? Напишіть рівняння реакції. Охолоджений розплав розчиніть у воді та доведіть наявність у розчині солі азотистої кислоти. б) Витісніть цинком 5 г свинцю з розчину ацетату свинцю. Промийте добутий дрібнодисперсний свинець на фільтрі та висушіть його у сушильній шафі. Розплавте 2,5 г нітрату калію у фарфоровому тиглі до початку розкладу та внесіть невеликими порціями свинець при старанному перемішуванні вмісту залізним дротом. (Захисні окуляри! Роботу необхідно проводити у витяжній шафі). Продовжуйте нагрівання 15-20 хвилин та вилийте розплав на залізний лист. Охолоджену та роздріблену масу розчиніть у 20 мл киплячої води. Профільтруйте розчин. Що залишиться на фільтрі і що перейде у фільтрат? Нейтралізуйте фільтрат розбавленою азотною кислотою та випарюйте до появлення плівки на поверхні розчину. Охолодіть розчин та відфільтруйте кристали, що випали. Маточний розчин висушіть досуха у попередньо висушеній фарфоровій чашці. (Уникати розбризкування!). Доведіть вагу чашки з кристалами до сталої маси у сушильній шафі. Розрахуйте масову частку виходу. Напишіть рівняння усіх реакцій, що відбуваються. Доведіть, що добуті кристали є кристалами нітриту калію. Лабораторна робота. Азотна кислота та її солі Дослід 13. Добування азотної кислоти
· Чому для добування азотної кислоти не можна використовувати селітри та розбавлену сірчану кислоту? Дослід 14. Розклад азотної кислоти при нагріванні Обережно нагрійте закріплену вертикально у штативі пробірку з 1-2 мл концентрованої азотної кислоти. Киньте до пробірки тліючу жаринку. Що спостерігається? Напишіть рівняння реакцій.
Дослід 15. Окисні властивості азотної кислоти а) Дія на органічні сполуки. Налийте до фарфорової чашки 1-2 мл добутої азотної кислоти та обережно прилийте піпеткою 2-3 краплини скипидару С10Н16. Що спостерігається? Капніть на шматочок вовни 1-2 краплини концентрованої азотної кислоти. Що відбувається з вовною? б) Дія на неметали. До двох пробірок налийте по 1-2 мл добутої азотної кислоти. До першої пробірки помістіть шматочок сірки та прокип’ятіть кілька хвилин. Напишіть рівняння реакції. Доведіть присутність іонів · Який газ утворюється при відновленні концентрованої азотної кислоти неметалами? в) Взаємодія азотної кислоти із сірководнем. До 5 мл прозорої сірководневої води прилийте 1-2 мл розбавленої азотної кислоти. Що спостерігається? Напишіть рівняння реакції. г) Окиснення соляної кислоти. До 2 мл концентрованої соляної кислоти додайте кілька крапель концентрованої азотної кислоти. Що спостерігається? Як змінюється колір зволоженого йодкрохмального папірця, піднесеного до отвору пробірки? Напишіть рівняння реакції. д) Взаємодія азотної кислоти з металами. Дослідіть дію концентрованої та розбавленої азотної кислоти на цинк та мідь. Занурте шматочок алюмінію у розчин соляної кислоти (2 моль/л). Що спостерігається? Витягніть алюміній з соляної кислоти, промийте водою та висушіть фільтрувальним папером, потім занурте алюміній на 1-2 хвилини у димлячу азотну кислоту. Обережно витягніть алюміній, промийте водою та знову занурте у соляну кислоту. Які явища спостерігаються? Дайте пояснення. Напишіть рівняння реакцій. · Чи впливає розбавлення азотної кислоти на ступінь відновлення її цинком? Дослід 16. Нітрати а) Термічний розклад нітратів. Помістіть до сухих пробірок трохи сухих солей - нітратів калію, свинцю, ртуті. Прожарте у полум’ї пальника наведені солі. Напишіть рівняння реакцій. б) Горіння вугілля та сірки у селітрі. В штативі закріпіть вертикально пробірку з 2 г калійної селітри. Під пробірку поставте піщану баню. Нагрійте селітру до розплавлення та киньте до неї розжареного вугілля. Що спостерігається? Приберіть пальник та киньте шматочок сірки. Коли сірка розплавиться, охолодіть пробірку, розчиніть її вміст у воді та доведіть присутність у розчині нітрит-іонів.
Дослід 17. Нітрозилхлорид
Рис.18. Прилад для добування нітрозилхлориду
Зберіть прилад (рис.18). До U-подібної трубки насипте шар свіжовиготовленого активованого вугілля. U-подібну трубку помістіть до термостату з температурою 50 0С. Приймач помістіть в охолоджувальну суміш. Витісніть повітря з пробірки струмом сухого оксиду азоту(ІІ). Не припиняючи пропускання оксиду азоту(ІІ), пропустіть сухий хлор. Напишіть рівняння реакцій. · Яка температура кипіння нітрозилхлориду? · Як довести присутність у розчині іонів Cl- та NO2-?
|
||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 372; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.17.128.129 (0.005 с.) |
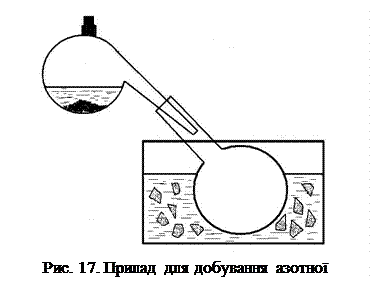 Зберіть прилад (рис. 17). До реторти крізь тубус насипте 10 г нітрату натрію, прилийте близько 10 мл сірчаної кислоти з мас. часткою 98%. Приймач помістіть у воду з льодом. Обережно нагрійте реторту. Чому нагрівання необхідне та разом з тим має проводитись обережно? В результаті якої реакції у реторті з’являється бура пара? Нагрівання треба припинити, коли в приймачі збереться близько 5 мл азотної кислоти. Добуту кислоту збережіть до наступних дослідів.
Зберіть прилад (рис. 17). До реторти крізь тубус насипте 10 г нітрату натрію, прилийте близько 10 мл сірчаної кислоти з мас. часткою 98%. Приймач помістіть у воду з льодом. Обережно нагрійте реторту. Чому нагрівання необхідне та разом з тим має проводитись обережно? В результаті якої реакції у реторті з’являється бура пара? Нагрівання треба припинити, коли в приймачі збереться близько 5 мл азотної кислоти. Добуту кислоту збережіть до наступних дослідів.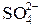 у розчині. До другої пробірки помістіть шматочок деревного вугілля та прокип’ятіть. Напишіть рівняння реакцій.
у розчині. До другої пробірки помістіть шматочок деревного вугілля та прокип’ятіть. Напишіть рівняння реакцій.



