
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Состав и характеристики атомных ядер
Ядро любого атома, кроме атома легкого водорода, состоит из частиц – нуклонов двух типов: Z протонов и N нейтронов. Нейтрон был открыт в 1932 г. Джеймсом Чэдвиком, тогда же Карлом Андерсоном – позитрон. Ядро атома легкого водорода состоит из одного протона. Протон открыт в является заряженной частицей – qp = +e. Масса протона составляет mp = 1.67265 10–27 кг. В ядерной физике принято энергию частиц выражать в единицах энергии (эВ), для чего умножают массу на квадрат скорости света c2, тогда масса протона mp = 938.26 МэВ. Протон имеет спин, равный s = 1/2. Нейтрон также имеет спин s = 1/2. Его масса близка к массе протона и составляет mn =1.67495 10–27 кг или в единицах энергии (эВ) mp = 939.55 МэВ. Однако нейтрон не имеет электрического заряда. В свободном состоянии нейтрон является радиоактивным, он самопроизвольно распадается, превращаясь в протон. При этом выделяется антинейтрино.
В составе ядра нейтрон стабилен. Атом характеризуют зарядовым числом Z (которое равно числу протонов в ядре). Число Z определяет порядковый номер атома в таблице Менделеева. Массовое число A = N + Z показывает полное число нуклонов в ядре. Масса всех нуклонов A вносит основной вклад в массу всего атома. Ядро также называют нуклидом. Принятая схема нуклида имеет вид: Атомы, ядра которых имеют одинаковые зарядовые числа Z и различные массовые числа A, имеют одни и те же химические свойства и называются изотопами. Изотопы одного и того же химического элемента различаются друг от друга лишь по числу нейтронов в ядре. Большинство веществ с атомами одного и того же Z представляют смесь различных изотопов. Так, водород, углерод и кислород имеют по 3 изотопа: Атомы, ядра которых имеют одни и те же массовые числа A, называются изобарами. Изобары, т.е. ядра с различными Z, соответствуют ядрам атомов различных химических элементов. В опытах Резерфорда по рассеянию α -частиц на атомах вещества было установлено, что ядра имеют конечный размер. С этого момента прошло много времени, однако до сих пор наиболее предпочтительными при определении размера ядра являются опыты по рассеянию частиц на атомных ядрах. Поскольку электроны испытывают только электростатическое взаимодействие с ядрами, то распределение заряда внутри ядра изучают с помощью рассеяния электронов. О распределении ядерной материи внутри ядра судят по рассеянию нейтронов, так как в этом случае взаимодействие между частицами сводится только к специфическому ядерному. Для того, чтобы ядро «почувствовало» налетающую частицу, учитывая массы, энергия электрона должна составлять не меньше 124 МэВ, а энергия нейтрона не меньше 8 МэВ. Эксперименты с электронами и нейтронами различных (но удовлетворяющих указанным условиям) энергий показали, что объем ядра пропорционален числу нуклонов в его составе:
В ядрах со спином, большим или равным 1, действительно наблюдается отклонение от сферической формы. Такие ядра могут быть сжатыми или вытянутыми эллипсоидами вращения, при этом разница между их большой и малой осями никогда не превышает 20% и, как правило, существенно меньше. В первом приближении ядро можно считать шаром, радиус ядра таким образом: Константа R0 ≈ 1.3·10–15м. Ее приблизительное значение связано с тем, что величина радиуса ядра, полученная по распределению ядерной материи, отличается от значения радиуса, полученного по распределению заряда. Это означает, что заряд и вещество распределены внутри ядра различным способом. В рамках ядерной теории используют величину 1 ферми = 1 f = 10–15м. Тогда радиус ядра равен Спином ядра I называется полный угловой момент ядра. Для ядра с массовым числом A он равен: В этом выражении первый член справа равен суммарному спиновому моменту нуклонов, а второй – суммарному орбитальному моменту нуклонов в ядре. Значения Si и li определяются значениями соответствующих квантовых чисел: sp = sn = 1/2 и l = 0, 1, 2,... Магнитный момент ядра μя складывается из собственных магнитных моментов протонов и нейтронов и орбитальных магнитных моментов протонов (нейтрон обладает нулевым орбитальным магнитным моментом при любом l). Итак, в состав ядра входят A нуклонов. Однако не все сочетания протонов и нейтронов образуют стабильные ядра. Это связано с существованием ядерных уровней энергии. Поскольку и протоны, и нейтроны являются фермионами (их спин s = 1/2), то на каждом уровне может быть не больше двух протонов и двух нейтронов. Заполнение уровней идет по принципу минимизации системы объединившихся частиц. Например, рассмотрим два изотопа
Рис. 13.1 Стабильный изотоп углерода и нестабильный изотоп бора На последнем уровне в нуклиде В легких ядрах (A < 20), как правило, число протонов и нейтронов одинаково (или отличается не единицу в случае ядер с нечетным числом нуклонов, причем число нейтронов обязательно больше числа протонов). В тяжелых ядрах доля нейтронов становится все больше. В таких ядрах помимо принципа минимизации энергии оказывается существенным кулоновское отталкивание протонов. В ядрах с числом протонов больше 10 это отталкивание настолько велико, что для устойчивости ядра эту силу необходимо чем-либо компенсировать. Между нейтронами действуют только ядерные силы притяжения. Поэтому увеличение числа нейтронов в составе ядра приводит к уравновешиванию сил, т.е. к стабильности ядра.
|
||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 573; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.149.27.202 (0.009 с.) |
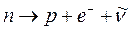 (13.1)
(13.1) Кроме нуклонов других частиц в ядре нет. Однако нуклоны не являются элементарными частицами: каждый из них состоит из трех кварков, о которых речь пойдет в другой лекции.
Кроме нуклонов других частиц в ядре нет. Однако нуклоны не являются элементарными частицами: каждый из них состоит из трех кварков, о которых речь пойдет в другой лекции. – обычный водород,
– обычный водород,  – дейтерий,
– дейтерий,  – тритий;
– тритий; 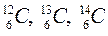 ;
;  ; у олова существует 10 изотопов.
; у олова существует 10 изотопов. (13.2)
(13.2) (13.3)
(13.3)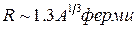 .
. (13.4)
(13.4)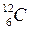 и
и 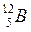 . Первые два уровня у них (рис. 13.1) заполнены одинаково.
. Первые два уровня у них (рис. 13.1) заполнены одинаково.
 не будет стабильным и довольно быстро распадется. В тоже время изотоп
не будет стабильным и довольно быстро распадется. В тоже время изотоп  (содержащий 5 протонов и 6 нейтронов) является стабильным.
(содержащий 5 протонов и 6 нейтронов) является стабильным.


