Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Тема «простые и сложные вещества. Металлы и неметаллы. Химические формулы веществ. Индексы и коэффициенты. Качественный и количественный состав вещества. Закон постоянства состава».Стр 1 из 2Следующая ⇒
Тема «Простые и сложные вещества. Металлы и неметаллы. Химические формулы веществ. Индексы и коэффициенты. Качественный и количественный состав вещества. Закон постоянства состава».
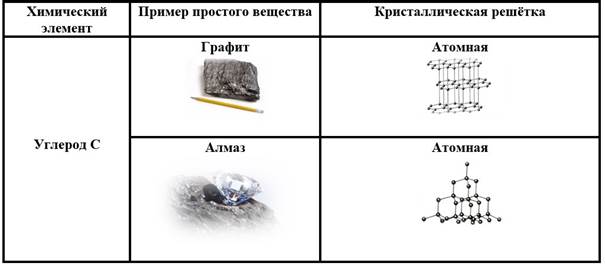
Химический элемент. Металлы и неметаллы В химии кроме терминов “атом” и “молекула” часто употребляется понятие “элемент”. Что общего и чем эти понятия различаются? Химический элемент – это атомы одного и того же вида. Так, например, все атомы водорода – это элемент водород; все атомы кислорода и ртути – соответственно элементы кислород и ртуть. В настоящее время известно более 107 видов атомов, то есть более 107 химических элементов. Нужно различать понятия “химический элемент”, “атом” и “простое вещество” Простые и сложные вещества По элементному составу различают простые вещества, состоящие из атомов одного элемента (H2, O2, Cl2, P4, Na, Cu, Au), и сложные вещества, состоящие из атомов разных элементов (H2O, NH3, OF2, H2SO4, MgCl2, K2SO4). К 70-м гг. XIX в. было уже известно более 60 химических элементов. Их условно классифицировали на металлы и неметаллы На 2019 год в периодической таблице – 118 химических элементов, которые образуют около 500 простых веществ. Способность одного элемента существовать в виде различных простых веществ, отличающихся по свойствам, называется аллотропией. Например, элемент кислород O имеет две аллотропные формы - кислород O2 и озон O3 с различным числом атомов в молекулах. Аллотропные формы элемента углерод C - алмаз и графит - отличаются строение их кристаллов. Существуют и другие причины аллотропии.
Сложные вещества часто называют химическими соединениями, например, оксид ртути(II) HgO (получается путем соединения атомов простых веществ - ртути Hg и кислорода O2), бромид натрия (получается путем соединения атомов простых веществ - натрия Na и брома Br2). Итак, подытожим вышесказанное. Молекулы вещества бывают двух видов: 1. Простые – молекулы таких веществ состоят из атомов одного вида. В химических реакциях не могут разлагаться с образованием нескольких более простых веществ. 2. Сложные – молекулы таких веществ состоят из атомов разного вида. В химических реакциях могут разлагаться с образованием более простых веществ. Различие понятий “химический элемент” и “простое вещество”
Отличить понятия “химический элемент” и “простое вещество” можно при сравнении свойств простых и сложных веществ. Например, простое вещество – кислород – бесцветный газ, необходимый для дыхания, поддерживающий горение. Мельчайшая частица простого вещества кислорода – молекула, которая состоит из двух атомов. Кислород входит также в состав оксида углерода (угарный газ) и воды. Однако, в состав воды и оксида углерода входит химически связанный кислород, который не обладает свойствами простого вещества, в частности он не может быть использован для дыхания. Рыбы, например, дышат не химически связанным кислородом, входящим в состав молекулы воды, а свободным, растворенным в ней. Поэтому, когда речь идет о составе каких – либо химических соединений, следует понимать, что в эти соединения входят не простые вещества, а атомы определенного вида, то есть соответствующие элементы. При разложении сложных веществ, атомы могут выделяться в свободном состоянии и соединяясь, образовывать простые вещества. Простые вещества состоят из атомов одного элемента. Различие понятий «химический элемент» и «простое вещество» подтверждается и тем, что один и тот же элемент может образовывать несколько простых веществ. Например, атомы элемента кислорода могут образовать двухатомные молекулы кислорода и трехатомные – озона. Кислород и озон – совершенно различные простые вещества. Этим объясняется тот факт, что простых веществ известно гораздо больше, чем химических элементов. Пользуясь понятием «химический элемент», можно дать такое определение простым и сложным веществам: Cостав соединений молекулярной структуры, т.е. состоящих из молекул, - является постоянным независимо от способа получения. Состав же соединений с немолекулярной структурой (с атомной, ионной и металлической решеткой) не является постоянным и зависит от условий получения. Задача №1 В каких массовых отношениях соединяются химические элементы в серной кислоте, химическая формула которой H2SO4? Решение: Используя ПСХЭ найдём относительные атомные массы химических элементов:
Ar(H)=1, Ar(S)=32, Ar(O)=16. Определим массовые отношения этих элементов в формуле H2SO4 m(H): m(S): m(O) = 2Ar(H): Ar(S): 4Ar(O) = 2: 32: 64 = 1: 16: 32 Таким образом, чтобы получить 49 г серной кислоты (1+16+32=49), необходимо взять 1 г - Н, 16 г - S и 32 г - О. Задача №2 Задача №3 Что обозначают записи? H2 - это одна молекула водорода (аш-два), в её состав входят два атома водорода. 5O2 - это пять молекул кислорода (пять-о-два), в состав одной молекулы входят два атома кислорода. 6Fe - это шесть атомов железа (шесть-феррум). 3H2SO4 - это три молекулы серной кислоты (три-аш-два-эс-о-четыре), в состав одной молекулы серной кислоты входят два атома водорода, один атом серы, четыре атома кислорода. Тема «Простые и сложные вещества. Металлы и неметаллы. Химические формулы веществ. Индексы и коэффициенты. Качественный и количественный состав вещества. Закон постоянства состава».
Химический элемент. Металлы и неметаллы В химии кроме терминов “атом” и “молекула” часто употребляется понятие “элемент”. Что общего и чем эти понятия различаются? Химический элемент – это атомы одного и того же вида. Так, например, все атомы водорода – это элемент водород; все атомы кислорода и ртути – соответственно элементы кислород и ртуть. В настоящее время известно более 107 видов атомов, то есть более 107 химических элементов. Нужно различать понятия “химический элемент”, “атом” и “простое вещество” Простые и сложные вещества По элементному составу различают простые вещества, состоящие из атомов одного элемента (H2, O2, Cl2, P4, Na, Cu, Au), и сложные вещества, состоящие из атомов разных элементов (H2O, NH3, OF2, H2SO4, MgCl2, K2SO4). К 70-м гг. XIX в. было уже известно более 60 химических элементов. Их условно классифицировали на металлы и неметаллы На 2019 год в периодической таблице – 118 химических элементов, которые образуют около 500 простых веществ. Способность одного элемента существовать в виде различных простых веществ, отличающихся по свойствам, называется аллотропией. Например, элемент кислород O имеет две аллотропные формы - кислород O2 и озон O3 с различным числом атомов в молекулах. Аллотропные формы элемента углерод C - алмаз и графит - отличаются строение их кристаллов. Существуют и другие причины аллотропии.
Сложные вещества часто называют химическими соединениями, например, оксид ртути(II) HgO (получается путем соединения атомов простых веществ - ртути Hg и кислорода O2), бромид натрия (получается путем соединения атомов простых веществ - натрия Na и брома Br2). Итак, подытожим вышесказанное. Молекулы вещества бывают двух видов: 1. Простые – молекулы таких веществ состоят из атомов одного вида. В химических реакциях не могут разлагаться с образованием нескольких более простых веществ. 2. Сложные – молекулы таких веществ состоят из атомов разного вида. В химических реакциях могут разлагаться с образованием более простых веществ. Различие понятий “химический элемент” и “простое вещество” Отличить понятия “химический элемент” и “простое вещество” можно при сравнении свойств простых и сложных веществ. Например, простое вещество – кислород – бесцветный газ, необходимый для дыхания, поддерживающий горение. Мельчайшая частица простого вещества кислорода – молекула, которая состоит из двух атомов. Кислород входит также в состав оксида углерода (угарный газ) и воды. Однако, в состав воды и оксида углерода входит химически связанный кислород, который не обладает свойствами простого вещества, в частности он не может быть использован для дыхания. Рыбы, например, дышат не химически связанным кислородом, входящим в состав молекулы воды, а свободным, растворенным в ней. Поэтому, когда речь идет о составе каких – либо химических соединений, следует понимать, что в эти соединения входят не простые вещества, а атомы определенного вида, то есть соответствующие элементы.
При разложении сложных веществ, атомы могут выделяться в свободном состоянии и соединяясь, образовывать простые вещества. Простые вещества состоят из атомов одного элемента. Различие понятий «химический элемент» и «простое вещество» подтверждается и тем, что один и тот же элемент может образовывать несколько простых веществ. Например, атомы элемента кислорода могут образовать двухатомные молекулы кислорода и трехатомные – озона. Кислород и озон – совершенно различные простые вещества. Этим объясняется тот факт, что простых веществ известно гораздо больше, чем химических элементов. Пользуясь понятием «химический элемент», можно дать такое определение простым и сложным веществам:
|
|||||||
|
Последнее изменение этой страницы: 2022-01-22; просмотров: 27; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.149.229.253 (0.009 с.) |