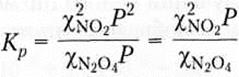Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Смещение положения химического равновесия
Равновесие, установившееся в химической системе, может быть смещено под воздействием различных внешних факторов. Общим принципом, определяющим результат внешнего воздействия и любую равновесную систему (и не только химическую), является принцип адаптивных перестроек, в химии называемый принципом Ле Шателье—Брауна. Если на систему, находящуюся в состоянии равновесия, оказывается какое-либо внешнее воздействие, то равновесие смещается таким образом, чтобы уменьшить это воздействие. Рассмотрим эти факторы: Концентрация. Изменение концентраций реагентов или продуктов реакции не влияет на величину константы равновесия. Однако если к равновесной системе добавить один из ее компонентов (т.е. увеличить его концентрацию), согласно принципу Ле Шателье—Брауна произойдет сдвиг равновесия в сторону уменьшения количества вещества добавленного компонента. Смещение равновесия можно провести несколькими способами: · при выведении из равновесной системы одного из ее компонентов смещение равновесия приводит к его образованию. Таким образом, непрерывно выводя продукты из реакционной смеси, можно постоянно удерживать систему в неравновесном (несбалансированном) состоянии. Это позволяет, вводя все новые количества реагентов, получать непрерывно соответствующие продукты. Предложенный способ проведения реакции осуществим, если один из продуктов реакции может выделяться в виде газа, конденсироваться или вымораживаться из газовой фазы в виде жидкости или твердого вещества, вымываться из газовой смеси потоком жидкости, в которой он обладает повышенной растворимостью, либо осаждаться из газа или раствора. · увеличение концентрации другого, менее ценного исходного вещества с целью более полного использования ценного исходного соединения. В качестве примера рассмотрим реакцию, приводящую к образованию карбида кальция при нагревании твердого оксида кальция и кокса (углерода) в электрической печи: СаО(тв) + 3С(тв:) → СаС2(тв) + CO(г)↑ Значение константы равновесия этой реакции при температуре ~2500°С близко к единице. Однако удаление из реакционной системы газа приводит к уменьшению концентрации продуктов реакции. Это благоприятствует протеканию прямой реакции.
При промышленном получении белого пигмента диоксида титана осуществляется реакция между газообразными тетрахлоридом титана и кислородом: ТlСl4(г) + O2(г) → TiO2(тв) + 2Сl2(г)↑ Продукт отделяют от реакционной газовой смеси в виде тонкоизмельченного порошка ТiO2. Уменьшение концентрации продуктов реакции и в этом случае сопровождается преимущественным протеканием прямой реакции. Увеличение концентраций исходных веществ и уменьшение концентраций продуктов смещает химическое равновесие вправо, а увеличение концентраций продуктов и уменьшение концентраций исходных веществ — влево. Давление. При постоянной температуре константа равновесия не изменяется при изменении давления. Однако соотношение количества вещества реагентов и продуктов при изменении давления может измениться за счет смещения равновесия в направлении, соответствующем принципу Ле Шателье — Брауна. Влияние давления на равновесные системы, в составе которых нет газов, пренебрежимо мало. Если в химическом равновесии принимают участие газы и количество вещества газообразных веществ в правой и левой части соответствующего химического уравнения различаются, при повышении давления равновесие смещается в сторону меньшего количества вещества газообразных веществ. В соответствии с этим принципом при понижении давления равновесие смещается в сторону образования большего количества вещества газообразных веществ. Следует отметить, что увеличение объема равновесной системы равноценно уменьшению давления, а уменьшение объема — увеличению давления Рассмотрим одну из реакций с участием газов: N2O4(г) D 2NO2(r) Константа равновесия этой реакции имеет следующий вид:
Парциальные давления газов (р) связаны с полным давлением системы (Р) следующими соотношениями:
где χ — молярные доли соответствующих газов. Подставив выражения для парциальных давлений в уравнение для константы равновесия, получим
При постоянной температуре правая часть уравнения тоже постоянная величина. Следовательно, если полное давление Р в системе возрастает то отношение должно уменьшится. Это означает, что доляχ(NO2) будет уменьшаться, а доляχ(N2O4) – увеличиваться, другими словами, буди протекать обратная реакция.
Температура. Зависимость положения химического равновесия от температуры определяется тепловым эффектом реакции. При повышении температуры мы привносим в систему тепло, поэтому согласно принципу Ле Шателье—Брауна происходит смещение равновесия в сторону эндотермической реакции. Если же мы понижаем температуру, равновесие смещается в сторону экзотермической реакции. Рассмотрим взаимодействие между водородом и иодом: Н2(г) + I2(г) D2НI(г) Данная реакция является эндотермической (∆Н> 0). Понижение температуры вызовет смещение равновесия в сторону обратной реакции. Наоборот, повышение температуры создаст более благоприятные условия для протекания прямой реакции (образование HI). Таким образом, можно заключить, что равновесие смещается в ту сторону, которая компенсирует эффект поступления тепла извне (повышение температуры) либо эффект его отвода (понижение температуры). Если прямая реакция в равновесной системе является экзотермической (∆Н <0), то при повышении температуры константа равновесия уменьшается. Если же прямая реакция — эндотермическая, то при повышении температуры константа равновесия увеличивается. Катализатор. Катализатор — вещество, которое увеличивает скорость химической реакции. В обратимой, протекающей в обоих направлениях, реакции катализатор в одинаковой степени увеличивает скорость и прямой, и обратной реакции. Отметим, что катализатор не оказывает влияния на концентрации продуктов и реагентов, а также на константу равновесия. Его влияние сказывается только на скорости, с которой достигается это равновесие. Константа равновесия является функцией температуры, но не зависит от концентрации реагентов или продуктов, давления, а также от наличия или отсутствия катализатора. В таблице суммировано влияние различных факторов на равновесие (принцип Ле Шателье—Брауна) для реакции а А+ b ВD с С + d D; ∆Н > 0 (а + b > с + d).
|
||||||
|
Последнее изменение этой страницы: 2022-01-22; просмотров: 33; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.217.167 (0.005 с.) |
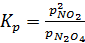 ;
;