
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Параметры орбит электронов в атоме гелия
Продолжение табл. 5.3
Рис. 5.2. Орбиты электронов в атоме гелия
Сравнивая данные таблиц 5.2 и 5.3, можно заметить, что в атоме водорода эффективное зарядовое число без учета эффекта движения имеет постоянное значение, равное единице. В атоме гелия при переходе наружного электрона с одной орбиты на другую оно для обоих электронов изменяется. Зарядовое число зависит от скорости наружного электрона и от его расстояния от ядра. Если при переходе наружного электрона на более удаленную орбиту стационарное состояние не изменяется, то его скорость уменьшается во столько же раз, во сколько увеличивается расстояние от ядра. Такой переход сопровождается уменьшением эффективного зарядового числа. Для данного стационарного состояния минимальное значение зарядового числа равно единице. Электрон при этом будет находиться на максимально возможном расстоянии от ядра. При большем расстоянии произойдет изменение стационарного состояния, сопровождающееся некоторым повышением значения эффективного зарядового числа. Увеличение зарядового числа обусловлено резким изменением скорости электрона и его расстояния от ядра. Скорость электрона уменьшается в меньшее, а расстояние от ядра увеличивается в большее число раз. В новом стационарном состоянии, по мере удаления электрона от ядра, зарядовое число будет также стремиться к единице.
Таким образом, у водорода вследствие постоянства зарядового числа в первом стационарном состоянии имеется одна круговая орбита, во втором - одна круговая и одна эллиптическая, в третьем - одна круговая и две эллиптические, в четвертом - одна круговая и три эллиптические и т.д. В гелии зарядовое число имеет переменное значение, поэтому в первом стационарном состоянии имеется одна круговая орбита, во втором - четыре круговых и одна эллиптическая, в третьем - пять круговых и две эллиптические и т.д. Периоды обращения электрона на наружных орбитах кратны периоду обращения электрона на внутренней орбите. Для каждого стационарного состояния максимальную кратность можно определить по формуле
где
Атом лития
Теория Бора-Зоммерфельда столкнулась с непреодолимыми трудностями при описании многоэлектронных атомов. Многочисленные попытки построения теории нейтрального атома гелия, одного из простейших атомов периодической системы элементов, потерпели полное крушение. Эти тягостные неудачи расцениваются как кризис теории Бора-Зоммерфельда [53]. Что касается электронного строения атома лития, то оно имеет только качественное описание [62]. Ниже приведены результаты расчетов всех параметров орбит электронов в атоме лития. В таблице 5.4 приведены параметры обит электронов в ионе лития для трех стационарных состояний. Расчет произведен следующим образом. По формуле (112) находим скорость электрона V на первой орбите у дважды ионизированного атома лития. Затем по Таблица 5.4
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 171; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.117.162 (0.005 с.) |
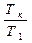

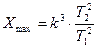 , (138)
, (138) - отношение периодов обращения электронов в невозбужденном атоме.
- отношение периодов обращения электронов в невозбужденном атоме.


