
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общая характеристика элементов
Электронная конфигурация марганца Mn, технеция Tc, рения Re характерна для переходных металлов. Каждый элемент имеет наполовину заполненную внутреннюю d -оболочку, т. е. имеет пять d -электронов на пяти d -орбиталях и 2 электрона на внешней s -орбитали:
Исходя из факта наполовину заполненной каждой d -орбитали, можно предсказать некоторые свойства элементов. Максимальная степень окисления +7. Соединения марганца (II) отличаются хорошей устойчивостью к окислению и восстановлению, а соединения Mn (III) склонны переходить в соединения Mn (II). Некоторые свойства d -элементов VII В группы приведены в табл.11.1. Таблица 11.1 Некоторые свойства d -элементов VII В группы
Металлические радиусы Tc и Re близки между собой, поэтому свойства этих элементов более сходны между собой, чем с Mn. Для марганца наиболее характерны степени окисления +2, +4, что отвечает устойчивой электронной конфигурации d 5, d 3. Для Тс и Re устойчива высшая степень окисления +7. Таким образом, в ряду Mn – Tc – Re устойчивость соединений в высшей степени возрастает. В степени окисления +7 соединения марганца значительно более сильные окислители, чем соединения технеция (VII) и рения (VII). С ростом степени окисления металла наблюдается тенденция к усилению кислотных свойств. Химическая активность в ряду Металлы подгруппы марганца имеют высокие t пл, что объясняется усилением в металлическом кристалле ковалентной связи, возникающей за счет d -электронов. Рений по температуре плавления уступает только вольфраму. Природные соединения. В свободном виде металлы не встречаются. Важнейшие минералы марганца: пиролюзит MnO2 × x H2O; браунит – Mn2O3; гаусманит Mn3O4; марганцевый шпат – MnCO3. Tc в природе не найден, его получают искусственным путем по ядерной реакции:
Re встречается в качестве примеси в молибденовых, вольфрамовых, платиновых рудах. Получение. Основную массу марганца получают в виде ферромарганца (сплава с железом), восстанавливая смесь пиролюзита и гематита коксом. MnO2 + Fe2O3 + C Mn можно получить алюмотермическим способом: 3Mn3O4 + 8Al Чистый марганец получают электролизом MnSO4 в слабощелочной среде с последующим вакуумным переплавом: катод ⊝: Mn2+ + 2 e – = Mn; 2Н2О + 2 е – = Н2 + 2ОН–; анод ⊝: 2H2O – 4 e – = O2 + 4H+. Re получают из перренатов восстановлением водородом или калием: 2NH4ReO4 + 4H2 2KReO4 + 7H2
Химические свойства
По химической активности Mn значительно превосходит Тс и Re. Марганец при высокой температуре соединяется с кислородом: 3Mn + 2O2 Тс и Re при горении образуют высшие оксиды: 4Re + 7O2 Mn взаимодействует с галогенами, образуя галогениды в низших степенях окисления: Mn + F2 = MnF2 (MnF3); Mn + Г2 = MnГ2 (Г = Cl, Br, I). Tc и Re образуют галогениды в высших степенях окисления. Реакция происходит только при нагревании: (Tc) Re + 3F2 (Tc) Re + Cl2 Mn с азотом образует нитриды: Mn3N2, MnN. Марганец взаимодействует с серой, образуя сульфиды: Mn + S Tc и Re взаимодействуют с неметаллами при сильном нагревании. Mn в расплавленном состоянии взаимодействует с углеродом, образуя металлоподобный карбид (чаще состава Mn3C). С водородом Mn, Tc, Re не реагируют. Марганец растворяет водород при нагревании, образуя твердые растворы внедрения. Поглощение водорода Тс и Re не характерно. Марганец имеет отрицательное значение стандартного электродного потенциала, это довольно активный металл, Тс и Re в ряду напряжений расположены правее водорода. Все элементы подгруппы покрываются пассивирующей пленкой; при разрушении пленки Mn становится реакционноспособным и вытесняет водород из воды и кислот -неокислителей: 3Mn + 4H2O Mn + 2HCl = MnCl2 + H2. С кислотами-окислителями: 3Mn + 8HNO3(разб) = 3Mn(NO3)2 + 2NO + 4H2O. Концентрированная серная и азотная кислоты на холоде пассивируют марганец. Tc, Re с водой и кислотами-неокислителями не реагируют, а концентрированной серной и азотной кислотами окисляются, образуя техницевую и рениевую кислоты:
3Re + 7HNO3 ® 3НReO4 + 7NO + 2H2O. Со щелочами марганец, техниций и рений не взаимодействуют.
|
||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 54; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.137.181.52 (0.011 с.) |

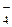 |Tc)
|Tc)
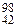 Мо +
Мо + 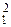 D =
D = 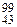 Тс +
Тс + 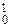 n.
n.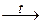 Mn x O y + CO + Fe.
Mn x O y + CO + Fe.


