
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Контроль показателя качества измерений ⇐ ПредыдущаяСтр 3 из 3
1) Методика измерений перманганатной окисляемости в пробах питьевых, природных и сточных вод титриметрическим методом
2)) Методика измерений массовой концентрации общего хлора в питьевых, природных и сточных водах титриметрическим методом
3)Методика измерений массовой концентрации фосфат-ионов в питьевых, поверхностных и сточных водах фотометрическим методом с молибдатом аммония
4)Методика измерений массовой концентрации хлорид-ионов в пробах питьевых, природных (поверхностных и подземных) и сточных вод меркуметрическим методом
11. Обработка, анализ и оформление полученных результатов эксперимента 1) Методика измерений перманганатной окисляемости в пробах питьевых, природных и сточных вод титриметрическим методом Значение перманганатной окисляемости, выраженное в расчете на атомарный кислород в мг/дм3, определяют по формуле:
где: V1 - объем раствора перманганата калия, израсходованного на титрование исследуемой пробы, см3; V2 - объем раствора перманганата калия, израсходованного на титрование холостой пробы, см3; K - поправочный коэффициент к раствору перманганата калия; С - концентрация раствора перманганата калия, равная 0,002 моль/дм3; V - объем пробы, взятой для анализа, см3; Кр - коэффициент разбавления пробы; 8 - атомная масса кислорода; 5 - стехиометрический коэффициент. Если поправочный коэффициент (К) к раствору перманганата калия имеет значение от 0,995 до 1,005, то при вычислении результатов его можно не учитывать.
Хср=2,34 мг/дм3 Х±∆, мг/дм3 (Р=0,95) Значение ∆ рассчитывают по формуле: ∆=0,01*δ*Х ∆=0,01*10*2,34*2 ∆=0,5 2,34*2=4,7 мг/дм3 4,7±0,5, мг/дм3 ,Р=0,95
2)) Методика измерений массовой концентрации общего хлора в питьевых, природных и сточных водах титриметрическим методом Массовую концентрацию "общего хлора", Х (мг/дм3) вычисляют по формуле: Х= Где Vт- объем раствора тиосульфата натрия, израсходованного на титрование анализируемой пробы, см3; Vпробы - аликвотная часть пробы, взятая для анализа, см3; M- концентрация раствора тиосульфата натрия, моль/дм3; K- поправочный коэффициент к титру раствора тиосульфата натрия;
Хср=2,065 мг/дм3 |X1-X2|≤0,01*r*Хср |2,05-2,08|≤0,01*11*2,07 0,03≤0,23 (Хср±∆), мг/дм3 ,Р=0,95 Где ∆ - показатель точности методики Значение ∆ рассчитывают по формуле: ∆=0,01*δ*Хср ∆=0,01*12*2,07
∆=0,25 2,07±0,25, мг/дм3 ,Р=0,95 3)Методика измерений массовой концентрации фосфат-ионов в питьевых, поверхностных и сточных водах фотометрическим методом с молибдатом аммония Массовую концентрацию фосфат-ионов Х,(мг/дм3) рассчитывают по формуле:
Где C- массовая концентрация фосфат-ионов, найденная по градуировочному графику, мг/дм3 50- объем, до которого была разбавлена проба, см3 V-объем, взятый для анализа, см3
Хср=1,58 мг/дм3 |X1-X2|≤0,01*r*Хср |1,57-1,59|≤0,01*11*1,58 0,2≤0,17 4)Методика измерений массовой концентрации хлорид-ионов в пробах питьевых, природных (поверхностных и подземных) и сточных вод меркуметрическим методом
Массовую концентрацию хлорид-ионов в анализируемой пробе, Х(мг/дм3),рассчитывают по формуле:
Где Vn-объем раствора нитрата ртути (),пошедший на титрование анализируемой пробы,см3; V0- объем раствора нитрата ртути (),пошедший на титрование холостой пробы,см3; C-молярная концентрация эквивалента раствора ртути (),моль/дм3; 35,45-молярная масса эквивалента хлорид-иона, г/моль; V-объем пробы, взятый для анализа, см3; 1000-коэффициент перевода г в мг; cv-коэффициент, равный 1,03, при использовании суспензии гидроксида алюминия для устранения цветности (в иных случаях 1)
Хср=6,21 моль/дм3 |X1-X2|≤0,01*r*Хср |7,09-5,32|≤0,01*10*6,21 1,77≤0,621
Список литературы: ПНД Ф 112 Фосфаты ПНД Ф 113 Общий хлор ПНД Ф 154 Перманганатная окисляемость ПНДФ 111 Хлорид-ион
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-06-14; просмотров: 55; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.19.30.232 (0.009 с.) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

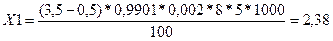 мг/дм3
мг/дм3 мг/дм3
мг/дм3
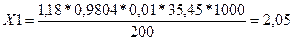 мг/дм3
мг/дм3 мг/дм3
мг/дм3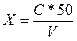
 мг/дм3
мг/дм3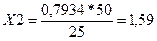 мг/дм3
мг/дм3
 моль/дм3
моль/дм3 моль/дм3
моль/дм3


