Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Стромально–клеточные опухоли (андробластома, опухоль Сертоли).
Андробластома относится к гормонально–активным маскулинизирующим опухолям и составляет около 1,5–2% всех новообразований яичников. Это маскулинизирующая гормонпродуцирующая опухоль, содержащая клетки Сертоли–Лейдига (хилюсные и стромальные). Образующиеся в избытке андрогены угнетают функцию гипофиза, и в организме снижается выработка эстрогенов. Опухоль преимущественно доброкачественная. Андробластома встречается у пациенток до 20 лет и у девочек, в этих наблюдениях нередко отмечается цзосексуальлое преждевременное половое созревание. Диаметр образования от 5 до 20 см. Капсула часто четко выражена, строение нередко дольчатое, на разрезе опухоль солидная, желтоватого, оранжевого или оранжево–серого цвета. Сохранившийся другой яичник всегда атрофичен. Фиброзно изменен, как у женщин в постменопаузе. Основное клиническое проявление опухоли – вирилизация. На фоне общего здоровья возникает аменорея, отмечается бесплодие, уменьшаются молочные железы (дефеминизация), позднее появляются признаки маскулинизации – грубеет голос, развивается оволосение по мужскому типу (гирсутизм), повышается либидо, уменьшается толщина подкожной жировой клетчатки, возникает гипертрофия клитора, контуры тела и лица приобретают мужские черты. Симптомы заболевания обычно развиваются постепенно. Клинические проявления в основном зависят от возраста. В репродуктивном периоде пациентка обращается к врачу, как правило, по поводу аменореи и бесплодия. В период климактерия и постменопаузы в большинстве наблюдений клинические признаки считают возрастными явлениями и лишь при развитии маскулинизации пациентки обращаются к врачу. Опухоль развивается медленно, поэтому более раннее обращение к врачу обычно связано с болями внизу живота (при осложнениях). Диагноз устанавливают на основании клинической картины и данных двуручного влагалищно–абдоминального исследования, а также УЗИ с ИД К При гинекологическом исследовании опухоль определяется сбоку от матки, она односторонняя, подвижная, безболезненная, диаметром от 5 до 20 см, овальной формы, плотной консистенции, с гладкой поверхностью. При УЗИ выделяют солидный, кистозный и кистозно–солидный типы. Эхографическая картина показывает неоднородное внутреннее строение с множественными гиперэхогенными участками и гипоэхогенными включениями.
Допплерография не имеет определенного значения в определении морфологической структуры опухоли, но иногда помогает обнаружить опухоль. Лечение вирилизирующих опухолей яичника оперативное, применяют как лапаротомический, так и лапароскопический доступ. Объем и доступ при оперативном лечении зависят от возраста больной, величины и характера объемного образования. При андробластоме у девочек и пациенток репродуктивного возраста достаточно удалить придатки матки на пораженной стороне. У больных в постменопаузе выполняют надвлагалищную ампутацию матки с придатками. После удаления опухоли функции организма женщины восстанавливаются в такой же последовательности, в какой развивались симптомы заболевания. Облик женщины меняется очень быстро, восстанавливаются менструальная и репродуктивная функции, но огрубение голоса, гипертрофия клитора и гирсутизм могут оставаться на всю жизнь. При подозрении на злокачественную опухоль показаны пангистерэктомия и удаление сальника. Прогноз при доброкачественной опухоли благоприятный.
Герминогенные опухоли
Герминогенные новообразования возникают из первичных половых клеток эмбриональных гонад и их производных, из трех зародышевых листков – эктодермы, мезодермы и эндодермы.
Дисгерминома
Дисгерминома (семинома яичника) – злокачественная опухоль яичника, обладает выраженным сходством с соответствующей тестикулярной опухолью. Дисгерминомы составляют около 1–2% опухолей яичников и около 3% всех злокачественных опухолей. Наиболее часто выявляются в возрасте от 10 до 30 лет (примерно в 5% наблюдений до 10 лет и очень редко после 50 лет). Дисгерминома представляет собой самую частую злокачественную опухоль при беременности. Состоит из клеток, морфологически сходных с примордиальными фолликулами. Считают, что дисгерминомы происходят из первичных герминогенных элементов. В норме к моменту рождения все половые клетки находятся в составе примордиальных фолликулов, половые клетки, не образующие фолликулов, погибают. Если этого не происходит, то половые клетки приобретают способность к бесконтрольной пролиферации и дают начало опухоли. Дисгерминома возникает у подростков и молодых женщин при общем и генитальном инфантилизме с поздним менархе. Часто наблюдаются аномалии наружных половых органов. Опухоль, как правило, односторонняя.
Типичная дисгерминома представлена солидной опухолью округлой или овоидной формы с гладкой белесоватой фиброзной капсулой. Опухоль может достигать значительных размеров, полностью замещая ткань яичника, дисгерминома при небольших узлах имеет различную консистенцию. На разрезе ткань опухоли желтоватая, бледно–бурая с розовым оттенком. Большие опухоли обычно пестрые из–за кровоизлияний и очагов некроза различной давности. Клинические проявления не имеют специфических признаков. Гормональная активность дисгерминоме не свойственна. Жалобы больных неспецифические, иногда появляются тупые тянущие боли внизу живота, общее недомогание, дизурические явления, слабость, сонливость, утомляемость, нередко нарушен менструальный цикл: длительная аменорея может сменяться маточными кровотечениями. Дисгерминома склонна к быстрому росту, метастатическому распространению и прорастанию в соседние органы. Метастазирование обычно происходит лимфогенным путем с поражением лимфатических узлов общей подвздошной артерии, дистальной части брюшной аорты и надключичных лимфатических узлов. Гематогенные метастазы встречаются в терминальной стадии заболевания, чаще в печени, легких, костях. Проявления метастазов дисгерминомы сходны с картиной первичной опухоли. Диагноз устанавливают на основании клинического течения заболевания, данных двуручного гинекологического исследования, УЗИ с ЦДК и морфологического исследования удаленного макропрепарата. При гинекологическом исследовании опухоль располагается обычно позади матки, чаще односторонняя, округлая, с нечеткими контурами, плотная, бугристая, диаметром от 5 до 15 см (чаще достигает больших размеров), в начальной стадии подвижная, безболезненная. Большую помощь оказывают УЗИ с ЦДК. На эхограммах опухоль имеет эхопозитивное средней эхогенности, часто дольчатое строение. Внутри новообразования нередки участки дегенеративных изменений, контуры неровные, форма неправильная. При допплерометрическом исследовании определяются множественные участки васкуляризации как по периферии, так и в центральных структурах опухоли: с низким ИР (‹0,4). Лечение дисгерминомы только хирургическое с последующей лучевой терапией. Целесообразно использовать лапаротомический доступ. При односторонней опухоли без признаков распространения за пределы пораженного яичника у молодых женщин, планирующих иметь в дальнейшем детей, можно ограничиться удалением придатков матки на пораженной стороне. У пациенток перименопаузального возраста выполняют экстирпацию матки с придатками, удаляют сальник. Во время операции не следует нарушать целостность капсулы, поскольку это значительно ухудшает прогноз. При распространении опухоли за пределы яичника показана более радикальная операция – удаление матки с придатками и сальника с последующей рентгенотерапией. Увеличенные лимфатические узлы подлежат удалению, а их область – рентгенотерапии. Как первичная опухоль, так и метастатические узлы хорошо поддаются рентгенотерапии. Чистые формы дисгермином высокочувствительны к лучевой терапии, что и определяет относительно благоприятный прогноз заболевания.
При правильном лечении возможно полное выздоровление. В настоящее время 5–летняя выживаемость больных с односторонней инкапсулированной дисгерминомой без метастазов достигает 90%. В прогностическом плане неблагоприятны метастазы и прорастание за пределы яичника, большие размеры и двусторонняя локализация дисгерминомы.
Тератомы.
Зрелая тератома относится к герминогенным опухолям. В зависимости от дифференцировки тканей тератомы делят на зрелые (дермоидная киста) и незрелые (тератобластома). Зрелые тератомы подразделяются на солидные (без кист) и кистозные (дермоидная киста). Выделяют и монодермальные тератомы – струму яичника и карциноид яичника; их строение идентично обычной ткани щитовидной железы и кишечным карциноидам. Зрелая кистозная тератома – одна из наиболее распространенных опухолей в детском и юношеском возрасте; может встречаться даже у новорожденных, что косвенно свидетельствует о ее тератогенном происхождении. Зрелая тератома встречается в репродуктивном возрасте, в постменопаузальном периоде (как случайная находка). Она состоит из хорошо дифференцированных производных всех трех зародышевых листков с преобладанием эктодермальных элементов (отсюда термин «дермоидная киста»). Опухоль является однокамерной кистой (многокамерное строение наблюдается редко), всегда доброкачественная и лишь изредка проявляет признаки малигнизации. В структуру дермоидных кист включен так называемый дермоидный бугорок, в котором выявляются зрелые ткани и рудиментарные органы. Капсула дермоидной кисты плотная, фиброзная, различной толщины, поверхность гладкая, блестящая. Тератома на разрезе напоминает мешок, содержащий густую массу, состоящую из сала и волос, в виде клубков или прядей различной длины, нередко встречаются и хорошо сформированные зубы. Внутренняя поверхность стенки выстлана цилиндрическим или кубическим эпителием. При микроскопическом исследовании определяются ткани эктодермального происхождения – кожа, элементы невральной ткани – глия, нейроциты, ганглии. Мезодермальные производные представлены костной, хрящевой, гладкомышечной, фиброзной и жировой тканью. Производные эндодермы встречаются реже и обычно включают бронхиальный и гастроинтестинальный эпителий, ткань щитовидной и слюнной желез. Объектом особо тщательного гистологического исследования должен быть дермоидный бугорок с целью исключения малигнизации.
Симптоматика дермоидных кист мало отличается от таковой доброкачественных опухолей яичников. Дермоидная киста не обладает гормональной активностью, редко обусловливает жалобы. Общее состояние женщины, как правило, не страдает. Болевой синдром отмечается в небольшом числе наблюдений. Иногда появляются дизурические явления, ощущение тяжести внизу живота. В ряде случаев происходит перекрут ножки дермоидной кисты, возникает симптоматика «острого живота», требующая экстренного оперативного вмешательства. Дермоидная киста нередко сочетается с другими опухолями и опухолевидными образованиями яичников. Чрезвычайно редко при зрелой тератоме возникает злокачественный процесс, в основном плоскоклеточный рак. Диагноз устанавливают на основании клинического течения заболевания, двуручного гинекологического исследования, применения УЗИ с ЦДК, лапароскопии. При гинекологическом исследовании опухоль располагается в основном кпереди от матки; она округлой формы, с гладкой поверхностью, имеет длинную ножку, подвижная, безболезненная, плотной консистенции. Диаметр зрелой тератомы – от 5 до 15 см. Дермоидная киста с включением костных тканей – единственная опухоль, которую можно определить на обзорном рентгеновском снимке брюшной полости. Эхография способствует уточнению диагноза зрелых тератом (выраженный акустический полиморфизм). Зрелые тератомы имеют гипоэхогенное строение с солитарным эхогенным включением, с четкими контурами. Непосредственно за эхогенным включением располагается акустическая тень. Зрелые тератомы могут иметь нетипичное внутреннее строение. Внутри опухоли визуализируются множественные небольшие гиперэхогенные включения. В ряде случаев за мелкоштриховыми включениями визуализируется слабый эффект усиления – «хвост кометы». Возможно кистозно–солидное строение с плотным компонентом с высокой эхогенностью, округлой или овальной формы, с ровными контурами. Полиморфизм внутреннего строения опухоли нередко создает сложности в трактовке эхографических картин (рис. 16.18). При ЦДК в зрелых тератомах практически всегда отсутствует васкуляризация, кровоток может визуализироваться в прилегающей к опухоли ткани яичника, ИР – в пределах 0,4. В качестве дополнительного метода в диагностике зрелых тератом после применения УЗИ возможно использовать КТ. При лапароскопии дермоидная киста неравномерного желтоватобелесоватого цвета, при пальпации манипулятором консистенция плотная. Определенное дифференциально–диагностическое значение имеет расположение кисты в переднем своде, в отличие от опухолей других видов, обычно располагающихся в маточно–прямокишечном пространстве. Ножка дермоидной кисты обычно длинная, тонкая, на капсуле могут быть мелкие кровоизлияния.
Лечение зрелых тератом хирургическое. Объем и доступ оперативного вмешательства зависят от величины объемного образования, возраста пациентки и сопутствующей генитальной патологии. У молодых женщин и девочек следует по возможности ограничиться частичной резекцией яичника в пределах здоровой ткани (кистэктомия). Предпочтительно использовать лапароскопический доступ с применением эвакуирующего мешочка. У пациенток перименопаузального возраста показана надвлагалищная ампутация матки с придатками с обеих сторон. Допустимо удаление придатков матки с пораженной стороны, если матка не изменена. Прогноз благоприятный.
Тератобластома (незрелая тератома)
Относится к злокачественным новообразованиям яичника. Опухоль чрезвычайно незрелая, дифференцировка низкая. Незрелая тератома встречается гораздо реже, чем зрелая. Опухоль имеет тенденцию к быстрому росту и может достигать значительных размеров. При микроскопическом исследовании определяется сочетание производных всех 3 зародышевых слоев. Поверхность разреза обычно пестрая, от бледно–серого до темно–бурого цвета. При осмотре определяются кости, хрящи, волосы, опухоль содержит жировые массы. Опухоль обычно располагается сбоку от матки. Она односторонняя, неправильной формы, неравномерно мягкой, местами плотной консистенции – в зависимости от преобладающего типа тканей и некротических изменений, большого размера, с бугристой поверхностью, малоподвижная, чувствительная при пальпации. При прорастании капсулы имплантируется в брюшину, дает метастазы в забрюшинные лимфатические узлы, легкие, печень, головной мозг. Метастазы незрелой тератомы, как и основная опухоль, обычно состоят из различных тканевых элементов с наиболее незрелыми структурами. Больные жалуются на боли внизу живота, общую слабость, вялость, повышенную утомляемость, снижение трудоспособности. Менструальная функция чаще не нарушена. В анализе крови отмечаются изменения, присущие злокачественным опухолям. При быстром росте клиническая картина из–за интоксикации, распада и метастазирования опухоли схожа с таковой при общесоматических заболеваниях. Это часто обусловливает неадекватное лечение. К моменту распознавания опухоль уже бывает запущенной. Применение эхографии с ЦДК способствует уточнению диагностики. Эхографические картины отражают смешанное, кистозно–солидное строение незрелой тератомы с неровными нечеткими контурами. Подобно всем злокачественным вариантам опухолей незрелая тератома имеет хаотическое внутреннее строение с выраженной неоваскуляризацией. При ЦДК визуализируется выраженная мозаичная картина с турбулентным кровотоком и преимущественно центрально расположенными артериовенозными шунтами. Индекс периферического сопротивления снижен (ИР ‹0,4). Лечение хирургическое. Допустимы надвлагалищная ампутация матки с придатками и удаление сальника. Незрелые тератомы малочувствительны к лучевой терапии, но иногда могут реагировать на комбинированную химиотерапию. Прогноз неблагоприятный.
Рак яичников
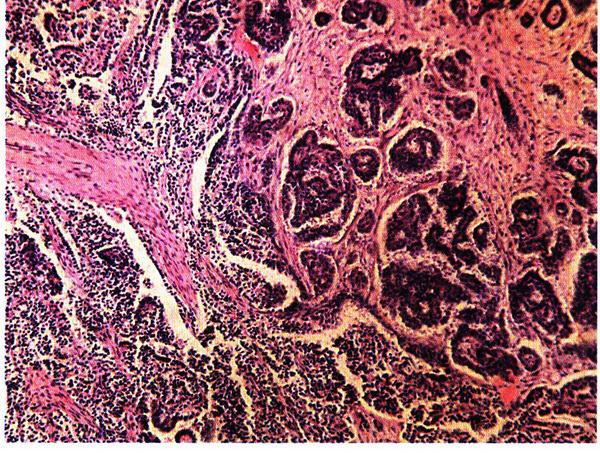
Ранняя диагностика и лечение рака яичников остается одной из самых сложных проблем онкологии. За последнее 10–летие как в России, так и во всем мире наметилась отчетливая тенденция к росту заболеваемости раком яичников. Он стабильно занимает 2–е место в структуре опухолей гинекологической локализации (после рака шейки матки), а по смертности остается на 1–м месте. В настоящее время этиологические факторы злокачественных опухолей яичников достоверно не определены. Существуют три основные гипотезы. Согласно первой, опухоли яичников возникают в условиях гиперактивности гипоталамо–гипофизарной системы, результатом чего становится хроническая гиперэстрогения. Эстрогены непосредственно не приводят к опухолевой трансформации клетки, но создают условия, при которых повышается вероятность возникновения рака в эстрогенчувствительных тканях. Другая гипотеза основана на представлениях о «непрекращающейся овуляции» (раннее менархе, поздняя менопауза, малое число беременностей, укорочение лактации). Постоянные овуляции приводят к повреждению эпителия коркового слоя яичника, что, в свою очередь, увеличивает вероятность возникновения аберрантных повреждений ДНК с одновременной инактивацией опухольсупрессирующих генов. Согласно третьей, генетической гипотезе, к категории лиц высокого риска относятся члены семей с аутосомно–доминантным раком молочной железы и яичников. По данным мировой литературы, наследственные формы рака яичников обнаруживают только у 5–10% больных. Успехи генной инженерии позволили выявить ряд онкогенов, экспрессия которых ассоциирована с семейными формами рака яичников. Существует зависимость между частотой опухолей различных морфологических типов и возрастом пациенток. Пик заболеваемости раком яичников отмечается между 60 и 70 годами жизни, но в последнее время он фиксируется на 10–летие раньше. Рак яичников бывает первичным, вторичным и метастатическим. Удельная частота первичного рака составляет не более 5%. При первичном раке опухоль формируется из покровного эпителия яичника, следовательно, в ней отсутствует смешение доброкачественных и злокачественных элементов. Первичным раком называют злокачественные опухоли, первично поражающие яичник. По гистологическому строению первичный рак яичников – это злокачественная эпителиальная опухоль железистого или папиллярного строения (рис. 16.19).
Рис. 16.19. Серозный папиллярный рак яичника (серозная цистаденокарцинома). Окраска гематоксилином и эозином, х 200. Фото О.В. Зайратьянца
Вторичный рак яичников (цистаденокарцинома) встречается наиболее часто и составляет 80–85% всех форм рака яичников; развивается на фоне доброкачественных или пограничных опухолей. Наиболее часто вторичный рак яичников возникает в серозных папиллярных, реже – в муцинозных цистаденомах. К вторичным поражениям яичников относится также эндометриоидная цистаденокарцинома. Метастатический рак яичников (опухоль Крукенберга) представляет собой метастаз из первичного очага, который чаще всего располагается в желудочно–кишечном тракте, желудке, молочной железе, щитовидной железе, матке. Метастазы из злокачественных опухолей желудочно–кишечного тракта распространяются гематогенным, ретроградно–лимфогенным и имплантационным путями. Метастазы обычно двусторонние. В 60–70% наблюдений возникает асцит. Опухоль растет очень быстро. Макроскопически метастатическая опухоль белесоватая, бугристая, на разрезе нередко волокнистая. Может быть плотной или тестоватой консистенции, что зависит от соотношения стромы и паренхимы опухоли, а также от вторичных изменений в виде отека или некроза. Микроскопически при метастатическом раке определяют перстневидные круглые клетки, наполненные слизью. В настоящее время принята Единая международная классификация, которая отражает как стадию процесса, так и гистологический тип опухоли. Стадию опухолевого процесса устанавливают на основании данных клинического обследования и во время операции.
Классификация рака яичников 1. Стадия I – опухоль ограничена одним яичником. 2. Стадия II – опухоль поражает один или оба яичника с распространением на область таза. 3. Стадия III – распространение на один или оба яичника с метастазами по брюшине за пределы таза и (или) метастазы в забрюшинных лимфатических узлах. 4. Стадия IV – распространение на один или оба яичника с отдаленными метастазами.
Клиническая картина.
Многообразие морфологических форм – одна из причин неоднородности клинического течения рака яичников. Патогномоничных признаков нет. Локализованные формы рака яичников, как правило, остаются бессимптомными, у молодых пациенток иногда возникает болевой синдром вплоть до выраженной картины «острого живота» (22%) в связи с возможностью перекрута ножки или перфорацией капсулы опухоли. У остальных пациенток симптоматика появляется в связи с распространенностью опухолевого процесса: интоксикация, похудение, общая слабость, недомогание, повышенная утомляемость, снижение и извращение аппетита, повышение температуры, нарушение функции желудочно–кишечного тракта (тошнота, рвота, ощущение распирания в подложечной области, тяжесть внизу живота, запор, чередующийся с поносом, дизурические явления). Живот увеличивается из–за асцита. Может быть выпот в одной или обеих плевральных полостях. Появляются признаки сердечно–сосудистой и дыхательной недостаточности, отеки на нижних конечностях. Диагностика злокачественной опухоли может быть затруднена из–за отсутствия пагогномоничных симптомов на ранних стадиях заболевания. Злокачественные новообразования не имеют явных клинических признаков, отличающих их от доброкачественных опухолей. В связи с этим особого внимания требуют пациентки группы высокого риска по развитию опухолей яичника. Это женщины с нарушением функции яичников, длительно наблюдающиеся по поводу тубоовариальных воспалительных образований, рецидивирующих гиперпластических процессов эндометрия в постменопаузе, ранее оперированные по поводу доброкачественных опухолей яичников, пациентки с нарушением фертильной функции. При двуручном гинекологическом исследовании чаще определяются двусторонние опухоли овальной или неправильной формы, с бугристой поверхностью, плотной консистенции, различной величины, ограниченно подвижные и (или) неподвижные. За маткой пальпируются плотные безболезненные выступающие в прямую кишку образования – «шипы». При раке яичников, как правило, выражен асцит. Ректовагинальное исследование необходимо для определения инвазии ракового процесса в параректальную и параметральную клетчатку. Современная диагностика злокачественных опухолей яичников включает трансвагинальную эхографию с применением акустических излучателей, обладающих высокой разрешающей способностью, и ЦДК, которое позволяет визуализировать кровоток органа. Измерение кровотока в систолу и диастолу позволяет судить о резистентности кровотока путем вычисления показателей периферического сосудистого сопротивления. Эхографически выявляется объемное образование значительных размеров, нередко двустороннее, неправильной формы, с толстой, неровной капсулой, с множественными папиллярными разрастаниями и перегородками (рис. 16.20, 16.21). Перегородки, как правило, неодинаковой величины, в малом тазу и в брюшной полости определяется свободная жидкость (асцит). При цветовой допплерографии в злокачественных опухолях яичника определяют множество сосудов (зоны неоваскуляризации) как по периферии, так и в центральных структурах опухоли на перегородках и в папиллярных разрастаниях с низкой резистентностью кровотока (ИР ‹0,4) (рис. 16.22, 16.23).
КТ и МРТ. На компьютерных томограммах злокачественные новообразования визуализируются как объемные образования, с неровными, бугристыми контурами, неоднородной внутренней структурой (участки жидкостной и мягкотканной плотности), утолщенной капсулой с внутренними перегородками неодинаковой толщины. КТ позволяет определить четкие границы между маткой, мочевым пузырем и кишечником и тем самым выявить спаечный процесс в малом тазу. Лапароскопия дает возможность произвести биопсию с морфологическим исследованием гистиотипа материала и цитологическое исследование перитонеальной жидкости. Содержание опухолево–ассоциированных антигенов в сыворотке крови больных коррелирует с течением заболевания. Наибольшее значение имеют маркеры СА–125, СА–19.9, СА–72.4. СА–125, которые обнаруживаются у 78–100% больных раком яичников. Уровень СА–125 превышает норму (35 МЕ/мл). При начальных формах опухолевого процесса специфичность СА–125 невысока, поэтому опухолевый маркер нельзя использовать в качестве скрининг–теста. Большую ценность СА–125 представляет в качестве контроля эффективности лечения распространенных форм заболевания и при последующем мониторинге. У 80–85% пациенток диагноз можно установить с помощью перечисленных методов, хотя в ряде случаев окончательный диагноз возможен во время лапаротомии (рис. 16.24).
Алгоритм обследования пациенток с подозрением на рак яичника: 1. двуручное влагалищное и ректовагинальное исследование; 2. УЗИ органов малого таза с ЦДК; 3. УЗИ яичникового образования в режиме 3D; 4. УЗИ брюшной полости, щитовидной железы, молочной железы; 5. РКТ; 6. МРТ; 7. маммография; 8. рентгеноскопия, гастроскопия, ирригоскопия, колоноскопия; 9. рентгеноскопия органов грудной клетки; 10. хромоцистоскопия.
Целесообразно произвести рентгеноскопию органов грудной клетки для исключения метастазов. Стадию злокачественного процесса, кроме перечисленных методов, позволяет уточнить хромоцистоскопия (особенно при больших неподвижных опухолях яичника). Больных с диагностированной или подозреваемой опухолью яичника (независимо от стадии) необходимо оперировать.
Лечение.
При выборе тактики лечения больных раком яичников следует учитывать стадию процесса, морфологическую структуру опухоли, степень дифференцировки, потенциальную чувствительность данного гистиотипа опухоли к химиотерапии и лучевому лечению, отягощающие факторы, возраст больной, иммунный статус, хронические заболевания как противопоказание к проведению того или иного метода лечения. Лечение рака яичников всегда комплексное. Ведущим, хотя и не самостоятельным, методом остается хирургический: экстирпация матки и придатков и экстирпация больного сальника. При чревосечении используют нижнесрединную лапаротомию. Это обеспечивает выведение опухоли в рану без нарушения ее капсулы, создает условия для тщательной ревизии органов брюшной полости, дает возможность при необходимости выполнить операцию в полном объеме. У некоторых больных (ослабленных, пожилых, с выраженной экстрагенитальной патологией) можно ограничиться надвлагалищной ампутацией матки с придатками и субтотальной резекцией большого сальника. Большой сальник обязательно удаляют и подвергают морфологическому исследованию. Удаление сальника предотвращает развитие в последующем асцита (рис. 16.25). У больных молодого возраста со злокачественными новообразованиями допустимы удаление придатков матки на пораженной стороне, резекция другого яичника и субтотальная резекция большого сальника. Подобные операции можно выполнять только больным со злокачественной трансформацией яичника I стадии. При II стадии рака яичников производят радикальную операцию, которая предусматривает экстирпацию матки с придатками и резекцию сальника. Точно установить стадию заболевания можно только при тщательной ревизии брюшной полости. Обязательно исследуют перитонеальную жидкость, производят ревизию парааортальных лимфатических узлов. Увеличенные лимфатические узлы пунктируют или осуществляют их биопсию для цитоморфологического исследования. При сомнении в операбельности больной хирургическое вмешательство целесообразно выполнить на 2–м этапе, после химиотерапии, которая повышает радикальность оперативного лечения в последующем.
|
|||||||||
|
Последнее изменение этой страницы: 2021-07-19; просмотров: 65; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.133.228 (0.065 с.) |