
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Впервые получен в 1825 году датским физиком Эрстедом.Стр 1 из 3Следующая ⇒
МЕТАЛЛУРГИЯ ЛЕКГИХ МЕТАЛЛОВ
МЕТАЛЛУРГИЯ АЛЮМИНИЯ
Свойства алюминия Впервые получен в 1825 году датским физиком Эрстедом. Находится в III группе 3-го периода. Порядковый номер 13. Молекулярная масса 26,98 г/моль. Температура плавления 660оС. Температура кипения 2500оС. Алюминий обладает малой плотностью, высокой пластичностью, электро-и теплопроводностью. Многие физические свойства алюминия изменяются в зависимости от его чистоты. Чем чище алюминий, тем выше его температура плавления и электропроводность, и ниже плотность. Алюминий обладает высокой химической активностью по отношению к кислороду, сере, углероду и галоидам. В ряду напряжений алюминий занимает место среди электроотрицательных элементов, что делает невозможным его электрохимическое выделение из водных растворов его солей. Взаимодействие алюминия с кислородом воздуха приводит к образованию на его поверхности тонкой, но очень прочной пленки, которая придает алюминию коррозионную стойкость. Вследствие высокого сродства к кислороду алюминий восстанавливает оксиды многих металлов до металлического состояния. При нагреве алюминий легко растворяется в разбавленных азотной и серной кислотах, холодная азотная кислота его пассивирует. Алюминий хорошо растворяется в щелочах с образованием алюминатов. В органических кислотах и воде он устойчив. Применение: электрические провода, химическая аппаратура, фольга, электроконденсаторы, отражательные стекла в телескопах, атомная энергетика, радиотехника, производство стали и сплавов.
Сырье для получения алюминия Алюминий занимает третье место по распространению (кислород, кремний). Из-за высокой химической активности алюминий встречается в природе только в виде соединений. Известно 250 минералов. Минерал Содержание Al 2 O 3, % Боксит формулы нет Корунд Al2O3 100 Диаспор, бёмит Al2O3*H2O 85 Шпинель Al2O3*MgO 71 Гидраргиллит Al2O3*3H2O 65.4 Каолинит Al2O3*2SiO2*2H2O 39.5
Алунит K2SO4*AL2(SO4)3*4Al(OH)3 37 Нефелин (Na,K)2O*AL2O3*2SiO2 32.3-35.9 Ортоклаз K2O*Al2O3*6SiO2 18.4 Альбит Na2O*Al2O3*6SiO2 19.3 Бокситы являются самой распространенной рудой. Бокситом называется горная порода, состоящая из гидратированных оксидов алюминия, железа, кремния, титана и других элементов. Химический состав в бокситах изменяется в очень широких пределах. По внешнему виду бокситы похожи на глину. Цвет от белого до темно-красного. Качество бокситов определяется кремниевым модулем.
Процесс получения металлического алюминия достаточно сложен и состоит из четырех отдельных технологий: 1. Производство глинозема; 2. Производства криолита и фтористых солей; 3. Производство угольных изделий; 4. Производство алюминия.
Технологическая схема получения алюминия Производство глинозема способом Байера
Используется высококачественный боксит с низким содержание кремнезема. Выщелачивание боксита Цель: перевод глинозема и щелочи в раствор. Растворитель: едкий натр NaOH Продукты выщелачивания: алюминатный раствор и красный шлам Оборудование: автоклав с глухим и острым паром Декомпозиция алюминатного раствора Цель: разложение раствора с выделением в осадок Al (OH)3 Реакция декомпозиции: NaAlO 2 + H 2 O = Al (OH)3+ NaOH Продукты декомпозиции: Al (OH)3 и маточный раствор Оборудование: декомпозер с воздушным и механическим перемешиванием Кальцинация Al (OH)3 Цель: обезвоживание Al (OH)3 с целью получения негигроскопичного глинозема Реакция: Al (OH)3= Al2O3+H2O Оборудование ТВП
МЕТАЛЛУРГИЯ МАГНИЯ
Свойства магния Магний – широко распространенный в природе элемент, относится к числу «молодых» металлов. В первые магний в металлическом состоянии был получен в 1808 году Г.Деви. В промышленном масштабе производство магния было организовано в 60-е годы 19 века в Англии и США. В нашей стране первые исследования по получению магния были начаты в 1914-1915 годах. Первый завод по производству магния в СССР в 1935 году в Запорожье, второй завод в 1936 году в Саликамске, в 1943 году в Березники.
Магний находится во второй группе 3-го периода таблицы Менделеева. Периодический номер 12. Молекулярная масса 24,305 г/моль. Температура плавления 650ОС, Температура кипения 1095оС. Распространенность магния в земной коре 1,87% (6 место). Магний - металл серебристо-белого цвета. В сухом воздухе на поверхности металлического магния образуется оксидная пленка, которая защищает металл от коррозии. Влажная среда значительно снижает коррозионную стойкость магния. Тушение магния водой недопустимо, т.к. при воздействии с парами воды образуется Mg(OH)2. Магний хорошо противостоит действию плавиковой и хромовой кислот и растворов едких щелочей. Магний устойчив по отношению к минеральным маслам, бензину и керосину. Магний хорошо растворяется в большинстве кислот и нестоек в водных растворах солей. Химическая активность магния резко возрастает при увеличении в нем содержания примесей. Магний в виде порошка или тонкой ленты легко воспламеняется и горит ярким пламенем. В виде слитков он не горит. Загорание компактного металла может произойти при температурах вблизи точки плавления металла и выше. Предохраняют расплавленный металл от возгорания с помощью покровных флюсов, изолирующих магний от контакта с кислородом окружающей среды. Применение магния В основном магний потребляют в виде сплавов. Легирование магния алюминием и цинком повышает механические и литейные свойства сплавов, марганец улучшает коррозионную стойкость. Важнейшая особенность магниевых сплавов- их невысокая плотность при относительно высокой механической прочности. Они также хорошо воспринимают ударные нагрузки, немагнитны и не дают искры при ударах и трении. Все выше названные свойства позволяют применять магний в авиационной, автомобильной промышленности, в приборостроении и машиностроении. В цветной металлургии магний применяют в качестве восстановителя при получении металлов: ванадий, хром, титан, цирконий, уран. Черная металлургия использует магний при раскислении некоторых марок сталей и в качестве модификатора при получении сверхпрочного чугуна. Способность магния давать при горении яркий свет и высокую температуру используют в военной технике для изготовления осветительных, зажигательных и трассирующих снарядов и авиационных бомб. Ряд соединений магния используется в резиновой промышленности в качестве наполнителя, для очистки нефтепродуктов, а также в радио- и электротехнике. Природный силикат магния – асбест – широко применяют в качестве электро- и теплоизоляции. Сырье для получения магния
В природе магний встречается только в виде соединений.
Минералы магния Магнезит MgCO 3 Доломит MgCO 3 * CaCO 3 Бишофит MgCl 2 *6 H 2 O Карналлит KCl * MgCl 2 *6 H 2 O Кизерит MgSO 4 * H 2 O Каинит MgSO 4 * KCl *3 H 2 O Лангбейнит 2 MgSO 4 * K 2 SO 4 * H 2 O Змеевик 2 MgO *2 SiO 2 *2 H 2 O Оливин MgSiO 4 Брусит Mg (OH)2 Также соединения магния находятся в воде морей, океанов и соляных озер. Магнезит – теоретически содержит 47,82%MgO и 52,18%CO2.твердость 3-5, плотность 2,9-3,1г/см3. Месторождения: Урал(Саткинское), Красноярский край, Хабаровский край, Иркутская область, Казахстан, Киргизия. Доломит – содержит 30,4%CaO, 21.8%MgO, 47.8%CO2. Твердость 3,5-4, плотность 2,86г/см3. Месторождения: Московская область, ленинградская область, Урал.
Карналлит – природная кристаллическая порода, имеющая разнообразную окраску в зависимости от присутствующих примесей. Отличается высокой гигроскопичностью. Содержит 34,5%MgCl2, 38.8%H2O, 26.7%KCl. Твердость 1-2, плотность 1,618г/см3. Месторождения: Урал, Украина.
Обезвоживание
МЕТАЛЛУРГИЯ ТИТАНА Свойства титана Открыт в 1791 году. Находится в IV группе 4-го периода Порядковый номер 22. Молекулярная масса 47,9 г/моль Температура плавления 1668оС Температура кипения 3330оС По внешнему виду титан похож на сталь. Его механическая прочность в два раза больше, чем у чистого железа и в 6 раз выше, чем у алюминия. В чистом виде титан пластичен и легко поддается механической переработке. На воздухе при обычной температуре титан устойчив. При нагреве выше 550оС он энергично окисляется и поглощает кислород и другие газы. Газы и многие другие примеси придают титану хрупкость. Разбавленная серная, а также азотная кислоты любой концентрации и слабые растворы щелочей реагируют с титаном медленно. Титан растворяется в соляной кислоте, концентрированной серной и плавиковой кислотах.
Сырье для получения титана
Рутил, брукит, анатаз –TiO2 Ильменит – FeTiO3 Титановые руды подвергают обогащению методом гравитации, магнитной сепарации. Технология получения титана При восстановительной плавки оксиды железа восстанавливаются до металлического состояния с получением чугуна, а титан в виде TiO2 переходит в шлак. Оборудование: рудно-термическая печь. В качестве восстановителя используют кокс или антарцит. Полученный шлак подвергают хлорированию по реакции: TiO2+Cl2+C=TiCl4+CO Затем после очистки технического тетрахлорида от примесей ректификацией его подвергают магниетермическому восстановлению до металлического титана. TiCl4+Mg=Ti+MgCl2 Газообразный хлор в виде анодного газа магниевых электролизеров и металлический магний, необходимые для получения титана, поступают из магниевого производства, а хлорид магния, получающийся по реакции, вновь возвращается на электролитическое получение магния. Температура восстановления 750-850оС. эта температура значительно ниже температуры плавления титана. По этой причине металл получают в виде спеченных кристаллов – губки.
Восстановительная плавка
Хлорирование
Тетрахлорид титана
МЕТАЛЛУРГИЯ ЛЕКГИХ МЕТАЛЛОВ
МЕТАЛЛУРГИЯ АЛЮМИНИЯ
Свойства алюминия Впервые получен в 1825 году датским физиком Эрстедом. Находится в III группе 3-го периода. Порядковый номер 13. Молекулярная масса 26,98 г/моль. Температура плавления 660оС. Температура кипения 2500оС. Алюминий обладает малой плотностью, высокой пластичностью, электро-и теплопроводностью. Многие физические свойства алюминия изменяются в зависимости от его чистоты. Чем чище алюминий, тем выше его температура плавления и электропроводность, и ниже плотность. Алюминий обладает высокой химической активностью по отношению к кислороду, сере, углероду и галоидам. В ряду напряжений алюминий занимает место среди электроотрицательных элементов, что делает невозможным его электрохимическое выделение из водных растворов его солей. Взаимодействие алюминия с кислородом воздуха приводит к образованию на его поверхности тонкой, но очень прочной пленки, которая придает алюминию коррозионную стойкость. Вследствие высокого сродства к кислороду алюминий восстанавливает оксиды многих металлов до металлического состояния. При нагреве алюминий легко растворяется в разбавленных азотной и серной кислотах, холодная азотная кислота его пассивирует. Алюминий хорошо растворяется в щелочах с образованием алюминатов. В органических кислотах и воде он устойчив. Применение: электрические провода, химическая аппаратура, фольга, электроконденсаторы, отражательные стекла в телескопах, атомная энергетика, радиотехника, производство стали и сплавов.
|
|||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-07-19; просмотров: 61; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.84.29 (0.043 с.) |
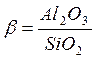

 Безводный карналлит
Безводный карналлит

 Электролиз
Электролиз

 Титановый шлак Чугун
Титановый шлак Чугун
 Ректификация
Ректификация


