Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Переваривание нуклеопротеинов в желудочно-кишечном тракте. Конечные продукты распада пиримидиновых и пуриновых нуклеотидов. Гиперурикемия, подагра, подходы к диагностике, профилактике и лечениюСтр 1 из 6Следующая ⇒
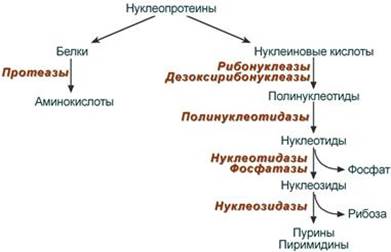
Переваривание нуклеопротеинов в желудочно-кишечном тракте. Конечные продукты распада пиримидиновых и пуриновых нуклеотидов. Гиперурикемия, подагра, подходы к диагностике, профилактике и лечению Нуклеотиды поступают в организм с пищей, главным образом в составе нуклеопротеинов. После воздействия соляной кислоты и протеолитических ферментов желудка нуклеопротеины распадаются до нуклеиновых кислот и белковой части. Белки перевариваются обычным образом, нуклеиновые кислоты – с помощью дополнительных ферментов. Панкреатический сок содержит рибонуклеазы и дезоксирибонуклеазы, гидролизующие все нуклеиновые кислоты до полинуклеотидов.
После действия панкреатических ферментов полинуклеотидазы (фосфодиэстеразы) кишечника гидролизуют нуклеиновые кислоты до мононуклеотидов. Далее, под действием нуклеотидаз и фосфатаз происходит гидролиз нуклеотидов до нуклеозидов, которые либо всасываются, либо под действием нуклеозидаз слизистой кишечника деградируют до пуриновых и пиримидиновых оснований. В просвете кишечника пуриновые основания могут подвергаться окислению до мочевой кислоты, которая всасывается и затем выделяется с мочой. Большая часть тех пуринов, что всосались, в энтероцитах также окисляется в мочевую кислоту, при этом не происходит их перехода в кровь, в другие клетки и включения во вновь образующиеся молекулы нуклеотидов и нуклеиновых кислот. Свободные пиримидиновые основания, подобно пуринам, в основном катаболизируют и выделяются без их использования в организме. N.B. Таким образом, полинуклеотиды и, тем более, нуклеиновые кислоты пищевых продуктов не поступают из кишечника в кровоток, не выступают в роли поставщика предшественников ДНК и РНК клеток организма. И хотя млекопитающие потребляют значительные количества нуклеиновых кислот и нуклеотидов, их жизнедеятельность не зависит от всасывания этих веществ или соответствующих продуктов распада. --- Применение ферментов и их ингибиторов в медицинской практике Энзимодиагностика Энзимодиагностика – это исследование активности ферментов плазмы крови, мочи, слюны с целью диагностики тех или иных заболеваний (подробнее). В основе энзимодиагностики лежат два факта:
Заболевание органа приводит к понижению синтеза ферментов в клетках. Если некоторые ферменты секретируются клетками наружу, то их активность в биологической жидкости снижается. Примером является снижение активности белков гемостаза, церулоплазмина и псевдохолинэстеразы в крови при заболеваниях печени. При воспалении или некрозе в ткани происходит разрушение клеток, в результате чего внутриклеточные ферменты (органоспецифичные) оказываются в плазме крови или в моче, их активность в сыворотке крови повышается. Примером для второго случая может служить фермент лактатдегидрогеназа, определение его активности в сыворотке крови необходимо при заболеваниях сердца, печени, скелетной мускулатуры. Увеличение активности α-амилазы в плазме крови и моче наблюдается при воспалительных процессах в поджелудочной и слюнных железах. В то же время заболевания тех или иных органов всегда сопровождаются специфичным "ферментативным профилем". Например, инфаркт миокарда сопровождается увеличением активности лактатдегидрогеназы, креатинкиназы, аспартатаминотрансферазы. Энзимотерапия Энзимотерапия – это использование ферментов в качестве лекарственных средств. Самыми распространенными ферментативными препаратами являются многочисленные комплексы ферментов (Ацидин-пепсин, Фестал, Энзистал, Панкреатин, Мезим форте, Воб-энзим, Креон и т.п.), отличающиеся по источнику ферментов (животная или растительная основа) и содержащие пепсин, трипсин, амилазу, лактазу и т.п., и используемые для заместительной терапии при нарушениях переваривания веществ в желудочно-кишечном тракте. Тканевой фермент гиалуронидаза нужна организму для обратимого изменения проницаемости межклеточного вещества, в основе которого находится гиалуроновая кислота. Лекарственную форму гиалуронидазы – лидазу – вводят для размягчения рубцов, появления подвижности в суставах, рассасывания гематом. Коллагеназу применяют для ускорения отторжения некротизированных тканей, для очистки трофических язв. Цитохром с – белок, участвующий в процессах тканевого дыхания. Его применяют при асфиксии новорожденных, при гипоксии тканей – астматические состояния, сердечная недостаточность, нарушения мозгового и периферического кровообращения и т.п.
Рибонуклеаза и дезоксирибонуклеаза входят в состав глазных капель для лечения вирусных конъюнктивитов, также при нанесении на рану они разжижают гной, при ингаляциях уменьшают вязкость слизи, деполимеризуя нуклеиновые кислоты в мокроте. Стрептокиназа и урокиназа используются как активаторы фибринолиза при тромбозах. Трипсин ингалируют при бронхолегочных заболеваниях для разжижения густой и вязкой мокроты. Фицин используется в фармацевтической промышленности в качестве добавки к зубным пастам для удаления зубного налета. Углеводный обмен В гепатоцитах активно протекают процессы углеводного обмена. Благодаря синтезу и распаду гликогена печень поддерживает концентрацию глюкозы в крови. Активный синтез гликогена происходит после приема пищи, когда концентрация глюкозы в крови воротной вены достигает 20 ммоль/л. Запасы гликогена в печени составляют от 30 до 100 г. При кратковременном голодании происходит гликогенолиз, в случае длительного голодания основным источником глюкозы крови является глюконеогенез из аминокислот и глицерина. Печень осуществляет взаимопревращение сахаров, т.е. превращение гексоз (фруктозы, галактозы) в глюкозу. Активные реакции пентозофосфатного пути обеспечивают наработку НАДФН, необходимого для микросомального окисления и синтеза жирных кислот и холестерола из глюкозы. Липидный обмен Если во время приема пищи в печень поступает избыток глюкозы, который не используется для синтеза гликогена и других синтезов, то она превращается в липиды – холестерол и триацилглицеролы. Поскольку запасать ТАГ печень не может, то их удаление происходит при помощи липопротеинов очень низкой плотности (ЛПОНП). Холестерол используется, в первую очередь, для синтеза желчных кислот, также он включается в состав липопротеинов низкой плотности (ЛПНП) и ЛПОНП. При определенных условиях – голодание, длительная мышечная нагрузка, сахарный диабет I типа, богатая жирами диета – в печени активируется синтез кетоновых тел, используемых большинством тканей как альтернативный источник энергии. Белковый обмен Больше половины синтезируемого за сутки в организме белка приходится на печень. Скорость обновления всех белков печени составляет 7 суток, тогда как в других органах эта величина соответствует 17 суткам и более. К ним относятся не только белки собственно гепатоцитов, но и идущие на "экспорт", составляющие понятие "белки крови" – альбумины, многие глобулины, ферменты крови, а также фибриноген и факторы свертывания крови. Аминокислоты подвергаются катаболическим реакциям с трансаминированием и дезаминированием, декарбоксилированию с образованием биогенных аминов. Происходят реакции синтеза холина и креатина благодаря переносу метильной группы от аденозилметионина. В печени идет утилизация избыточного азота и включение его в состав мочевины. Реакции синтеза мочевины теснейшим образом связаны с циклом трикарбоновых кислот.
Пигментный обмен Участие печени в пигментном обмене заключается в превращении гидрофобного билирубина в гидрофильную форму (прямой билирубин) и секреция его в желчь.
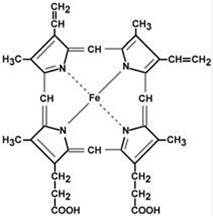
К пигментному обмену можно отнести и обмен железа, поскольку железо входит в состав многочисленных гемопротеинов по всему организму. В гепатоцитах находится белок ферритин, играющий роль депо железа, и синтезируется гепсидин, регулирующий всасывание железа в ЖКТ. --- Строение и синтез гема Гем – структура, включающая в себя порфириновое кольцо (состоящее из 4 пиррольных колец) и иона Fe2+. Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
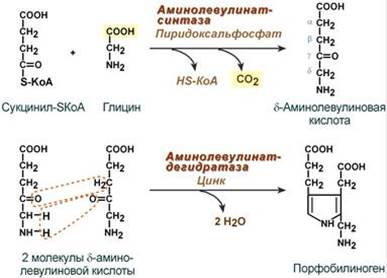
Синтез гема в основном идет в предшественниках эритроцитов, в клетках печени, почек, слизистой кишечника и в остальных тканях. Первая реакция синтеза с участием δ-аминолевулинат-синтазы (греч. δ - "дельта") происходит в митохондриях. Следующая реакция при участии аминолевулинатдегидратазы (порфобилиноген-синтазы) протекает в цитозоле, здесь из двух молекул δ‑аминолевулиновой кислоты образуется циклический порфобилиноген (монопиррол).
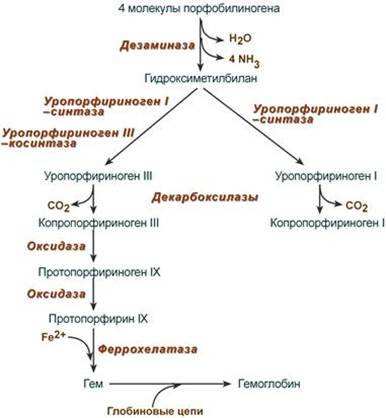
После синтеза порфобилиногена четыре его молекулы конденсируются в гидроксиметилбилан, который далее превращается в уропорфириноген типа I и уропорфириноген типа III. В синтезе обоих видов порфиринов принимает участие уропорфириноген I-синтаза, в образовании уропорфириногена III дополнительно принимает участие фермент уропорфириноген III-косинтаза. Судьба обоих типов уропорфириногена двояка: они могут окисляться до уропорфирина (на рисунке не показано) или декарбоксилироваться до копропорфириногена соответствующего типа.
Копропорфириноген III возвращается в митохондрии и окисляется в протопорфириноген IX и далее в протопорфирин IX. Последний после связывания с железом образует гем, реакцию катализирует феррохелатаза (гемсинтаза). Скорость синтеза глобиновых цепей зависит от наличия гема, он ускоряет биосинтез "своих" белков. Основная часть желчных пигментов образуется при распаде гема и гемоглобина в клетках ретикулоэндотелиальной системы (РЭС) и представляет собой многоступенчатый процесс: при окислении гемоглобина образуется вердоглобин; после отщепления глобина и железа образуется биливердин, который далее восстанавливается до билирубина. Билирубин — желто-красный пигмент, представляющий собой линейный тетрапиррол, токсичное, жирорастворимое вещество, способное нарушать окислительное фосфорилирование в клетках, в первую очередь в нервной ткани. В крови билирубин либо находится в свободном состоянии, либо в комплексе с альбумином (частично в виде альбумин-фосфатидного комплекса), в меньшем количестве — в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами. Образование таких комплексов предотвращает выделение билирубина с мочой. Такая форма билирубина называется свободной (неконъюгированной, несвязанной, непрямой). Она не дает прямой реакции с диазореактивом Эрлиха.
Из сосудистого русла в гепатоциты билирубин попадает с помощью белка-переносчика (лигандина). В печени, при участии фермента УДФ‑глюкуронилтрансферазы, происходит реакция этерификации — взаимодействие OH‑группы глюкуроновой кислоты с карбоксильными группами билирубина и образование конъюгированного (связанного, прямого) билирубина, представляющего собой парное соединение с одним или двумя остатками глюкуроновой кислоты (моно- или диглюкуронид). Кроме глюкуроновой кислоты в реакцию могут вступать сульфаты, фосфаты, глюкозиды. В норме конъюгированный билирубин активно секретируется в желчные капилляры, где при участии β‑глюкуронидазы, вновь превращается в свободный билирубин и с током желчи попадает в тонкий кишечник. Здесь ферментами бактериальной флоры он восстанавливается до мезобилирубина и мезобилиногена (уробилиногена). Часть последних всасывается и с током крови вновь попадает в печень, где окисляется до ди‑ и трипирролов. При этом в здоровом организме в общий круг кровообращения и в мочу мезобилирубин и уробилиноген не попадают, а полностью задерживаются гепатоцитами. Невсосавшаяся часть пигментов ферментами бактериальной флоры толстого кишечника восстанавливается до стеркобилиногена и выделяется из организма, окрашивая кал. Незначительное количество стеркобилиногена через геморроидальные вены попадает в большой круг кровообращения, отсюда –– в почки и выделяется с мочой. На воздухе стеркобилиноген и уробилиноген превращаются, соответственно, в стеркобилин и уробилин. --- Соляная кислота Одним из важнейших компонентов желудочного сока является соляная кислота. В образовании соляной кислоты принимают участие париетальные (обкладочные) клетки желудка, секретирующие ионы Н+. Источником ионов Н+ является угольная кислота, образуемая ферментом карбоангидразой. При ее диссоциациии, кроме ионов водорода, образуются карбонат-ионы НСО3–. Они по градиенту концентрации движутся в кровь в обмен на ионы Сl–. В полость желудка ионы Н+ попадают энергозависимым антипортом с ионами К+ (Н+,К+-АТФаза), хлорид-ионы перекачиваются в просвет желудка также с затратой энергии. Функции соляной кислоты: - Денатурация белков пищи. - Бактерицидное действие. - Высвобождение железа из комплекса с белками, что необходимо для его всасывания. Аналогично высвобождаются и другие металлы. - Высвобождение различных органических молекул, прочно связанных с белковой частью (гем, коферменты - тиаминдифосфат, ФАД, ФМН, пиридоксальфосфат, кобаламин, биотин), что позволяет витаминам впоследствии всасываться.
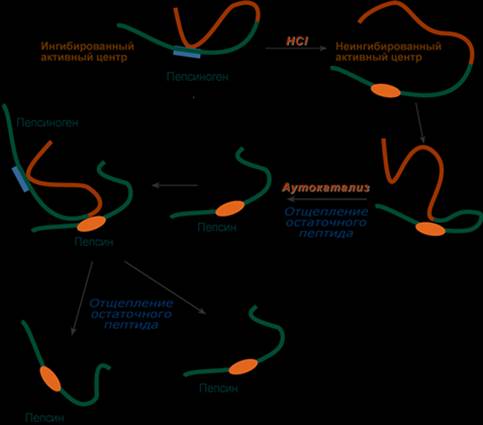
- Превращение неактивного пепсиногена в активный пепсин. - Снижение рН желудочного содержимого до 1,5-2,5 и создание оптимума рН для работы пепсина. - После перехода в 12-перстную кишку – стимуляция секреции кишечных гормонов и, следовательно, выделения панкреатического сока и желчи. Пепсин Пепсин является эндопептидазой, то есть он расщепляет внутренние пептидные связи в молекулах белков и пептидов. Синтезируется в главных клетках желудка в виде неактивного профермента пепсиногена, в котором активный центр "прикрыт" N-концевым фрагментом. При наличии соляной кислоты конформация пепсиногена изменяется таким образом, что "раскрывается" активный центр фермента, который отщепляет остаточный пептид (N-концевой фрагмент), т.е. происходит аутокатализ. В результате образуется активный пепсин, активирующий и другие молекулы пепсиногена.
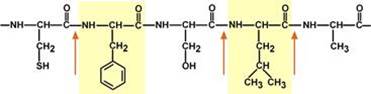
Пепсин обладает невысокой специфичностью, в основном он гидролизует пептидные связи, образованные аминогруппами ароматических аминокислот (тирозина, фенилаланина, триптофана), меньше и медленнее – аминогруппами и карбоксигруппами лейцина, глутаминовой кислоты и т.д. Оптимум рН для работы пепсина 1,5-2,0.
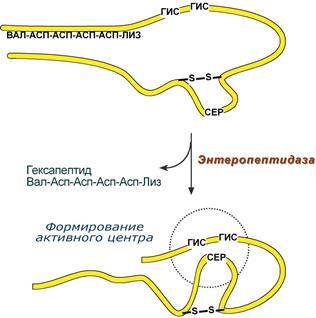
Гастриксин Гастриксин по своим функциям близок к пепсину, его количество в желудочном соке составляет 20-50% от количества пепсина. Синтезируется главными клетками желудка в виде прогастриксина (профермент) и активируется соляной кислотой. Оптимум рН гастриксина соответствует 3,2-3,5 и значение этот фермент имеет при питании молочно-растительной пищей, слабее стимулирующей выделение соляной кислоты и одновременно нейтрализующей ее в просвете желудка. Гастриксин является эндопептидазой и гидролизует связи, образованные карбоксильными группами дикарбоновых аминокислот. --- 10. Сок поджелудочной железы. Участие в переваривании углеводов и липидов. Принципы и клиническое значение определения активности амилазы в моче. Сок поджелудочной железы содержит проферменты – трипсиноген, химотрипсиноген, прокарбоксипептидазы, проэластазу. Проферменты в просвете кишечника активируются, соответственно, до трипсина, химотрипсина, карбоксипептидаз и эластазы способом ограниченного протеолиза. Указанные ферменты осуществляют основную работу по перевариванию белков. В кишечном соке активны ферменты щеточной каймы – дипептидазы и аминопептидазы. Они заканчивают переваривание белков. Трипсин, химотрипсин, эластаза являются эндопептидазами. Карбоксипептидазы и аминопептидазы – экзопептидазы. Трипсин Синтезируемый поджелудочной железой трипсиноген в двенадцатиперстной кишке подвергается частичному протеолизу под действием фермента энтеропептидазы, секретируемой клетками кишечного эпителия. От профермента отделяется гексапептид (Вал-Асп-Асп-Асп-Асп-Лиз), что приводит к формированию активного центра трипсина. Трипсин специфичен к пептидным связям, образованным с участием карбоксильных групп лизина и аргинина, может осуществлять аутокатализ, т.е. превращение последующих молекул трипсиногена в трипсин, также он активирует остальные протеолитические ферменты панкреатического сока – химотрипсиноген, проэластазу, прокарбоксипептидазу. Параллельно трипсин участвует в переваривании пищевых липидов, активируя фермент переваривания фосфолипидов – фосфолипазу А2, и колипазу панкреатической липазы, отвечающей за гидролиз триацилглицеролов.
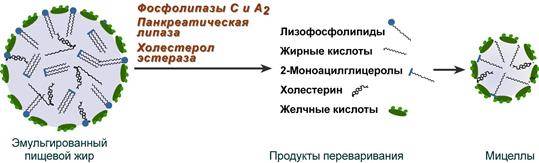
Химотрипсин Образуется из химотрипсиногена при участии трипсина, который расщепляет пептидную связь между аргинином-15 и изолейцином-16 с образованием уже активных промежуточных форм π-химотрипсина и δ-химотрипсина, которые аутолизисом удаляют два дипептида из собственных цепей. Три образованных фрагмента удерживаются друг с другом посредством дисульфидных связей, формируя стабильный α-химотрипсин. Фермент специфичен к пептидным связям, образованных с участием карбоксильных групп ароматических аминокислот – фенилаланина, тирозина и триптофана. Эластаза Активируется в просвете кишечника трипсином из проэластазы. Гидролизует связи, образованные карбоксильными группами малых аминокислот – аланина, пролина, глицина. Карбоксипептидазы Карбоксипептидазы являются экзопептидазами, они гидролизуют пептидные связи с С-конца пептидной цепи. Различают два типа карбоксипептидаз – карбоксипептидазы А и карбоксипептидазы В. Карбоксипептидазы А отщепляют с С-конца остатки алифатических и ароматических аминокислот, карбоксипептидазы В – остатки основных аминокислот – лизина и аргинина. Аминопептидазы Являясь экзопептидазами, аминопептидазы отщепляют N-концевые аминокислоты. Представителями аминопептидаз являются аланин-аминопептидаза и лейцин-аминопептидаза, обладающие широкой специфичностью. Например, лейцин-аминопептидаза отщепляет с N-конца белка не только лейцин, но и ароматические аминокислоты и гистидин. Дипептидазы Дипептидазы гидролизуют дипептиды, в изобилии образующиеся в кишечнике при работе других ферментов. --- Этапы переваривания липидов пищи в желудочно-кишечном тракте. Роль желчных кислот, ферментов. Печеночно-кишечная рециркуляция желчных кислот. Механизмы всасывания продуктов ферментативного гидролиза жира. Образование мицелл В результате воздействия на эмульгированные жиры ферментов панкреатического и кишечного соков образуются 2-моноацилглицеролы, свободные жирные кислоты и свободный холестерол, формирующие структуры мицеллярного типа (размер уже около 5 нм). Свободный глицерол всасывается напрямую в кровь.
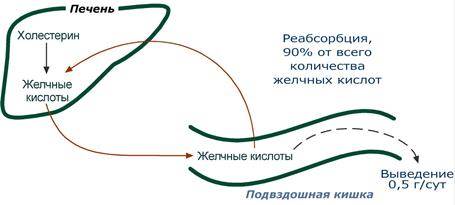
Полученные смешанные мицеллы достигают эпителия кишечника и их компоненты диффундируют в клетки и попадают в гладкую эндоплазматическую сеть. Желчные кислоты почти не всасываются и остаются в просвете кишечника. Далее желчные кислоты достигают подвздошной кишки и всасываются там (Кишечно-печеночная циркуляция). Циркуляция желчных кислот заключается в их непрерывном движении из гепатоцитов в просвет кишечника и реабсорбция большей части желчных кислот в подвздошной кишке, что сберегает ресурсы холестерола. В сутки происходит 6-10 таких циклов. Таким образом, небольшое количество желчных кислот (всего 3-5 г) обеспечивает переваривание липидов, поступающих в течение суток. Потери в размере около 0,5 г/сут соответствуют суточному синтезу холестерола de novo.
---
Переваривание нуклеопротеинов в желудочно-кишечном тракте. Конечные продукты распада пиримидиновых и пуриновых нуклеотидов. Гиперурикемия, подагра, подходы к диагностике, профилактике и лечению Нуклеотиды поступают в организм с пищей, главным образом в составе нуклеопротеинов. После воздействия соляной кислоты и протеолитических ферментов желудка нуклеопротеины распадаются до нуклеиновых кислот и белковой части. Белки перевариваются обычным образом, нуклеиновые кислоты – с помощью дополнительных ферментов. Панкреатический сок содержит рибонуклеазы и дезоксирибонуклеазы, гидролизующие все нуклеиновые кислоты до полинуклеотидов.
После действия панкреатических ферментов полинуклеотидазы (фосфодиэстеразы) кишечника гидролизуют нуклеиновые кислоты до мононуклеотидов. Далее, под действием нуклеотидаз и фосфатаз происходит гидролиз нуклеотидов до нуклеозидов, которые либо всасываются, либо под действием нуклеозидаз слизистой кишечника деградируют до пуриновых и пиримидиновых оснований. В просвете кишечника пуриновые основания могут подвергаться окислению до мочевой кислоты, которая всасывается и затем выделяется с мочой. Большая часть тех пуринов, что всосались, в энтероцитах также окисляется в мочевую кислоту, при этом не происходит их перехода в кровь, в другие клетки и включения во вновь образующиеся молекулы нуклеотидов и нуклеиновых кислот. Свободные пиримидиновые основания, подобно пуринам, в основном катаболизируют и выделяются без их использования в организме. N.B. Таким образом, полинуклеотиды и, тем более, нуклеиновые кислоты пищевых продуктов не поступают из кишечника в кровоток, не выступают в роли поставщика предшественников ДНК и РНК клеток организма. И хотя млекопитающие потребляют значительные количества нуклеиновых кислот и нуклеотидов, их жизнедеятельность не зависит от всасывания этих веществ или соответствующих продуктов распада. ---
|
|||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 359; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.227.194 (0.061 с.) |