Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Глава II . Объекты исследования
Образование продуктов деградации в аминовых растворах Расход аминов – один из важных показателей работы установок очистки газов, поскольку стоимость абсорбентов высока и затраты на абсорбент составляют существенную часть эксплуатационных затрат. Основные составляющие потерь аминов на установках: унос с газом, термохимическая деструкция аминов, механические потери [45, 46]. Унос с газом. Общий унос амина с газом определяется уносом в паровой фазе и в капельном виде. Величина первого определяется давлением паров амина над водными растворами и зависит от температуры, типа и концентрации амина в растворе. Хотя давление паров аминов относительно невелико, потери их из-за испарения значительны, вследствие больших объемов очищаемого газа. Потери амина за счет уноса в капельном состоянии зависятот нагрузок по газу и раствору, от эффективности работы сепарирующих устройств на газовых потоках, от вида применяемых контактных элементов в колонных аппаратах. Капельный унос резко возрастает при вспенивании поглотительного раствора. Эта величина потерь амина при нормальной работе заводских установок составляет 20-30 мг/м³ газа и возрастает до 100 мг/м³ при вспенивании раствора. Термическое разложение аминов без углекислоты протекает в малой степени и усиливается с повышением температуры и степени насыщения аминов СО2. Потери ДЭА под действием СО2 незначительны при температуре 100ºС и давлении 1,2 МПа и достигают более 90% при температуре 175ºС и давлении 4,1 МПа. Насыщенный СО2 водный 20%-ый раствор ДЭА в течении 8 ч при давлении 1,7 МПа и температуре 125ºС разлагается на 22%. При нагревании раствора ДЭА без СО2 в атмосфере азота в течение 8 ч при давлении 4,1 МПа и температуре 205ºС не наблюдается значительных изменений концентрации ДЭА или образования продуктов деструкции амина [47, 48]. Механизм взаимодействия СО2 с аминами с образованием побочных нерегенерируемых или труднорегенерируемых соединений изучен не полностью. Считают [39], что на первой стадии карбонаты или карбаматы, образовавшиеся в результате взаимодействия СО2 с аминами, превращаются в оксазолидон-2, который затем образует оксиэтилимидазолидон-2. Замещенный имидазолидон гидролизуется до оксиэтилэтилен-диамина. В растворах ДЭА оксазолидон при повышенных температурах может превратиться в другое термически стойкое соединение – оксиэтилпиперазин. Оксазолидон-2 может образовываться и при обычных температурах, если в газе имеется сероокись углерода. В растворах амина были обнаружены и другие содержащие азот и имеющие сложную структуру не идентифицированные продукты разложения.
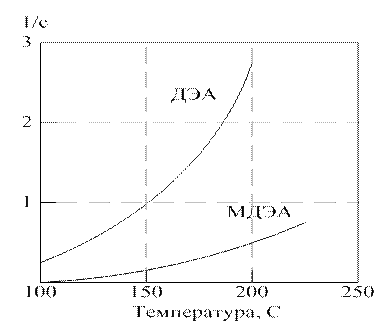
Скорости побочных реакций обычно низки. Однако при длительной циркуляции поглотительного раствора происходит накопление труднорегенерируемых продуктов в системе. Это приводит к снижению концентрации активного амина, повышению вязкости раствора и в целом к уменьшению эффективности процесса абсорбции. Кроме того, наличие продуктов деградации аминов вызывает вспенивание и усиливает коррозионную агрессивность раствора. Установлено [48], что продукты превращения ДЭА несколько тормозят реакции его разложения; сероводород тормозит деструкцию ДЭА под воздействием СО2. Сложность происходящихв растворе процессов деструкции аминов и отсутствие в литературе представительных данных по кинетике и механизму побочных реакций СО2 с ДЭА и МДЭА затрудняют количественную оценку этой статьи потерь аминов. В связи с этим в работе [49] было проведено экспериментальное исследование термохимической деструкции ДЭА и МДЭА под действием СО2 в автоклавах при температуре до 250ºС и парциальном давлении СО2 до 5 МПа. Было установлено, что процесс деградации аминов подчиняется кинетическому уравнению первого порядка: d [ A ]/ dτ =- K [ A ]. (2.1.1) Зависимость константы K от скорости деструкции аминов под действием СО2 от температуры приведена на рисунке 2.1.1. Представленные данные свидетельствуют о значительно более высокой термохимической стабильности МДЭА по сравнению с ДЭА, причем это различие с ростом температуры проявляется все сильнее. Рисунок 2.1.1. Зависимость константы скорости процесса термохимической деструкции аканоламинов от температуры при pСО2 > 0,1 МПА.
Экспериментальные данные по зависимости константы скорости процесса деструкции аминов (К, моль/(л*ч) от парциального давления СО2 (рСО2 , МПа) и температуры (ºС) описываются следующими критериальными уравнениями:
Для МДЭА при рСО2 > 4 МПа: К = -0,0846+0,169*ln рСО2 (2.1.2) t = 185ºC;
К = exp(-15.1335+0.0749* t), (2.1.3) 100ºС < t < 165ºС; К = -0,8505+5,5*10-3-3 t, (2.1.4) 165ºС < t < 205ºC. Для МДЭА (при рСО2 > 2 МПа): К = exp (-12.05+0.03856* t) (2.1.5) По уравнениям (2.1.2-2.1.5) можно рассчитать примерный расход аминов с учетом технологических режимов работы установок сероочистки газа и состава перерабатываемого сырья. Следует отметить, что в промышленных условиях наибольшую деструкцию амина следует ожидать в зонах с повышенной температурой и степенью насыщения СО2. Такой зоной, по-видимому, является линия насыщенного раствора в интервале температур 80-110ºС. В производственном цикле очистки газа водные растворы ЭА постояноо испытывают термическое воздействие и в процессе абсорбции, и особенно десорбции, где температура достигает 120-130 оС. В этих условиях даже химически стабильные ЭА подвергаются побочным превращениям, в частности, окислению под воздействием кислорода. Кислород обычно присутствует в небольшом количестве и в воде, идущей на приготовление раствора ЭА, и в очищаемом природном газе [42]. В промышленных растворах ДЭА и МДЭА установлено наличие до 1,3% масс. щавелевой, уксусной и муравьиной кислот в виде их солей с ЭА [45]. Последние, термостабильные соли, не регенерируются, снимают концентрацию ЭА и вызывают коррозию. H2S обратимо реагирует с этаноламином, но в присутствии кислорода реакция идет с побочным получением тиосульфата (ЭА)2∙S2O3, не разлагающегося при десорбции кислых газов из растворов ЭА [45]. Известны [25] совместные окислительные первращения ЭА, тиолов, моно- и диалкилсульфидов, тиофенов, приводящие к образованию микропримесей тиомочевины, тиосульфатов ЭА и других солей тиосерной кислоты. COS и CS2 также частично по необратимым реакциям взаимодействуют с ЭА, особенно с первичным МЭА, давая соли N-(гидроксиэтил)-тиокарбаминовой и N-(гидроксиэтил)-дитиокарбаминовой кислот [48]. Установлено [51], что под влиянием COS (парциальное давление 0,3-1,17 МПа) и нагревании (t=120-180 оС) развивается деградация растворов ДЭА с образованием производных этилендиамина, имидазолидона и пиперазина, а также других соединений. При нагревании (t=180 оС, τ=144 ч.) водного раствора, содержащего 4,28 моль/л МДЭА, в нем обнаружены 2-(диметиламино)-этанол, 1,4-диметилпиперазин, N-(гидроксиэтил)-метилпиперазин, N,N'-бис-(гидроксиэтил)-пиперазин, ТЭА, триметиламин, этиленгликоль, оксид этилена и метанол [51]. Константа скорости деструкции МДЭА меньше, чем ДЭА, примерно в 10 раз. Изучение превращений смесей МДЭА+ДЭА и МДЭА+МЭА под действием CO2 (парциальное давление ~2,6 МПа) при t=120-180 оС [52] показало, что скорость образования побочных продуктов увеличивается в ряду МДЭА<МЭА<ДЭА согласно кинетическим уравнениям (2.1.6 – 2.1.8): ln kМДЭА = 20,34 – 96,420/RT (2.1.6) ln kМЭА = 19,36 – 85,476/RT (2.1.7) ln kДЭА = 12.60 – 58.212/RT (2.1.8) Соответственно, уменьшается энергия активации (Ea) протекающих с CO2 реакций. В таблице 2.1.1 указаны основные изученные продукты деградации аминовых растворов. Таблица 2.1.1.
|
||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 156; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.111.125 (0.006 с.) |