Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Масса молекул. Количество веществаСодержание книги
Поиск на нашем сайте Единица количества вещества называется молем (моль). Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 12 г вещества углерода. Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул). Это число называется постоянной Авогадро NА: NА = 6,02·1023 моль–1. Постоянная Авогадро – одна из важнейших постоянных в молекулярно-кинетической теории. Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NА: ν = N/ NА Массу одного моля вещества принято называть молярной массой M. Молярная масса выражается в килограммах на моль (г/моль). Для веществ, молекулы которых состоят из одного атома, часто используется термин атомная масса. За единицу массы атомов и молекул принимается 1/12 массы атома углерода 12C Она называется атомной единицей массы (а. е. м.): 1 а. е. м. = 1,66·10–27 кг. Относительная атомная масса – безразмерная величина, равная отношению средней массы атома элемента к 1 а.е.м. Аr = m(атома)/1 а.е.м. Значения относительных атомных масс указаны в таблице Д.М.Менделеева. Относительная молекулярная масса – безразмерная величина, находится как сумма относительных атомных масс элементов, входящих в состав молекул. Мr(H2SO4) = 1·2 + 32 = 16·4 = 98 Относительная молекулярная масса численно совпадает с относительной молекулярной. Мr(H2SO4) = М(H2SO4) = 98 г/моль Абсолютная масса молекулы – равна произведению молярной массы, умноженной на количество моль вещества: m = M · ν
Задачи 1. Определите относительную молекулярную массу веществ, молекулярные формулы которых: N2O5 , K2CO3, Zn(NO3)2, CaCO3 М r(N2O5) = 14 · 2 + 16 · 5 = 108 М r(K2CO3) = 39 · 2 + 12 = 16 · 3 = 138 М r(Zn(NO3)2 = 65 + (14 + 16 · 3) · 2 = 189 Мr(CaCO3) = 40 + 12 + 12·3 = 100
2. Заполнить таблицу, определив неизвестные величины: ν (1/моль) Число частиц, N О2 32 32·4 = 128 4 4·6,02·1023 = 24·1023 SO2 64 32 32/64 = 0,5 0,5·6,02·1023 = 3·6,02·1023 NH3 17 17·2 = 34 2 12·1023
3. Плотность воздуха при нормальных условиях (t0 = 00 C и атмосферном давлении Р0 = 101325 Па.) равна 1,29 кг/м3. Найдите среднюю молярную массу воздуха. Решение: Уравнение состояния идеального газа: РV = (m\M)· R T Отсюда находим молярную массу: М = mRTo = V Р0 = ρ0 R Т0 / Р0 = 1,29·8,31·273/101325 = 0,029 кг/моль
Электростатика. Электрический заряд. Элементарные частицы
Тела могут взаимодействовать между собой силами различной природы: гравитационными, электромагнитными, сильными (ядерными) и слабыми (взаимодействия, обусловленные процессами с участием нейтрино). Электромагнитные взаимодействия занимают первое место по широте и по разнообразию проявлений. Электродинамика – это наука о свойствах и закономерностях поведения особого вида материи – электромагнитного поля, осуществляющего взаимодействие между электрически заряженными телами или частицами. Раздел электродинамики, посвященный изучению покоящихся электрически заряженных тел, называют электростатикой.
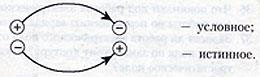
Электрический заряд Все тела простроены из мельчайших частиц, которые неделимы на более простые и поэтому называются элементарными. Все элементарные частицы имеют массу и поэтому притягиваются друг к другу согласно закону Всемирного тяготения. С увеличением расстояния между частицами сила тяготения убывает обратно пропорционально квадрату расстояния между ними. Большинство элементарных частиц, кроме того, обладают способностью взаимодействовать друг с другом силой, которая также убывает обратно пропорционально квадрату расстояния, но эта сила в огромное число раз превосходит силу тяготения. Если частицы взаимодействуют друг с другом силами, которые убывают с увеличением расстояния также, как и силы всемирного тяготения, но превышают силы тяготения во много раз, то говорят, что эти частицы имеют электрический заряд. Сами Частицы называют заряженными. Бывают частицы без заряда, но не бывает заряда без частицы. Взаимодействия между заряженными частицами носят название электромагнитных. Электрический заряд определяет интенсивность электромагнитных взаимодействий, подобно тому, как масса определяет интенсивность гравитационных взаимодействий. Заряженные частицы могут притягиваться и отталкиваться друг от друга. Это объясняется тем, что в природе есть частицы с электрическими зарядами противоположных знаков; при зарядах одинаковых знаков частицы отталкиваются; а при разных – притягиваются. Заряд элементарных частиц – протонов, входящих в состав атомных ядер, называют положительным, а заряд электронов – отрицательным. Между положительными и отрицательными зарядами внутренних различий нет. Кроме электронов и протонов, есть еще несколько типов заряженных элементарных частиц. Но только электроны и протоны могут неограниченно долго существовать в свободном состоянии. Остальные же заряженные частицы живут менее миллионных долей секунды. Они рождаются при столкновениях быстрых элементарных частиц и, просуществовав ничтожно мало, распадаются, превращаясь в другие частицы. К частицам, не имеющим электрического заряда, относится нейтрон. Он также, как и протон входит в состав атомного ядра.
Закон Кулона Открытие взаимодействия неподвижных друг относительно друга электрических зарядов было сделано под влиянием идей Ньютона и, в частности, его законов всемирного тяготения. В середине 18 века уже высказывались предположения, что закон взаимодействия зарядов аналогичен закону всемирного тяготения. Первым доказал это экспериментально англичанин Кевендиш. Но этот выдающийся ученый отличался странностями. Своих работ по электричеству Кевендиш не печатал. Более ста лет рукописи пролежали в библиотеке Кембриджского университета, пока их не извлек Максвелл и не опубликовал. К этому времени закон взаимодействия зарядов был установлен во Франции Шарлем Кулоном и с тех пор носит его имя. Его открытие было сделано в 1785 году. Опыты Кулона привели к открытию закона, поразительно напоминающего закон тяготения. Сила взаимодействия неподвижных заряженных тел прямо пропорциональна произведению их зарядов и обратно пропорциональна квадрату расстояния между ними.
| g1| · | g2| F = k R2
k – коэффициент пропорциональности, численно равный силе взаимодействия единичных зарядов на расстоянии равном единицы длины. Его значение зависит от выбора системы единиц. В системе СИ его значение равно - 9·109 Н·м2/Кл2 | g1| и | g2| - модули зарядов двух частиц. R – расстояние между частицами. Силы взаимодействия двух неподвижных тел направлены вдоль прямой, соединяющей эти тела. Единицей заряд является Кулон. Один кулон (1 Кл) – это заряд, проходящий за 1 секунду через поперченное сечение проводника при силе ток 1 Ампер. Коэффициент k в законе Кулона при записи его в единицах СИ выражается в Н·м2/Кл2 Минимальный заряд, существующий в природе, - это заряд элементарных частиц. В единицах СИ модуль этого заряда равен: е = 1,6·10-19 Кл.
Задачи 1. Сколько электронов содержится в капле воды массой 0,6 г? Масса молекулы воды - 3·10-23 г. Дано: m = 0,6 г m0 = 3·10-23 г. H2O Решение: Молекула Н2О содержит 10 электронов, так как молекула состоит из двух атомов водорода, каждый из которых имеет по одному электрону и одного атома кислорода, которых содержит восемь электронов. В капле воды содержится m/ m0 молекул, т.е. m/ m0 = 0,6/3·10-23 = 2·1022 молекул, и следовательно, 2·1022 электронов.
2. Определите, с какой силой взаимодействуют между собой два шарика, если один из них имеет заряд - 2·10-10 Кл, а другой - 4·10-11 Кл, если они находятся на расстоянии 2 м? Решение: F = 9·109 · 2·10-10 · 4·10-11/ 22 = 18·10-12 Н
3. Определите расстояние, на котором находятся два взаимодействующие между собой заряженные шарики, если сила взаимодействия составляет 5 ·10-6 Н, а заряды 5·10-10 Кл и ·10-12 Кл соответственно. Решение: R2 = k·g1 · g1/ F = 9·109 · 5·10-10 · 6·10-12/5·10-6 = 54·10-7 Отсюда находим r = 0,023 м.
4. С какой силой будут взаимодействовать две капли воды на расстоянии 1 м, если бы удалось передать одной из капель 1% всех электронов, содержащихся в другой капле массой 0,6 г?
Решение: Используя данные предыдущей задачи можно сказать, что в одной капле воды массой 0, 6 г содержится 2·1022 электронов. Следовательно, одна капля будет содержать 2·1022 + 2·1022 ·0,01 = 2,02 ·1022 электронов, другая 2·1022 - 2·1022 ·0,01 = 1,98 ·1022 электронов. Взаимодействие между каплями воды будет происходить за счет разницы между количеством электронов в одной и другой капле: 2,02 ·1022 - 1,98 ·1022 = 0,04 ·1022 Сила взаимодействия будет определяться: F = 9·109 · 0,04 ·1022 · 1,6 10-19 /1 = 0,576·1012 Н
Законы постоянного тока. Сила тока. Закон Ома для участка цепи. Сопротивление
Неподвижные электрические заряды редко используются на практике. Для того, чтобы использовать электрические заряды на практике, необходимо привести их в движение – создать электрический ток. Электрический ток - упорядоченное движение заряженных частиц (свободных электронов или ионов). При этом через поперечное сечение проводника переносится электрический заряд (при тепловом движении заряженных частиц суммарный перенесенный электрический заряд = 0, т.к. положительные и отрицательные заряды компенсируются).
Электрический ток имеет определенное направление. За положительное направление тока принимают направление движения положительно заряженных частиц. Если ток образован движением отрицательно заряженных частиц, то направление тока считают противоположным направлению движения частиц.
|
||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 171; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.15 (0.01 с.) |