
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Повышенный уровень сложности. 69. Установите соответствие между тривиальным названием карбоновой кислоты и ее
69. Установите соответствие между тривиальным названием карбоновой кислоты и ее формулой
70. Установите соответствие между систематическим и тривиальным названием органических кислот
71. В состоянии sp3- и sp2-гибридизации атомы углерода находятся в молекулах
72. Установите соответствие между формулой органического вещества и средой его водного раствора.
73. Установите соответствие между названием органического вещества и средой его водного раствора
74. Установите соответствие между названием органического вещества и цветом лакмуса в его водном растворе.
75. И муравьиная, и уксусная кислота взаимодействуют с
76. И муравьиная, и уксусная кислота взаимодействуют с
77. И пропановая, и акриловая кислота могут взаимодействовать с
78. И уксусная, и олеиновая кислота взаимодействуют с
79. Уксусную кислоту можно получить, используя
80. Гидролиз жиров в промышленности используют для получения
81. С раствором гидроксида калия способны взаимодействовать
82. Для метановой кислоты справедливы утверждения
83. Для уксусной кислоты справедливы утверждения
84. В результате каталитического окисления бутана объемом 33,6 л (н.у.) с выходом 80% получили уксусную кислоту, масса которой составила _________ г. (Запишите число с точностью до целых.) 85. При взаимодействии уксусной кислоты массой 30 г с магнием массой 4,8 г выделился водород, объем которого равен _________ л. (Запишите число с точностью до сотых.) 86. Муравьиную кислоту массой 46 г нагрели с метанолом массой 45 г в присутствии концентрированной кислоты. Масса сложного эфира, полученного в результате реакции этерификации, равна _________ г. (Запишите число с точностью до целых.) 87. В результате гидролиза 14,8 г этилформиата с выходом 90% получили муравьиную кислоту, масса которой составила _________ г. (Запишите число с точностью до сотых.)
88. В результате щелочного гидролиза 29,6 г метилацетата получили ацетат натрия, масса которого равна _________ г. (Запишите число с точностью до десятых.) 89. В результате гидролиза этилацетата с выходом 90% получили 3,24 г уксусной кислоты. Масса этилацетата, подвергшегося гидролизу, равна _________ г. (Запишите число с точностью до сотых.) 90. В 150 г воды растворили 50 г 70%-ной уксусной эссенции. Массовая доля уксусной кислоты в полученном растворе равна _________ %. (Запишите число с точностью до десятых.) 91. Какую массу воды надо добавить к 10 г 80%-ной уксусной эссенции для получения 3%-ного раствора? Ответ: _________ г. (Запишите число с точностью до целых.) 92. К 200 г 5%-ного раствора уксусной кислоты добавили 20 г 60%-ного раствора той же кислоты. Массовая доля уксусной кислоты в полученном растворе равна _________ %. (Запишите число с точностью до целых.) Высокий уровень сложности
93. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: СаС2 Укажите условия протекания реакций.
94. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: СО Укажите условия протекания реакций.
95. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: С2Н5СООН Укажите условия протекания реакций.
96. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: C6H12О6 → С2Н5ОН Укажите условия протекания реакций.
97. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: С6H6 → C6H5CH3 → C6H5COOH Укажите условия протекания реакций.
98. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: метилциклогексан → толуол
Укажите условия протекания реакций.
99. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: CH3COOК Укажите условия протекания реакций. 100. (С3) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения: C2H5Cl → C4H10 → CH3COOH
Укажите условия протекания реакций. 101. (С4) К 22,2 г пропионовой кислоты добавили 168 г 5%-ного раствора гидрокарбоната натрия. Определите массовые доли веществ в растворе после окончания реакции.
102. (С4) К 23 г 20%-ного раствора муравьиной кислоты добавили 262,5 г 8%-ного раствора гидрокарбоната натрия. Определите массовые доли веществ в растворе после окончания реакции.
103. (С4) К 12 г уксусной кислоты добавили 180,2 мл 10%-ного раствора гидроксида натрия (плотность 1,11 г/мл). После выпаривания воды сухой остаток прокалили, а затем полученную твердую смесь растворили в 300 мл воды. Определите массовые доли веществ в полученном растворе. 104. (С4) Определите массу муравьиной кислоты, которую следует добавить к 34,97 мл 40%-ного раствора гидроксида натрия (плотность 1,43 г/мл), чтобы массовая доля соли в полученном растворе стала равна 20%. Вычислите массовую долю гидроксида натрия в образовавшемся растворе.
105. (С4) Для полного гидролиза 10,4 г смеси сложных эфиров, состоящей из этилацетата и метилформиата, необходимо затратить 35,6 мл 20%-ного раствора гидроксида калия (плотность 1,18 г/мл). Определите массовые доли сложных эфиров в смеси. 106. (С5) Установите формулу предельной одноосновной карбоновой кислоты, плотность паров по аргону которой равна 1,85.
107. (С5) Установите формулу предельной одноосновной карбоновой кислоты, массовая доля углерода в которой равна 54,55%. 108. (С5) Установите молекулярную формулу предельной одноосновной карбоновой кислоты, массовая доля кислорода в которой в 1,333 раза больше массовой доли углерода.
109.(С5) Для нейтрализации предельной одноосновной карбоновой кислоты массой 13,8 г потребовалось 120 г 10%-ного раствора гидроксида натрия. Определите молекулярную формулу кислоты.
110.(С5) При взаимодействии предельной одноосновной карбоновой кислоты массой 24 г с избытком магния выделилось 4,48 л (н.у.) водорода. Определите молекулярную формулу кислоты.
111. (С5) При полном гидролизе 2,64 г сложного эфира образовалось 1,8 г предельной одноосновной карбоновой кислоты и 1,38 г предельного одноатомного спирта. Установите молекулярную формулу сложного эфира.
112. (С5) Для полного сгорания 3,7 г сложного эфира, образованного предельной одноосновной карбоновой кислотой и предельным одноатомным спиртом, потребовалось 3,92 л (н.у.) кислорода. Установите молекулярную формулу сложного эфира.
113. (С5) При сгорании органического вещества массой 2,16 г получили 3,96 г углекислого газа (н.у.) и 1,08 г воды. Плотность паров вещества по кислороду равна 2,25. Установите молекулярную формулу вещества. С3Н4О2
Углеводы Базовый уровень сложности
1. Состав большинства углеводов может быть выражен формулой
2. Число гидроксильных групп в молекуле фруктозы равно
3. Глюкоза взаимодействует с каждым из двух веществ
4. И глюкоза, и фруктоза взаимодействуют с
5. В результате гидролиза сахарозы образуется (образуются)
6. Крахмал взаимодействует с
7. Конечным продуктом гидролиза целлюлозы является
8. Целлюлоза взаимодействует с каждым из двух веществ
9. И крахмал, и целлюлоза взаимодействуют с
10. И для крахмала, и для целлюлозы справедливо утверждение
11. Аммиачный раствор оксида серебра является реактивом на
12. Раствор глюкозы можно отличить от раствора фруктозы с помощью
13. Какие из приведенных утверждений об углеводах верны? А. Углеводы являются компонентами клеток всех растительных и животных организмов. Б. И крахмал, и целлюлоза обладают высокой питательной ценностью для организма человека.
14. Верны ли следующие суждения о глюкозе? А. Изомером глюкозы является рибоза. Б. Глюкоза подвергается гидролизу.
15. Верны ли следующие суждения о глюкозе? А. Глюкоза является альдегидоспиртом. Б. Продуктом спиртового брожения глюкозы является этанол.
16. Верны ли следующие суждения о глюкозе? А. Глюкоза образуется в процессе фотосинтеза. Б. Продуктом восстановления глюкозы является шестиатомный спирт сорбит.
17. Верны ли следующие суждения о сахарозе? А. Сахароза взаимодействует с гидроксидом меди(II) с образованием раствора ярко-синего цвета. Б. Единственным продуктом гидролиза сахарозы является глюкоза.
18. Верны ли следующие суждения о крахмале? А. Крахмал хорошо растворяется в холодной воде. Б. Конечным продуктом гидролиза крахмала является фруктоза.
19. Верны ли следующие суждения о крахмале? А. Крахмал - дисахарид. Б. Реактивом на крахмал является раствор йода.
20. Верны ли следующие суждения о целлюлозе? А. Макромолекулы целлюлозы имеют разветвленное строение. Б. Целлюлоза вступает в реакцию «серебряного зеркала».
21. Верны ли следующие суждения о целлюлозе? А. Является сырьем для получения искусственных волокон. Б. При взаимодействии с азотной кислотой образует простые эфиры.
22. В схеме превращений C6H12О6 веществом Х является
23. В схеме превращений CО2 веществами Х1 и Х2 соответственно могут быть
24. В соответствии с термохимическим уравнением реакции С6Н12О6(к) + 6О2(г) = 6СО2(г) + 6Н2О(ж) + 2800 кДж количество теплоты, выделяющееся при окислении 36 г глюкозы, равно
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-12; просмотров: 1028; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.23.101.60 (0.094 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
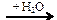 Х1 → CH3COH → CH3COOH
Х1 → CH3COH → CH3COOH 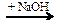 X2 → CH4
X2 → CH4 Х1
Х1 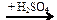 X2 → HCOOCH3 → X2
X2 → HCOOCH3 → X2 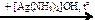 X3
X3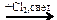 Х1
Х1  X2
X2  Х3
Х3 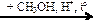 X4
X4 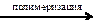 Х5
Х5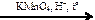 X1
X1 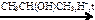 X2 → СН3СООК → С2Н6
X2 → СН3СООК → С2Н6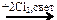 X1 → С6Н5СОН
X1 → С6Н5СОН 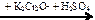
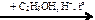 X3
X3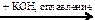 Х1 → C2H2 → К2C2O4 → Н2C2O4
Х1 → C2H2 → К2C2O4 → Н2C2O4 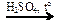 X2
X2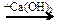 X1
X1 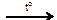
 X → C2H4
X → C2H4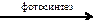 X1
X1 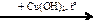 X2
X2


