
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Лабораторное получение спиртовСодержание книги Поиск на нашем сайте
1. Гидролиз галогеналканов с помощью водного раствора щелочи: С3Н7Cl + KOH = C3H7OH + KCl 2. Двухатомные спирты образуются при окислении алкенов перманганатом калия в нейтральной или щелочной среде (эта реакция знакома вам как качественная реакция на алкены):
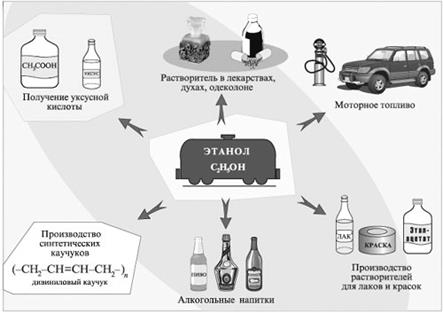
Применение этанола Применение этанола представлено на рисунке 2.
Рис. 2. Применение этанола Получение синтетического каучука по методу Лебедева:
Применение многоатомных спиртов и фенола Рассмотрите рис. 3. применение многоатомных спиртов.
Рис. 3. Применение многоатомных спиртов Применение фенола · Получение полимеров, в том числе фенолформальдегидных смол:
· Получение искусственных волокон, лекарств, пестицидов. · Антисептик. Реакция со щелочными металлами
Рис. 1. Реакция натрия со спиртом (фото В.В. Загорского) Спирт и вода в реакциях с натрием отдают ион водорода, т.е. в данной реакции они проявляют кислотные свойства. Продукт реакции спирта с натрием – соль (Рис. 1). Общее название солей спиртов – алкоголяты. Реакции спиртов со щелочными металлами довольно широко используются в лабораторной практике. Остатки щелочных металлов опасно уничтожать, вводя их в реакцию с водой, поскольку вода очень активно взаимодействует с ними. Поэтому чаще всего для этих целей используют этиловый спирт. Реакция со щелочами CH3CH2–O–H+NaOH Реакция не идет! Причина: спирт – более слабая кислота, чем вода, и не может вытеснить воду. Алкоголяты вступают в обратную реакцию: CH3–CH2–ONa+Н2О → CH3–CH2–OH+NaOH CН3СН2ОNa этилат натрия. В чем причина различия активности воды и спиртов? Причина кислотных свойств воды и спиртов – высокая полярность связи О-Н:
Чем больше величина положительного заряда на атоме водорода, тем легче вещество будет отдавать протон и, следовательно, сильнее проявлять кислотные свойства. Чем разветвленнее углеводородный радикал, тем менее полярна связь О-Н и меньше кислотные свойства спирта: НОН > CH3OH > CH3-CH2OH > (CH3)2-CHOH > (CH3)3-COH Включение в молекулу спирта электроотрицательного атома делает увеличение полярности связи О-Н и, как следствие, усиление кислотных свойств: Cl-CH2-CH2OH > CH3OH СН2ОН-СНОН-СН2ОН > ОН-CH2-CH2OH > Cl-CH2-CH2OH Основные свойства спиртов Что происходит с водой, если к ней добавить кислоту? 1. В результате диссоциации кислоты образуется ион водорода: HCl 2. Ион водорода присоединяется к неподеленной электронной паре атома кислорода воды. Образуется ион гидроксония:
ион гидроксония Вода в данной реакции выступает основанием, т.к. присоединяет ион водорода.
|
||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 246; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.15 (0.008 с.) |


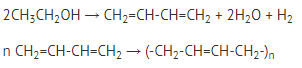




 CH3CH2–O–Na+H2O
CH3CH2–O–Na+H2O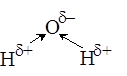

 H+ +Cl-
H+ +Cl- + H+
+ H+ 




