Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Строение карбоксильной группы
Карбоксильная группа сочетает в себе две функциональные группы – карбонил >C=O и гидроксил -OH, взаимно влияющие друг на друга:
Для насыщенных монокарбоновых кислот характерна высокая химическая активность. Это определяется, главным образом, реакциями карбоксильной группы (разрыв связей O - H или C - O), а также реакциями замещения H -атомов при α-С атоме. Химические свойства предельных карбоновых кислот.
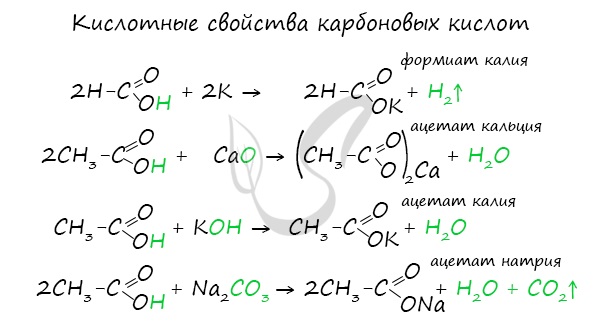
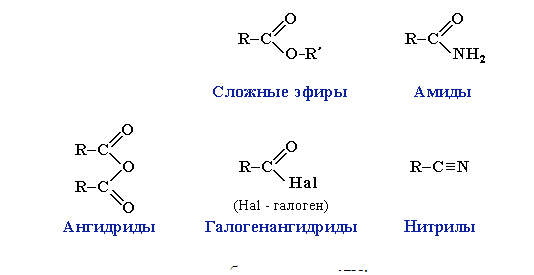
-Сила кислот уменьшается в ряду: H - COOH > CH 3 - COOH > CH 3 - CH 2 - COOH а) изменяют окраску индикаторов, лакмус краснеет б) взаимодействуют с металлами до H 2: 2R-COOH + 2Na → 2R-COONa + H2↑ в) взаимодействуют с основными оксидами и основаниями: 2R-COOH + CaO → (R-COO)2Ca + H2O R-COOH + NaOH → R-COONa + H2O г) Взаимодействуют с солями слабых кислот: R-COOH + NaHCO3 → R-COONa + H2O + CO2↑ Соли карбоновых кислот разлагаются сильными минеральными кислотами и водой: R-COONa + H С l → NaCl + R-COOH R-COONa + H2O → NaOH + R-COOH Например:
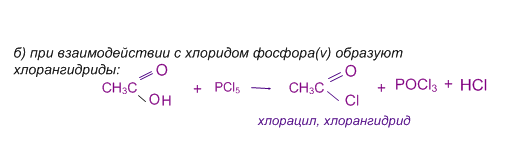
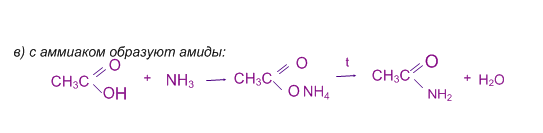
карбоновые кислоты образуют функциональные производные:
а) со спиртами образуют сложные эфиры:
или
II. Свойства, обусловленные радикалом 1.По месту разрыва связи С-H дают реакции замещения в α- положении:
При появлении атома галогена в радикале сила кислот нарастает.
Муравьиная кислота обладает двойственной природой свойств, так как представляет собой сочетание двух функциональных групп: карбоксильной и альдегидной. 1. Обладает общими свойствами кислот. 2. Как альдегид: а) даёт реакцию «серебряного зеркала»: б) вступает в реакцию с гидроксидом меди(II): H-COOH + 2Cu(OH)2 t → Cu2O↓ + CO2↑ + 3H2O в) окисляется хлором: H-COOH + Cl2 → CO2 + 2HCl 3. Особые свойства: а) разлагается при нагревании в присутствии серной кислоты: HCOOH t , H 2 SO 4 → CO↑ + H2O б) не образует ангидрида. Получение карбоновых кислот Общие способы I.Окисление 1) алканов 2CH4 + + 3O2 t , kat → 2HCOOH + 2H2O метан муравьиная кислота 2CH3-CH2-CH2-CH3 + 5O2 t,kat,p → 4CH3COOH + 2H2O н-бутан уксусная кислота 2) алкенов: CH2=CH2 + O2 t,kat → CH3COOH этилен СH3-C≡C- СH3 + 8KMnO4 + 12H2SO4 → 10CH3-COOH + 4K2SO4 + 8MnSO4 + 12H2O 3) алкинов: СH3-CH=CH-СH2 -СH3+ KMnO4 + 1H2SO4 → 4) окисление гомологов бензола (получение бензойной кислоты): 5C6H5-CH3 + 6KMnO4 + 9H2SO4 → 5C6H5-COOH + 3K2SO4 + 6MnSO4 + 14H2O
5. окисление первичных спиртов, альдегидов и кетонов: R-CH2-OH → R-COH → R-COOH II. Гидролиз 1) солей карбоновых кислот: R-COONa + H2О → R-COOH + NaOH или R-COONa + HCl → R-COOH + NaCl 2) сложных эфиров:
Ангидридов карбоновых кислот: (R-CO)2O + H2O → 2 R-COOH 4) гидролиз галогенангидридов карбоновых кислот: С H3-CO-Cl + H2 О → С H3-COOH + HCl или
щелочной гидролиз:
5) гидролиз амидов: С H3-CO-NH2 + H2 О → С H3-COONH4 С H3-COONH4 + HCl → С H3-COOH + NH4Cl
6) гидролиз нитрилов (цианидов): R-Br + NaC≡N → R- C≡N +NaBr R- C≡N +2H2 О → С H3-COONH4 С H3-COONH4 + HCl → С H3-COOH + NH4Cl
|
|||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 124; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.69.152 (0.008 с.) |



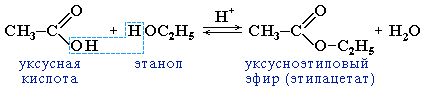
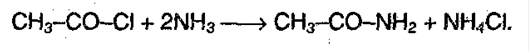
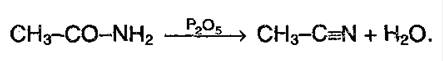 нитрил
нитрил


 Особенности муравьиной кислоты H - COOH:
Особенности муравьиной кислоты H - COOH: