Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
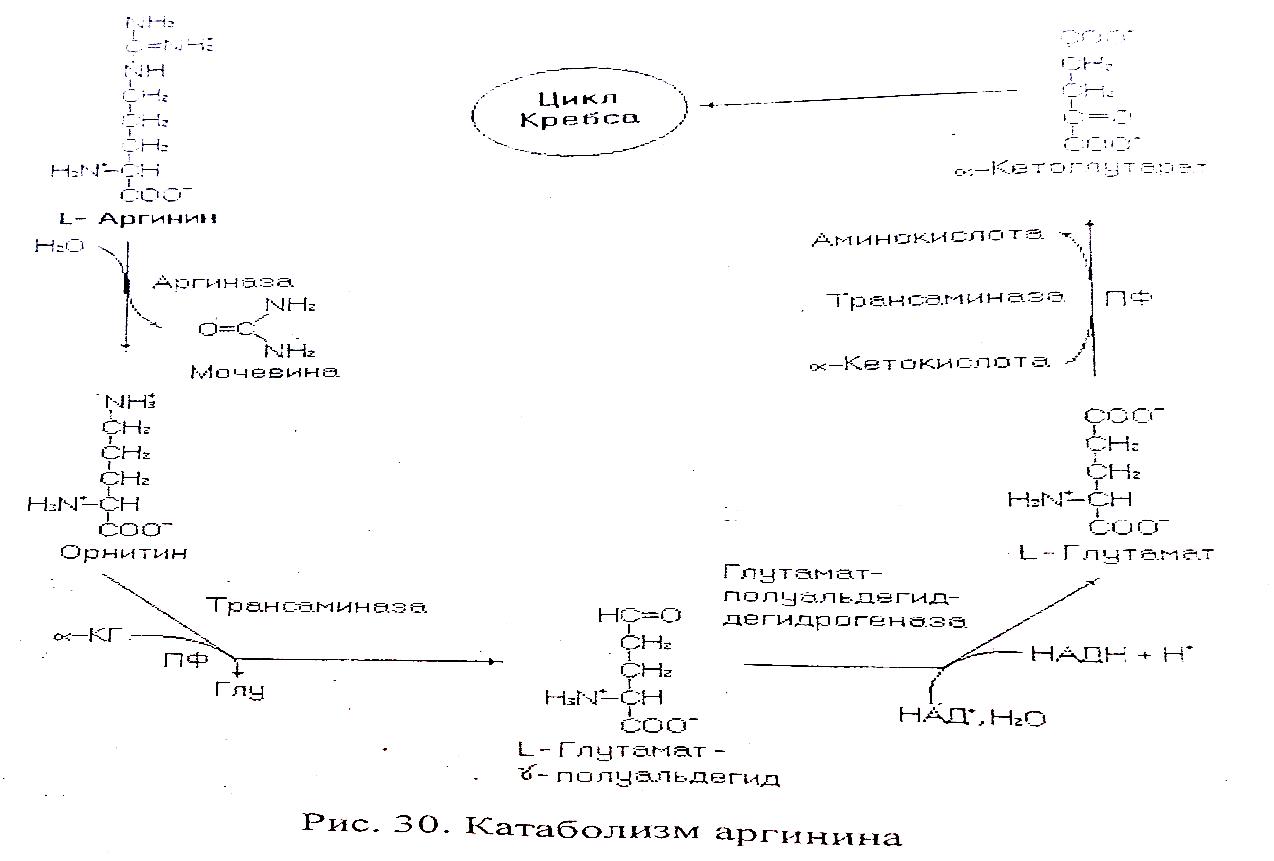
Метаболизм аргинина. Окисление аргинина до конечных продуктов, биоэнергетика процесса. Орнитиновый цикл.
АРГИНИН: 1) частично заменимая аминокислота (может синтезироваться в орнитиновом цикле) 2) гликогенная 3) с положительно заряженным радикалом
1.в организм поступает с пищей 2. образуется при протеолизе эндогенных белков и в орнитиновом цикле 3. входит состав ядерных белков – гистонов 4. в ферментах – остатки аргинина участвуют в формировании и функционировании их активного центра 5. одна из важнейших реакций для организма с участием аргинина – реакция образования оксида азота (NO – первичный мессенджер, он взаимодействует с геном гунилатциклазы, и приводит образованию цГМФ (вторичного мессенджера)-расширяет сосуды, снижает частоту сердечных сокращений.) NO – регулирует апоптоз, предотвращает агрегацию тромбоцитов, выполняет функцию нейромедиатора, препятствует развитию опухолей. 6. аргинин – используется в синтезе биогенных аминов (путресцина, спермина, спермидина), креатинфосфата 7. у микроорганизмов аргинин используется в синтезе аргининфосфата 8. при декарбо ксилировании аргинина образуется агматин 9. углеводородный скелет аргинина может участвовать в синтезе углеводородов, липидов, аминокислот и др. соединений. 10. при нарушении всасывания аргинина и некоторых аминокислот – заболевание – гипераргинемия – увеличение концентрации аргинина в крови КАТАБОЛИЗМ АРГИНИНА
α- Кетоглутарат окисляется ч/з 2,5 оборота ЦТК. Биоэнергетика окисления аргинина – 22 молекулы АТФ Орнитиновый цикл Мочевина - основной конечный продукт азотистого обмена В 40-х годах XX века немецкие биохимики Г. Кребс и К. Гензелейт установили, что синтез мочевины представляет собой циклический процесс, состоящий из нескольких стадий, ключевым соединением которого, замыкающим цикл, является орнитин. Поэтому процесс синтеза мочевины получил название "орнитиновый цикл".
Далее под действием орнитинкарбамоилтрансферазы карбамоильная группа карбамоилфосфата переносится на α-аминокислоту орнитин, и образуется другая α-аминокислота - цитруллин
В следующей реакции аргининосукцинатсинтетаза связывает цитруллин с аспартатом и образует аргининосукцинат (аргининоянтарную кислоту). Этот фермент нуждается в ионах Mg2+. В реакции затрачивается 1 моль АТФ, но используется энергия двух макроэргических связей. Аспартат - источник второго атома азота мочевины Далее фермент аргининосукцинатлиаза (аргининосукциназа) расщепляет аргининосукцинат на аргинин и фумарат, при этом аминогруппа аспартата оказывается в молекуле аргинина Аргинин подвергается гидролизу под действием аргиназы, при этом образуются орнитин и мочевина. Кофакторами аргиназы являются ионы Са2+ или Мn2+. Высокие концентрации орнитина и лизина, являющихся структурными аналогами аргинина, подавляют активность этого фермента: Образующийся орнитин взаимодействует с новой молекулой карбамоилфосфата, и цикл замыкается. Первые две реакции процесса происходят в митохондриях гепатоцитов. Затем цитруллин, являющийся продуктом этих реакций, транспортируется в цитозоль, где и осуществляются дальнейшие превращения
Метаболизм гистидина. Альтернативные пути катаболизма гистидина. Образование гистамина и его роль в организме. ГИСТИДИН: 1)частично заменимая 2)гликогенная 3) с положительно заряженным радикалом
МЕТАБОЛИЗМ:
1) организм взрослого человека может продолжительное время существовать без поступления этой аминокислоты с пищей, однако растущий организм в ней нуждается 2) радикалы гистидина участвуют в формировании третичной структуры белков 3) некоторые ферменты содержат радикалы гистидина в каталитическом участке активного центра 4)остатки гистидина играют роль также в молекуле гемоглобина – каждая из четырех полипептидных цепей присоединена к молекуле гемма ч/з координационную связь м/уазотом имидазола гистидина протомера и железом гемма. 5) ряд остатков гистидина гемоглобина участвуют в транспорте протонов от периферических тканей к легким, т.к. легко присоединяют и легко отдают протоны 6) др остатки гистидина в гемоглобине участвуют в связывании 2,3- дифосфоглицерата – регулирует сродство гемоглобина к кислороду
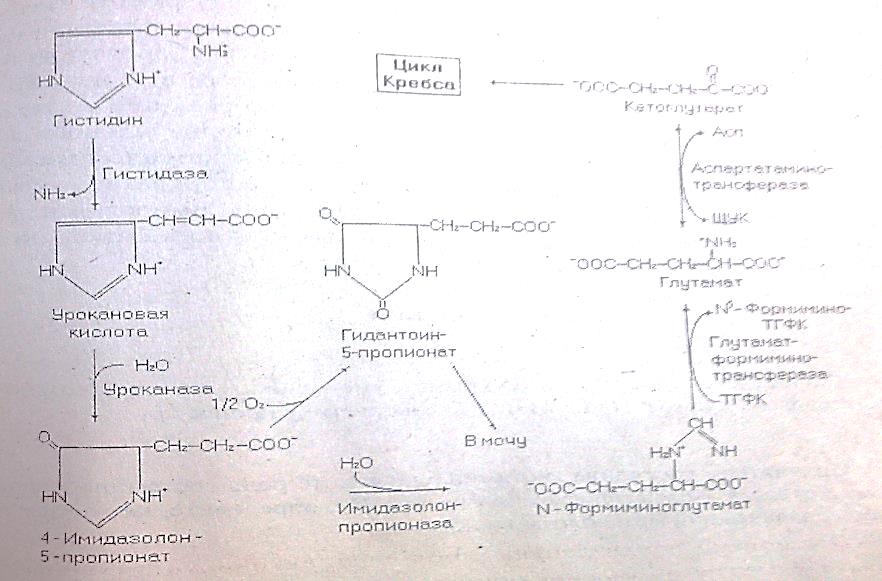
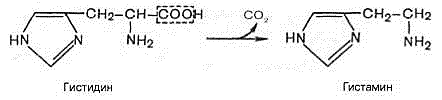
7) гистидин используется в синтезе дипептидов карнозина и ансерина (они – полуфункциональные молекулы, выполняют буферную функцию, защищают клетки от действия активных форм кислорода, замедляют старение организма, активируют гуанилатциклазу) 8)в головном мозге человека присутствует гомокарнозин, который синтезируется из гистидина и y-аминомасляной кислоты. 9) существуют 2 пути катаболизма гистидина:1-гистидин преобразуется до гидантоин-5-пропионовой кислоты, в виде которой поступает в мочу; 2-гистидин трансформируется до α-кетоглутаровой кислоты, дальнейшее окисление в цикле Кребса и цепи переноса электронов 10) БИОЭНЕРГЕТИКА: окисления гистидина ч/з цикл Кребса и ЦПЭ (цепь переноса электронов) – 23,5 мол АТФ (с учетом обезвреживания аммиака в орнитиновом цикле и трансаминазной реакции) или 26 мол АТФ (с учетом обезвреживания аммиака в орнитиновом цикле и глутаматдегидрогеназной реакции) Декарбоксилирование гистидина приводит к образованию гистамина (фермент – декарбоксилаза ароматическихL-аминокислот, неспецифических по отношению к гистидину ферментом) Гистамин выполняет функцию нейромедиатора в нервной ткани и медиатора в других тканях, депонируется в тучных клетках соединительной ткани базофильных гранулоцитах крови, участвует в развитии аллергических и воспалительных реакций. Высвобождение гистамина из его депо стимулируют тканевые гормоны, некот-ые лекарственные препараты и аллегрены. Гистамин стимулирует сокращение гладких мышц бронхов (ч/з Н1 рецептор), расширяет капилляры и повышает их проницаемость; ч/з Н2 рецептор стимулирует образование HCl в желудке и замедляет сердечный ритм, а ч/з Н3 рецептор активирует ЦНС. В организме гистамин быстро разрушается, превращаясь а имидазолацеториботид, который удаляется с мочой Метаболизм метионина. Образование S -аденозилметионина и его участие в реакциях метилирования. Катаболизм метионина до конечных продуктов, биоэнергетика процесса. МЕТИОНИН: 1)гликогенная
3) с неполярным радикалом
S-аденозилметионин (SАМ) – активная форма метионина 1) образуется в реакции метионина с АТФ 2) участвует в реакциях метилирования 3) метилированию подвергаются – нуклеиновые кислоты, белки, гормоны и др. (метилирование нукл кислот по азотистым основаниям защищает их от действия нуклеаз, ферментов, гидролизирующих нукл кислоты) 4) участвуя в реакциях метилирования, SАМ преобразуется до сукцинил-КоА
5) преобразование SАМ в сукцинил-КоА тормозится при недостатке метионина (она незаменимая АК). В этом случае происходит регенерация метионина из гомоцистеина (промежуточный продукт катаболизма SАМ) Катаболизм
БИОЭНЕРГЕТИКА: окисление метионин сукцинил-КоА ЦТК – 26 мол АТФ, но с учетом предыдущих этапов и затрат на нейтрализацию аммиака энергетический баланс – 19,5 мол АТФ
|
||||||
|
Последнее изменение этой страницы: 2021-05-27; просмотров: 288; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.143.4.181 (0.012 с.) |
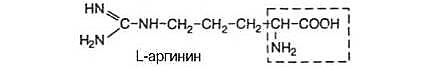
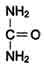 Мочевина (карбамид) - полный амид угольной кислоты - содержит 2 атома азота. Источником одного из них является аммиак, который в печени связывается с диоксидом углерода с образованием карбамоилфосфата под действием карбамоилфосфатсинтетазы I.
Мочевина (карбамид) - полный амид угольной кислоты - содержит 2 атома азота. Источником одного из них является аммиак, который в печени связывается с диоксидом углерода с образованием карбамоилфосфата под действием карбамоилфосфатсинтетазы I.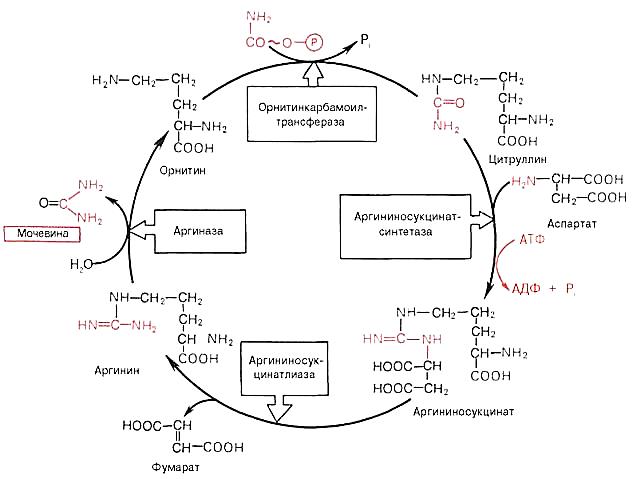
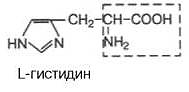

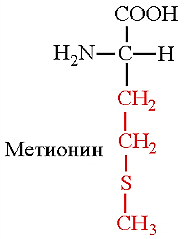 2)незаменимая
2)незаменимая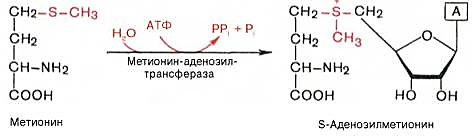
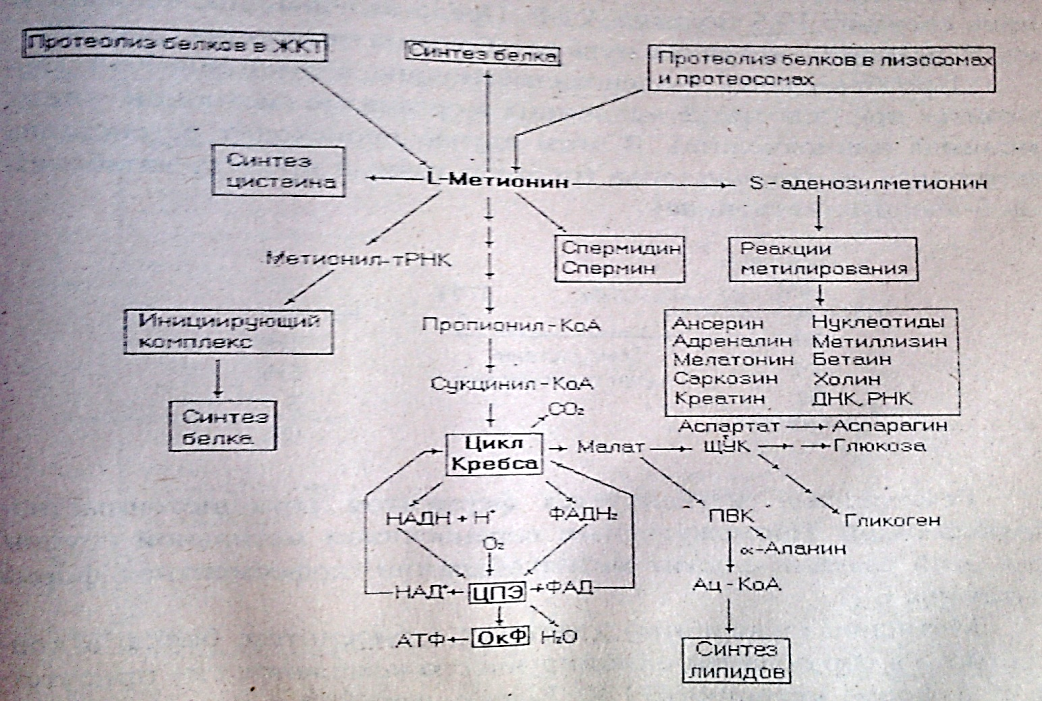 метаболизм
метаболизм